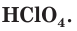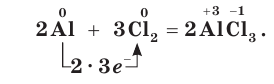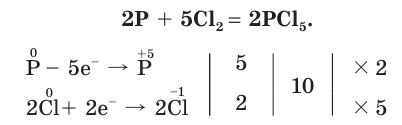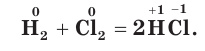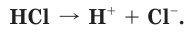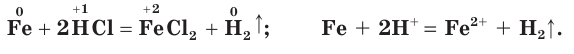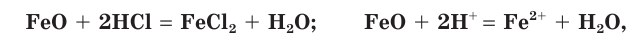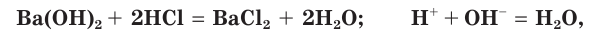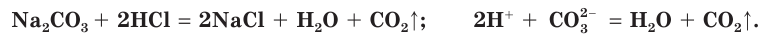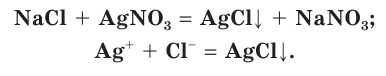Содержание:
Хлор — химический элемент и простое вещество:
Химические элементы с наиболее ярко выраженными неметаллическими свойствами в периодической системе составляют VIIА-группу: фтор F, хлор Cl, бром Br, иод I и очень редко встречающийся в природе астат At. Эти элементы называются галогенами.
Хлор в природе
Наиболее распространенным в природе галогеном является хлор. Его массовая доля в земной коре составляет около 0,2 % — 11-е место по распространенности среди всех элементов. Широко распространены минералы и горные породы, содержащие хлориды, — соли соляной кислоты: галит (каменная или поваренная соль) NaCl, сильвин KCl, карналлит
Хлор — один из химических элементов, без которых немыслимо существование живых организмов. Ионы хлора вместе с ионами натрия и калия регулируют водно-солевой обмен в организме человека. Хлор участвует в энергетическом обмене у растений, положительно влияет на поглощение корнями кислорода, а также соединений калия, кальция, магния.
Химический элемент хлор
Охарактеризуем хлор по плану, который вы применяли в 8-м классе.
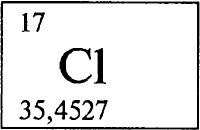
Химический знак — Cl, относительная атомная масса — 35,5, атомный номер — 17. Этот элемент находится в третьем периоде в VIIА-группе.
Заряд ядра атома хлора равен 17+, следовательно, ядро содержит 17 протонов, а ядра двух его природных нуклидов 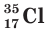
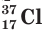
В атоме хлора 17 электронов, которые располагаются на трех электронных слоях: 17Cl 2e– , 8e– , 7e– .
На внешнем (незавершенном) электронном слое у атомов хлора находится по 7 электронов, следовательно, этот элемент относится к неметаллам. Максимальная положительная степень окисления хлора равна +7, формула его высшего оксида — 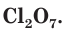
Степень окисления хлора в летучем водородном соединении равна –1, формула этого соединения — HCl.
Простое вещество
Хлор является веществом молекулярного строения. Его молекула состоит из двух атомов — 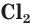
При обычных условиях хлор — желто-зеленый газ с резким запахом. Он в 2,5 раза тяжелее воздуха, ядовит. В Первую мировую войну хлор использовался даже в качестве боевого отравляющего вещества.
Растворимость хлора в воде небольшая: в одном объеме воды при 20 °С растворяется 2,5 объема хлора. Водный раствор хлора называется хлорной водой.
Химические свойства
Хлор является химически активным простым веществом. Он взаимодействует практически со всеми простыми веществами, за исключением кислорода, азота и благородных газов, образуя хлориды. С металлами хлор реагирует при слабом нагревании, а с некоторыми даже при обычных условиях, выступая в качестве окислителя:
Как окислитель хлор реагирует с менее электроотрицательными неметаллами:
Хлор своеобразно реагирует с водородом. При обычной температуре в темноте реакция не происходит, но при сильном освещении или при нагревании смесь хлора и водорода может взорваться.
С большинством сложных веществ хлор также ведет себя как окислитель. Взаимодействуя с растворами бромидов и иодидов металлов, хлор вытесняет из них бром и иод:
Приведенные выше реакции подтверждают, что простое вещество хлор проявляет более сильные окислительные свойства, чем нижестоящие в группе галогены.
Применение хлора
По масштабам промышленного применения хлор намного превосходит все остальные галогены (рис. 36). В больших количествах хлор используется для обеззараживания питьевой воды. Хлор и его соединения применяются для отбеливания льняных и хлопчатобумажных тканей, бумаги, древесины и т. д. Особенно много его расходуется при производстве пластмасс, каучуков, красителей, различных растворителей. Огромны масштабы использования хлора в производстве соляной кислоты.
Хлор является самым распространенным галогеном.
Минимальная отрицательная степень окисления хлора равна –1, максимальная положительная — +7.
При обычных условиях простое вещество хлор — желто-зеленый газ с резким запахом, тяжелее воздух, ядовит.
Хлор взаимодействует непосредственно практически со всеми простыми веществами, за исключением кислорода, азота и благородных газов, а также со многими сложными веществами, выступая обычно в качестве окислителя.
Хлороводород и соляная кислота
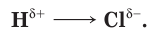
Одним из важнейших соединений хлора является продукт его взаимодействия с водородом — хлороводород HCl. Это бесцветный газ с резким запахом, несколько тяжелее воздуха. Химическая связь в молекуле HCl — ковалентная полярная:
Молекула хлороводорода HCl полярна и представляет собой диполь.
Хлороводород очень хорошо растворяется в воде. Это легко проверить, если цилиндр, заполненный этим газом, опустить в чашку с водой (куда заранее было внесено несколько капель лакмуса). Вода быстро поднимется вверх, при этом раствор окрасится в красный цвет, что является свидетельством образования в цилиндре кислого раствора (рис. 37).
Соляная кислота
Раствор хлороводорода в воде — хлороводородная кислота, которую на практике чаще называют соляной кислотой. Это бесцветная жидкость с резким запахом. В концентрированной кислоте массовая доля HCl составляет около 37 %.
Соляная кислота является сильной одноосновной кислотой, в разбавленном растворе полностью диссоциирует на ионы:
Соляная кислота проявляет характерные для кислот свойства. Она изменяет окраску индикаторов: лакмус и метилоранж в растворе HCl становятся красными. Соляная кислота взаимодействует с теми металлами, которые в ряду активности металлов расположены до водорода:
В этих реакциях ионы водорода выступают в качестве окислителя. Соляная кислота взаимодействует с основными оксидами:
со щелочами и нерастворимыми основаниями:
а также с солями:
Реакции с солями идут только тогда, когда образуются осадок, газ или слабый электролит.
В организме человека соляная кислота вырабатывается клетками слизистой оболочки желудка и входит в состав желудочного сока. Массовая доля HCl в желудочном соке человека равна 0,3 % — 0,5 %. Соляная кислота в составе желудочного сока улучшает пищеварение, уничтожает большинство бактерий, которые попадают с пищей в желудок, что замедляет или даже останавливает гнилостный процесс. Желудок здорового человека вырабатывает до 2,5 дм3 желудочного сока в сутки. Желудочный сок начинает выделяться уже тогда, когда вы начинаете пережевывать пищу. Поэтому жевать жевательную резинку на голодный желудок вредно: в отсутствии пищи соляная кислота разрушительно действует на стенки желудка.
Продуктом взаимодействия хлора с водородом является хлороводород — бесцветный газ с резким запахом, тяжелее воздуха.
Раствор хлороводорода в воде представляет собой кислоту, которая называется хлороводородной или соляной.
Соляная кислота проявляет все типичные свойства кислот: взаимодействует с основаниями, основными оксидами, солями и металлами, стоящими в ряду активности до водорода.
Хлориды
Соли соляной кислоты называются хлоридами. Большинство хлоридов растворимы в воде. Так, например, большая часть растворенных в морской воде солей приходится на хлорид натрия. Объясняется это тем, что соли вымываются из горных пород и выносятся реками в моря и океаны. Но в засушливых и пустынных районах в результате интенсивного испарения воды концентрация солей в воде сильно повышается, и они выделяются в твердом виде. Так образуются солончаки (рис. 38).
Растворы хлоридов — обязательная составная часть живых организмов. В теле взрослого человека содержится примерно 200 г хлорида натрия, причем, около 45 г растворено в крови. Соль поддерживает нормальную деятельность клеток, из которых состоят все ткани и органы. Взрослому человеку необходимо получать в день примерно 5—6 г хлорида натрия, включая и ту соль, которая входит в состав готовых продуктов. Употребление избыточного количества поваренной соли приводит к ухудшению самочувствия: появлению головной боли, отекам, повышению артериального давления.
К практически нерастворимым хлоридам относится хлорид серебра(I) AgCl. Это свойство хлорида серебра(I) используется для обнаружения хлорид ионов в растворе. При добавлении к соляной кислоте или к раствору хлорида натрия раствора нитрата серебра(I) 
Такая реакция является качественной реакцией на ионы хлора, а нитрат серебра(I) служит реактивом на соляную кислоту и ее соли.
Если содержание хлорид-ионов в растворе невелико, то осадок не выпадает, а наблюдается помутнение раствора. Этой реакцией можно пользоваться для проверки наличия хлоридионов в питьевой воде.
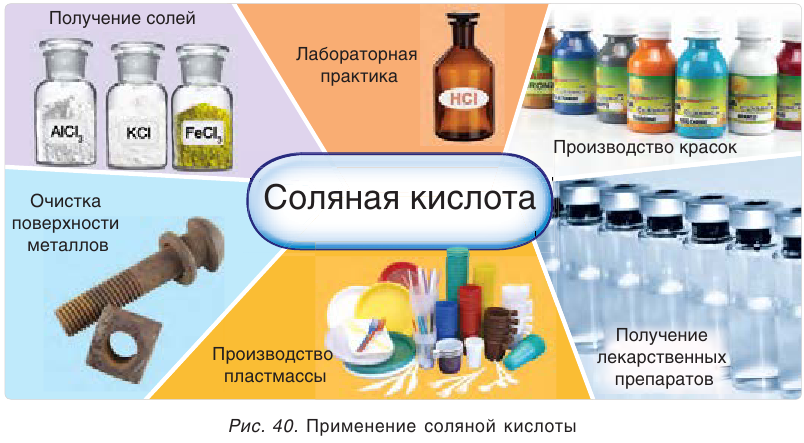
Применение соляной кислоты и хлоридов
Соляная кислота и ее соли относятся к тем веществам, которые постоянно сопровождают человека, являясь неотъемлемой частью его жизни. В больших объемах соляная кислота расходуется в самых разнообразных областях практической деятельности человека: в химической, пищевой
и фармацевтической промышленности, для обработки поверхности металлов и др. Как реагент соляная кислота используется во всех химических лабораториях (рис. 40).
Важнейшими солями соляной кислоты являются хлориды натрия и калия. Поваренная соль NaCl известна как пищевая добавка, которая служит консервантом при подготовке пищевых продуктов к длительному хранению.
Поваренная (каменная) соль издавна ценилась очень высоко. Ею вместо денег платили жалованье римским воинам и крестоносцам. В Китае изготавливали соляные монеты, на которых ставилось клеймо правителя. А в Эфиопии еще в XIX в. были в ходу соляные деньги — стандартные бруски каменной соли (см. рис.).
Хлорид натрия используют для профилактики и лечения простудных заболеваний. Посещение соляных пещер, воздух в которых чрезвычайно богат аэрозолем хлорида натрия, оказывает положительное влияние на состояние дыхательных путей и кожи детей и взрослых (рис. 41). Водный раствор хлорида натрия широко применяется в медицине для приготовления различных лекарственных препаратов.
Хлориды натрия и кальция используют для борьбы с гололедицей, а NaCl — в производстве химических препаратов, стекла и бумаги.
Хлорид калия KCl — ценное минеральное удобрение. Это основной экспортный продукт химической промышленности Беларуси (рис. 42). Хлориды других металлов используются в сельском хозяйстве, химической промышленности, медицине.
- Соли соляной кислоты называются хлоридами.
- Реактивом на соляную кислоту и ее соли служит раствор нитрата серебра(I).
- Соляная кислота и хлориды имеют важное значение для жизнедеятельности живых организмов.
Хлор
Химический элемент
Желтовато-зелёный газ
| Атомная масса | 35,457 а.е.м. |
| Электронная конфигурация | [Ne] 3s2 3p5 |
| Электроотрицательность | 3,16 по шкале Поллинга |
| Степени окисления | 7; 6; 5; 4; 3; 1; 0; −1 |
| Температура плавления | 172,2 K |
| Температура кипения | 238,6 K |
| Структура кристаллической решетки | орторомбическая |
| Теплопроводность | (300 K) 0,009 Вт/(м·К) |
Хлор — химический элемент № 17 в таблице Менделеева. Относится к галогенам, в нормальных условиях — ядовитый газ желтовато-зелёного цвета.
[править] История
Впервые хлор был получен в 1774 году шведским химиком Карлом Шееле. Он описал выделение хлора при взаимодействии пиролюзита с соляной кислотой в своем трактате о пиролюзите:
- 4HCl + MnO2 = Cl2 + MnCl2 + 2H2O.
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, согласно господствующей тогда в химии теории флогистона, предположил, что хлор представляет собой дефлогистированую соляную кислоту, то есть оксид соляной кислоты. Бертолле и Лавуазье предположили, что хлор является оксидом элемента мурия, однако попытки его выделения оставались тщетными до времени работ Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор. В 1810 году ученый Г. Дэви выразил мнение, что этот газ является простым веществом. Через 2 года французский химик и физик Жозеф-Луи Гей-Люссак дал этому газу современное название хлор.
Название происходит от греческого χλωρός — «зеленый».
[править] Распространение в природе
Хлор — достаточно распространенный элемент. В свободном состоянии в природе он не встречается, так как в химическом отношении хлор очень активен. Самым распространенным природным соединением хлора является хлорид натрия NaCl, огромные количества которого растворены в воде морей, океанов и некоторых озер. Во многих местах хлорид натрия в виде минерала галита (или каменной соли) образует мощные залежи. Богатые залежи очень чистой каменной соли расположены в районах Соль-Илецка на Южном Урале и Артёмовска на Донбассе.
Кроме того, очень распространенными соединениями хлора является хлорид калия KCl и хлорид магния MgCl2. Хлорид калия и хлорид натрия образуют минерал сильвинит KCl·NaCl, мощные месторождения которого расположены на Украине (города Калуш и Стебник), а хлорид калия и хлорид магния образуют минерал карналлит KCl·MgCl2·6H2O, большие залежи которого имеются на Урале.
[править] Физические свойства
Хлор — тяжелый газ желтовато-зеленого цвета с резким, удушливым запахом, неметалл. При вдыхании очень раздражает слизистую оболочку и вызывает острый кашель, а в больших количествах — даже смерть.
Под давлением около 6 атмосфер хлор уже при обычной температуре сжижается в желтую тяжелую жидкость, которая под нормальным давлением кипит при −34 °С, а при −102,4 °С замерзает в желтоватую кристаллическую массу. Сжиженный хлор хранят и транспортируют в стальных баллонах.
В воде хлор растворяется хорошо. В одном объеме воды при обычной температуре растворяется более двух объемов хлора. Раствор хлора в воде называют хлорной водой.
[править] Химические свойства
Химически очень активен. Окислитель. Образует соединения почти со всеми элементами. Атомы хлора, имея во внешнем электронном слое семь электронов, легко отнимают валентные электроны от атомов других элементов и превращаются в отрицательно одновалентные ионы Cl−. Этим проявляются его резко выраженные окислительные свойства. По своим окислительным свойствам хлор уступает только фтору и примерно равноценен кислороду. Благодаря большому родству его атомов к электрону, хлор непосредственно соединяется со всеми металлами и большинством неметаллов. Причем со многими металлами он реагирует очень энергично с выделением тепла и света. Например, если в наполненный хлором цилиндр внести растертый в порошок сурьмы, он вспыхивает и сгорает, образуя густой белый дым трихлорида сурьмы SbCl3:
- 2Sb + 3Cl2 = 2SbCl3
Предварительно нагретые кальций, железо, медь и другие металлы тоже энергично сгорают в атмосфере хлора, образуя соответствующие хлориды. Например:
- Cu + Cl2 = CuCl2
Зажженый на воздухе красный фосфор продолжает энергично гореть в атмосфере хлора:
- 2Р + 3Cl2 = 2PCl3
С водородом хлор тоже реагирует. Но при обычной температуре реакция идет очень медленно, а при нагревании и под воздействием солнечного света — достаточно быстро и даже со взрывом:
- Cl2 + Н2 = 2HCl
[править] Реакции с органическими соединениями
[править] Замещения
При высокой температуре хлор может отнимать водород от различных органических соединений. Зажженная свеча продолжает гореть в атмосфере хлора, выделяя много копоти, потому что с хлором сочетается только водород, входящий в состав вещества свечи, а углерод выделяется в виде копоти:
- CnH2n+2 + (n+1) Cl2 → n C + (2n+2) HCl
Алканы реагируют с хлором при нагревании, реакция проходит по радикальному механизму:
- CH3-CH3 + Cl2 → C2H6-xClx + HCl
Ароматические соединения реагируют по ионному механизму, в присутствии катализаторов (например, AlCl3, FeCl3):
- C6H6 + Cl2 → C6H5Cl + HCl
Кетоны хлорируются гораздо легче, чем соответствующие алканы:
- CH3-CH2-CO-CH2-CH3 + Cl2 -H+→ CH3-CHCl-CO-CH2-CH3 + HCl
- CH3-CH2-CO-CH2-CH3 + 4Cl2 -OH—→ CH3-CCl2-CO-CCl2-CH3 + 4HCl
С метилкетонами реакция идет дальше и происходит расщепление
- CH3-CO-CH3 — Cl2/-OH—→ CHCl3
[править] Присоединения
Хлор присоединяется по двойной связи алкенов
- CH2=CH2 + Cl2 → Cl-CH2-CH2-Cl
[править] Окисления
Хлор — сильный окислитель, и редко применяется в этом качестве. Он окисляет спирты (до кислот или кетонов), альдегиды (до кислот).
- CH3-CH2-OH —Cl2 / OH—→ [CH3-CHO] →CHCl3
[править] Получение
В лабораторных условиях хлор обычно получают взаимодействием соляной кислоты HCl с двуокисью марганца MnO2 (это также и первый промышленный метод получения):
- 4HCl + MnO2 → MnCl2 + Cl2 ↑ + 2H2O
Также используют другие окислители:
- 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
- K2Cr2O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2O
[править] Промышленное производство
В технике хлор получают электролизом водного раствора хлорида натрия NaCl. Хлорид натрия в водном растворе диссоциирует на ионы натрия и хлора:
- NaCl ⇌ Na+ + Cl−
Молекулы воды также частично диссоциируют:
- H2O ⇌ H+ + OH−
Таким образом, к катоду привлекаются катионы натрия и катионы водорода, а к аноду — анионы хлора и анионы гидроксила. Катионы водорода восстанавливаются легче, чем катионы натрия, а анионы хлора окисляются легче, чем анионы гидроксила. Поэтому на катоде выделяется водород, а аноде — хлор. Электродные реакции можно обозначить такими уравнениями:
- Катод: 2Н+ + 2е = Н2↑
- Анод: 2Cl− − 2е = Cl2↑
Катионы натрия и анионы гидроксила все время накапливаются в растворе и образуют гидроксид натрия NaOH. Он реагирует с хлором, частично растворяется в воде, образуя гипохлорит и хлорид натрия
- NaOH + Cl2 → NaCl + NaOCl
Раствор NaClO используют как отбеливатель.
[править] Применение
В технике хлор применяется очень широко. Используют в производстве хлорорганических соединений (например, винилхлорида, хлоропренового каучука, дихлорэтана и др.), красителей, лекарственных и других веществ, для отбеливания ткани, бумаги, дезинфекции и т. п.
Значительные количества его используют для производства:
- соляной кислоты
- хлорной извести
Применение хлора для обеззараживания (хлорирования) питьевой воды пытаются ограничить и заменить озонированием, но на сегодня оно является основным в большинстве стран.
В металлургии хлор применяют для хлорирования руд для получения целого ряда цветных и редких металлов — титана, ниобия, тантала и других — в виде их хлоридов, из которых затем электролизом добывают чистые металлы.
Много хлора потребляет химическая промышленность для получения различных хлорорганических соединений, используемых для борьбы с вредителями и сорняками в сельском хозяйстве, а также для изготовления различных красителей, синтетического каучука, пластмасс и т. п. Самыми известными из них являются:
- Винилхлорид и его полимер поливинилхлорид (ПВХ), который применяется для производства оконных профилей
- Хлороформ
- ДДТ (снято с производства и запрещено к употреблению из-за токсичности)
- Диоксины
[править] Действие на человека
Ядовит. ПДК в воздухе производственных помещений 1 мг/м3, в атмосфере населенных пунктов одноразовая (кратковременная) — 0,1 мг/м3, среднесуточная — 0,003 мг/м3. Защититься от хлора можно с помощью гражданских или промышленных противогазов.
[править] Литература
- Глоссарий терминов по химии // Й.Опейда, О.Швайка. Ин-т физико-органической химии и углехимии им. Л. М. Литвиненко НАН Украины, Донецкий национальный университет — Донецк: «Вебер», 2008. — 758 с. ISBN 978-966-335-206-0
- Горный энциклопедический словарь: в 3 т. / Под ред. В. С. Белецкого. — Донецк: Восточный издательский дом, 2001—2004.
- Ф. А. Деркач «Химия» Л., 1968.
| [+] Боевые отравляющие вещества | |||||||
|---|---|---|---|---|---|---|---|
| Общеядовитого действия | Циановодород (AC) • Хлорциан (CK) • Арсин (SA) • Фосфин (PH) • Угарный газ (CO) | ||||||
| Удушающего действия | Фосген (CG, Р-10 • Дифосген (DP) • Хлор (CL) | ||||||
| Кожно-нарывного действия | Иприт (HD) • Люизит (L, Р-43) • Метилдихлорарсин (MD) • Этилдихлорарсин (ED) • Фенилдихлорарсин (PD) • Сесквииприт (Q) • Азотистые иприты (Газ HN1, Газ HN2, Газ HN3) • Кислородный иприт (T) | ||||||
| Нервно-паралитического действия |
| ||||||
| Раздражающего действия (ирританты) |
| ||||||
| Психохимического действия (инкапаситанты) | Хинуклидил-3-бензилат (BZ, Р-78) • Фенциклидин (SN) • ЛСД (K) • Апоморфин • EA 3167 | ||||||
| Болевого действия (алгогены) | 1-метокси-1,3,5-циклогептатриен (CH) | ||||||
| Метаболические яды (цитотоксиканты) | 1,2-дихлорэтан • Оксид этилена • Полихлордибензодиоксины (ПХДД) • Полихлордибензофураны (ПХДФ) | ||||||
ХЛОР -а;
м.
[от греч. chlōros — бледно-зелёный] Химический элемент (Cl), удушливый газ зеленовато-жёлтого цвета с резким запахом (используется как отравляющее и обеззараживающее средство). Соединения хлора. Отравление хлором.
◁ Хло́рный (см.).
* * *
хлор
(лат. Chlorum), химический элемент VII группы периодической системы, относится к галогенам. Название от греческого chlōros — жёлто-зелёный. Свободный хлор состоит из двухатомных молекул (Cl2); газ жёлто-зелёного цвета с резким запахом; плотность 3,214 г/л; tпл —101°C; tкип —33,97°C; при обычной температуре легко сжижается под давлением 0,6 МПа. Химически очень активен (окислитель). Главные минералы — галит (каменная соль), сильвин, бишофит; морская вода содержит хлориды натрия, калия, магния и других элементов. Применяют в производстве хлорсодержащих органических соединений (60—75%), неорганических веществ (10—20%), для отбеливания целлюлозы и тканей (5—15%), для санитарных нужд и обеззараживания (хлорирования) воды. Токсичен.
* * *
ХЛОР
ХЛОР (лат. Сhlorum), Cl (читается «хлор»), химический элемент с атомным номером 17, атомная масса 35,453. В свободном виде — желто-зеленый тяжелый газ с резким удушливым запахом (отсюда название: греч. chloros — желто-зеленый).
Природный хлор представляет смесь двух нуклидов (см. НУКЛИД) с массовыми числами 35 (в смеси 75,77% по массе) и 37 (24,23%). Конфигурация внешнего электронного слоя 3s2p5. В соединениях проявляет главным образом степени окисления –1, +1, +3, +5 и +7 (валентности I, III, V и VII). Расположен в третьем периоде в группе VIIА периодической системы элементов Менделеева, относится к галогенам (см. ГАЛОГЕНЫ).
Радиус нейтрального атома хлора 0,099 нм, ионные радиусы равны, соответственно (в скобках указаны значения координационного числа): Cl— 0,167 нм (6), Cl5+ 0,026 нм (3) и Clr7+ 0,022 нм (3) и 0,041 нм (6). Энергии последовательной ионизации нейтрального атома хлора равны, соответственно, 12,97, 23,80, 35,9, 53,5, 67,8, 96,7 и 114,3 эВ. Сродство к электрону 3,614 эВ. По шкале Полинга электроотрицательность хлора 3,16.
История открытия
Важнейшее химическое соединение хлора — поваренная соль (химическая формула NaCl, химическое название хлорид натрия) — было известно человеку с древнейших времен. Имеются свидетельства того, что добыча поваренной соли осуществлялась еще 3—4 тысячи лет до нашей эры в Ливии. Возможно, что, используя поваренную соль для различных манипуляций, алхимики сталкивались и с газообразным хлором. Для растворения «царя металлов» — золота — они использовали «царскую водку» — смесь соляной и азотной кислот, при взаимодействии которых выделяется хлор.
Впервые газ хлор получил и подробно описал шведский химик К. Шееле (см. ШЕЕЛЕ Карл Вильгельм) в 1774 году. Он нагревал соляную кислоту с минералом пиролюзитом (см. ПИРОЛЮЗИТ) MnO2 и наблюдал выделение желто-зеленого газа с резким запахом. Так как в те времена господствовала теория флогистона (см. ФЛОГИСТОН), новый газ Шееле рассматривал как «дефлогистонированную соляную кислоту», т. е. как окись (оксид) соляной кислоты. А.Лавуазье (см. ЛАВУАЗЬЕ Антуан Лоран) рассматривал газ как оксид элемента «мурия» (соляную кислоту называли муриевой, от лат. muria — рассол). Такую же точку зрения сначала разделял английский ученый Г. Дэви (см. ДЭВИ Гемфри), который потратил много времени на то, чтобы разложить «окись мурия» на простые вещества. Это ему не удалось, и к 1811 году Дэви пришел к выводу, что данный газ — это простое вещество, и ему отвечает химический элемент. Дэви первым предложил в соответствие с желто-зеленой окраской газа назвать его chlorine (хлорин). Название «хлор» элементу дал в 1812 французский химик Ж. Л. Гей-Люссак (см. ГЕЙ-ЛЮССАК Жозеф Луи); оно принято во всех странах, кроме Великобритании и США, где сохранилось название, введенное Дэви. Высказывалось мнение о том, что данный элемент следует назвать «галоген» (т. е. рождающий соли), но оно со временем стало общим названием всех элементов группы VIIA.
Нахождение в природе
Содержание хлора в земной коре составляет 0,013% по массе, в заметной концентрации он в виде иона Cl– присутствует в морской воде (в среднем около 18,8 г/л). Химически хлор высоко активен и поэтому в свободном виде в природе не встречается. Он входит в состав таких минералов, образующих большие залежи, как поваренная, или каменная, соль (галит (см. ГАЛИТ)) NaCl, карналлит (см. КАРНАЛЛИТ) KCl·MgCl2·6H21O, сильвин (см. СИЛЬВИН) КСl, сильвинит (Na, K)Cl, каинит (см. КАИНИТ) КСl·MgSO4·3Н2О, бишофит (см. БИШОФИТ) MgCl2·6H2O и многих других. Хлор можно обнаружить в самых разных породах, в почве.
Получение
Для получения газообразного хлора используют электролиз крепкого водного раствора NaCl (иногда используют KCl). Электролиз проводят с использованием катионообменной мембраны, разделяющей катодное и анодное пространства. При этом за счет процесса
2NaCl + 2H2O = 2NaOH + H2 + Cl2
получают сразу три ценных химических продукта: на аноде — хлор, на катоде — водород (см. ВОДОРОД) , и в электролизере накапливается щелочь (1,13 тонны NaOH на каждую тонну полученного хлора). Производство хлора электролизом требует больших затрат электроэнергии: на получение1 т хлора расходуется от 2,3 до 3,7 МВт.
Для получения хлора в лаборатории используют реакцию концентрированной соляной кислоты с каким-либо сильным окислителем (перманганатом калия KMnO4, дихроматом калия K2Cr2O7, хлоратом калия KClO3, хлорной известью CaClOCl, оксидом марганца (IV) MnO2). Наиболее удобно использовать для этих целей перманганат калия: в этом случае реакция протекает без нагревания:
2KMnO4 + 16HCl = 2KСl + 2MnCl2+ 5Cl2+ 8H2O.
При необходимости хлор в сжиженном (под давлением) виде транспортируют в железнодорожных цистернах или в стальных баллонах. Баллоны с хлором имеют специальную маркировку, но даже при ее отсутствии хлорный баллон легко отличить от баллонов с другими неядовитыми газами. Дно хлорных баллонов имеет форму полушария, и баллон с жидким хлором невозможно без опоры поставить вертикально.
Физические и химические свойства
При обычных условиях хлор — желто-зеленый газ, плотность газа при 25°C 3,214 г/дм3 (примерно в 2,5 раза больше плотности воздуха). Температура плавления твердого хлора –100,98°C, температура кипения –33,97°C. Стандартный электродный потенциал Сl2/Сl— в водном растворе равен +1,3583 В.
В свободном состоянии существует в виде двухатомных молекул Сl2. Межъядерное расстояние в этой молекуле 0,1987 нм. Сродство к электрону молекулы Сl2 2,45 эВ, потенциал ионизации 11,48 эВ. Энергия диссоциации молекул Сl2 на атомы сравнительно невелика и составляет 239,23 кДж/моль.
Хлор немного растворим в воде. При температуре 0°C растворимость составляет 1,44 масс.%, при 20°C — 0,711°C масс.%, при 60°C — 0,323 масс. %. Раствор хлора в воде называют хлорной водой. В хлорной воде устанавливается равновесие:
Сl2 + H2O H+ = Сl— + HOСl.
Для того, чтобы сместить это равновесие влево, т. е. понизить растворимость хлора в воде, в воду следует добавить или хлорид натрия NaCl, или какую-либо нелетучую сильную кислоту (например, серную).
Хлор хорошо растворим во многих неполярных жидкостях. Жидкий хлор сам служит растворителем таких веществ, как ВСl3, SiCl4, TiCl4.
Из-за низкой энергии диссоциации молекул Сl2 на атомы и высокого сродства атома хлора к электрону химически хлор высоко активен. Он вступает в непосредственное взаимодействие с большинством металлов (в том числе, например, с золотом) и многими неметаллами. Так, без нагревания хлор реагирует с щелочными (см. ЩЕЛОЧНЫЕ МЕТАЛЛЫ) и щелочноземельными металлами (см. ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ), с сурьмой:
2Sb + 3Cl2 = 2SbCl3
При нагревании хлор реагирует с алюминием:
3Сl2 + 2Аl = 2А1Сl3
и железом:
2Fe + 3Cl2 = 2FeCl3.
С водородом H2 хлор реагирует или при поджигании (хлор спокойно горит в атмосфере водорода), или при облучении смеси хлора и водорода ультрафиолетовым светом. При этом возникает газ хлороводород НСl:
Н2 + Сl2 = 2НСl.
Раствор хлороводорода в воде называют соляной (см. СОЛЯНАЯ КИСЛОТА) (хлороводородной) кислотой. Максимальная массовая концентрация соляной кислоты около 38%. Соли соляной кислоты — хлориды (см. ХЛОРИДЫ) , например, хлорид аммония NH4Cl, хлорид кальция СаСl2, хлорид бария ВаСl2 и другие. Многие хлориды хорошо растворимы в воде. Практически нерастворим в воде и в кислых водных растворах хлорид серебра AgCl. Качественная реакция на присутствие хлорид-ионов в растворе — образование с ионами Ag+ белого осадка AgСl, практически нерастворимого в азотнокислой среде:
СаСl2 + 2AgNO3 = Ca(NO3)2 + 2AgCl.
При комнатной температуре хлор реагирует с серой (образуется так называемая однохлористая сера S2Cl2) и фтором (образуются соединения ClF и СlF3). При нагревании хлор взаимодействует с фосфором (образуются, в зависимости от условий проведения реакции, соединения РСl3 или РСl5), мышьяком, бором и другими неметаллами. Непосредственно хлор не реагирует с кислородом, азотом, углеродом (многочисленные соединения хлора с этими элементами получают косвенными путями) и инертными газами (в последнее время ученые нашли способы активирования подобных реакций и их осуществления «напрямую»). С другими галогенами хлор образует межгалогенные соединения, например, очень сильные окислители — фториды ClF, ClF3, ClF5 . Окислительная способность хлора выше, чем брома, поэтому хлор вытесняет бромид-ион из растворов бромидов, например:
Cl2 + 2NaBr = Br2 + 2NaCl
Хлор вступает в реакции замещения со многими органическими соединениями, например, с метаном СН4 и бензолом С6Н6:
СН4+ Сl2 = СН3Сl + НСl или С6Н6 + Сl2 = С6Н5Сl + НСl.
Молекула хлора способна присоединятся по кратным связям (двойным и тройным) к органическим соединениям, например, к этилену С2Н4:
С2Н4 + Сl2 = СН2СlСН2Сl.
Хлор вступает во взаимодействие с водными растворами щелочей. Если реакция протекает при комнатной температуре, то образуются хлорид (например, хлорид калия КCl) и гипохлорит (см. ГИПОХЛОРИТЫ) (например, гипохлорит калия КClО):
Cl2 + 2КОН = КClО + КСl +Н2О.
При взаимодействии хлора с горячим (температура около 70—80°C) раствором щелочи образуется соответствующий хлорид и хлорат (см. ХЛОРАТЫ) , например:
3Сl2+ 6КОН= 5КСl + КСlО3+ 3Н2О.
При взаимодействии хлора с влажной кашицей из гидроксида кальция Са(ОН)2 образуется хлорная известь (см. ХЛОРНАЯ ИЗВЕСТЬ) («хлорка») СаСlОСl.
Степени окисления хлора +1 отвечает слабая малоустойчивая хлорноватистая кислота (см. ХЛОРНОВАТИСТАЯ КИСЛОТА) НСlО. Ее соли — гипохлориты, например, NaClO — гипохлорит натрия. Гипохлориты — сильнейшие окислители, широко используются как отбеливающие и дезинфицирующие агенты. При взаимодействии гипохлоритов, в частности, хлорной извести, с углекислым газом СО2 образуется среди других продуктов летучая хлорноватистая кислота (см. ХЛОРНОВАТИСТАЯ КИСЛОТА) , которая может разлагаться с выделением оксида хлора (I) Сl2О:
2НСlО = Сl2О + Н2О.
Именно запах этого газа Сl2О — характерный запах «хлорки».
Степени окисления хлора +3 отвечает малоустойчивая кислота средней силы НСlО2. Эту кислоту называют хлористой, ее соли — хлориты (см. ХЛОРИТЫ (соли)) , например, NaClO2 — хлорит натрия.
Степени окисления хлора +4 соответствует только одно соединение — диоксид хлора СlО2.
Степени окисления хлора +5 отвечает сильная, устойчивая только в водных растворах при концентрации ниже 40%, хлорноватая кислота (см. ХЛОРНОВАТИСТАЯ КИСЛОТА) НСlО3. Ее соли — хлораты, например, хлорат калия КСlО3.
Степени окисления хлора +6 соответствует только одно соединение — триоксид хлора СlО3 (существует в виде димера Сl2О6).
Степени окисления хлора +7 отвечает очень сильная и довольно устойчивая хлорная кислота (см. ХЛОРНАЯ КИСЛОТА) НСlО4. Ее соли — перхлораты (см. ПЕРХЛОРАТЫ) , например, перхлорат аммония NH4ClO4 или перхлорат калия КСlО4. Следует отметить, что перхлораты тяжелых щелочных металлов — калия, и особенно рубидия и цезия мало растворимы в воде. Оксид, соответствующий степени окисления хлора +7 — Сl2О7.
Среди соединений, содержащих хлор в положительных степенях окисления, наиболее сильными окислительными свойствами обладают гипохлориты. Для перхлоратов окислительные свойства нехарактерны.
Применение
Хлор — один из важнейших продуктов химической промышленности. Его мировое производство составляет десятки миллионов тонн в год. Хлор используют для получения дезинфицирующих и отбеливающих средств (гипохлорита натрия, хлорной извести и других), соляной кислоты, хлоридов многих металлов и неметаллов, многих пластмасс (поливинилхлорида (см. ПОЛИВИНИЛХЛОРИД) и других), хлорсодержащих растворителей (дихлорэтана СН2СlСН2Сl, четыреххлористого углерода ССl4 и др.), для вскрытия руд, разделения и очистки металлов и т.д. Хлор применяют для обеззараживания воды (хлорирования (см. ХЛОРИРОВАНИЕ) ) и для многих других целей.
Биологическая роль
Хлор относится к важнейшим биогенным элементам (см. БИОГЕННЫЕ ЭЛЕМЕНТЫ) и входит в состав всех живых организмов. Некоторые растения, так называемые галофиты, не только способны расти на сильно засоленных почвах, но и накапливают в больших количествах хлориды. Известны микроорганизмы (галобактерии и др.) и животные, обитающие в условиях высокой солености среды. Хлор — один из основных элементов водно-солевого обмена животных и человека, определяющих физико-химические процессы в тканях организма. Он участвует в поддержании кислотно-щелочного равновесия в тканях, осморегуляции (см. ОСМОРЕГУЛЯЦИЯ) (хлор — основное осмотически активное вещество крови, лимфы и др. жидкостей тела), находясь, в основном, вне клеток. У растений хлор принимает участие в окислительных реакциях и фотосинтезе.
Мышечная ткань человека содержит 0,20—0,52% хлора, костная — 0,09%; в крови — 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3—6 г хлора, что с избытком покрывает потребность в этом элементе.
Особенности работы с хлором
Хлор — ядовитый удушливый газ, при попадании в легкие вызывает ожог легочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 0,006 мг/л. Хлор был одним из первых химических отравляющих веществ (см. ОТРАВЛЯЮЩИЕ ВЕЩЕСТВА) , использованных Германией в Первую мировую войну. При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3. ПДК хлора в воздухе рабочих помещений 1 мг/м3, в воздухе населенных пунктов 0,03 мг/м3.
Энциклопедический словарь.
2009.
| Хлор | |
|---|---|
 Жидкий хлор в запаянном сосуде | |
| Название, символ, номер | Хлор / Chlorum (Cl), 17 |
| Атомная масса (молярная масса) | [35,446; 35,457]а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s2 3p5 |
| Радиус атома | 99 пм |
| Ковалентный радиус | 102±4 пм |
| Радиус иона | (+7e)27 (-1e)181 пм |
| Электроотрицательность | 3,16 (шкала Полинга) |
| Электродный потенциал | 0 |
| Степени окисления | 7, 6, 5, 4, 3, 1, 0, −1 |
| Энергия ионизации (первый электрон) | 1254,9(13,01) кДж/моль (эВ) |
| Плотность (при н. у.) | 3,21 г/л; (жид. при −35 °C) 1,557 г/см3; (тв. при −105 °C) 1,9 г/см³ |
| Температура плавления | 172,2К; −100,95 °C |
| Температура кипения | 238,6К; −34,55 °C |
| Критическая точка | 416,9 К, 7,991 МПа |
| Уд. теплота плавления | 6,41 кДж/моль |
| Уд. теплота испарения | 20,41 кДж/моль |
| Молярная теплоёмкость | 21,838 Дж/(K·моль) |
| Молярный объём | 18,7 см³/моль |
| Структура решётки | орторомбическая |
| Параметры решётки | a=6,29 b=4,50 c=8,21 Å |
| Теплопроводность | (300 K) 0,009 Вт/(м·К) |
| Номер CAS | 7782-50-5 |
Хлор (от греч. χλωρός — «жёлто-зелёный») — химический элемент с атомным номером 17. Принадлежит к 17-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA), находится в третьем периоде таблицы. Атомная масса элемента 35,446…35,457 а. е. м.. Обозначается символом Cl (от лат. Chlorum). Химически активный неметалл. Входит в группу галогенов.
Простое вещество хлор при нормальных условиях — ядовитый газ желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом. Молекула хлора двухатомная (формула Cl2).

История открытия хлора
См. также: Мурий
Соединение с водородом — газообразный хлороводород — был впервые получен Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
- 4HCl + MnO2 → MnCl2 + Cl2↑ + 2H2O
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теорией флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Г. Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
В 1811 г. Дэви предложил для нового элемента название «хлорин» (chlorine). Спустя год Ж. Гей-Люссак «сократил» название до хлора (chlore). В том же 1811 г. немецкий физик Иоганн Швейгер предложил для хлора название «галоген» (дословно солерод), однако впоследствии этот термин закрепился за всей 17-й (VIIA) группой элементов, в которую входит и хлор.
В 1826 году атомная масса хлора была с высокой точностью определена шведским химиком Йёнсом Якобом Берцелиусом (отличается от современных данных не более, чем на 0,1 %).
Распространение в природе
В природе встречаются два изотопа хлора 35Cl и 37Cl. В земной коре хлор самый распространённый галоген. Хлор очень активен — он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl·NaCl, бишофита MgCl2·6H2O., карналлита KCl·MgCl2·6H2O., каинита KCl·MgSO4·3H2O. Самые большие запасы хлора содержатся в составе солей вод морей и океанов (содержание в морской воде 19 г/л). На долю хлора приходится 0,025 % от общего числа атомов земной коры; кларковое число хлора — 0,017 %. Человеческий организм содержит 0,25 % ионов хлора по массе. В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
Изотопный состав
Основная статья: Изотопы хлора
В природе встречаются 2 стабильных изотопа хлора: с массовым числом 35 и 37. Доли их содержания соответственно равны 75,78 % и 24,22 %. Свойства стабильных и некоторых радиоактивных изотопов хлора перечислены в таблице:
| Изотоп | Относительная масса, а. е. м. | Период полураспада | Тип распада | Ядерный спин |
|---|---|---|---|---|
| 35Cl | 34,968852721 | Стабилен | — | 3/2 |
| 36Cl | 35,9683069 | 301 тыс. лет | β-распад в 36Ar | 0 |
| 37Cl | 36,96590262 | Стабилен | — | 3/2 |
| 38Cl | 37,9680106 | 37,2 минуты | β-распад в 38Ar | 2 |
| 39Cl | 38,968009 | 55,6 минуты | β-распад в 39Ar | 3/2 |
| 40Cl | 39,97042 | 1,38 минуты | β-распад в 40Ar | 2 |
| 41Cl | 40,9707 | 34 c | β-распад в 41Ar | |
| 42Cl | 41,9732 | 46,8 c | β-распад в 42Ar | |
| 43Cl | 42,9742 | 3,3 c | β-распад в 43Ar |
Физические и химические свойства

При нормальных условиях хлор — жёлто-зелёный газ с удушающим запахом. Некоторые его физические свойства представлены в таблице.
| Свойство | Значение |
|---|---|
| Цвет (газ) | Жёлто-зелёный |
| Температура кипения | −34 °C |
| Температура плавления | −100 °C |
| Температура разложения (диссоциации на атомы) | ~1400 °C |
| Плотность (газ, н.у.) | 3,214 г/л |
| Сродство к электрону атома | 3,65 эВ |
| Первая энергия ионизации | 12,97 эВ |
| Теплоёмкость (298 К, газ) | 34,94 Дж/(моль·K) |
| Критическая температура | 144 °C |
| Критическое давление | 76 атм |
| Стандартная энтальпия образования (298 К, газ) | 0 кДж/моль |
| Стандартная энтропия образования (298 К, газ) | 222,9 Дж/(моль·K) |
| Энтальпия плавления | 6,406 кДж/моль |
| Энтальпия кипения | 20,41 кДж/моль |
| Энергия гомолитического разрыва связи Х—Х | 243 кДж/моль |
| Энергия гетеролитического разрыва связи Х—Х | 1150 кДж/моль |
| Энергия ионизации | 1255 кДж/моль |
| Энергия сродства к электрону | 349 кДж/моль |
| Атомный радиус | 0,073 нм |
| Электроотрицательность по Полингу | 3,20 |
| Электроотрицательность по Оллреду — Рохову | 2,83 |
| Устойчивые степени окисления | −1, 0, +1, +3, (+4), +5, (+6), +7 |
Газообразный хлор относительно легко сжижается. Начиная с давления в 0,8 МПа (8 атмосфер), хлор будет жидким уже при комнатной температуре. При охлаждении до температуры в −34 °C хлор тоже становится жидким при нормальном атмосферном давлении. Жидкий хлор — жёлто-зелёная жидкость, обладающая очень высоким коррозионным действием (за счёт высокой концентрации молекул). Повышая давление, можно добиться существования жидкого хлора вплоть до температуры в +144 °C (критической температуры) при критическом давлении в 7,6 МПа.
При температуре ниже −101 °C жидкий хлор кристаллизуется в орторомбическую решётку с пространственной группой Cmca и параметрами a = 6,29 Å, b = 4,50 Å, c = 8,21 Å. Ниже 100 К орторомбическая модификация кристаллического хлора переходит в тетрагональную, имеющую пространственную группу P42/ncm и параметры решётки a = 8,56 Å и c = 6,12 Å.
Растворимость
| Растворитель | Растворимость г/100 г |
|---|---|
| Бензол | Растворим |
| Вода (0 °C) | 1,48 |
| Вода (20 °C) | 0,96 |
| Вода (25 °C) | 0,65 |
| Вода (40 °C) | 0,46 |
| Вода (60 °C) | 0,38 |
| Вода (80 °C) | 0,22 |
| Тетрахлорметан (0 °C) | 31,4 |
| Тетрахлорметан (19 °C) | 17,61 |
| Тетрахлорметан (40 °C) | 11 |
| Хлороформ | Хорошо растворим |
| TiCl4, SiCl4, SnCl4 | Растворим |
Степень диссоциации молекулы хлора Cl2 → 2Cl при 1000 К равна 2,07⋅10−4%, а при 2500 К — 0,909 %.
Порог восприятия запаха в воздухе равен 2—3 мг/м³.
По электропроводности жидкий хлор занимает место среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 1022 раз хуже серебра. Скорость звука в газообразном хлоре примерно в полтора раза меньше, чем в воздухе.
Химические свойства
Строение электронной оболочки
На валентном уровне атома хлора содержится 1 неспаренный электрон: 1s2 2s2 2p6 3s2 3p5, поэтому валентность, равная 1 для атома хлора, очень стабильна. За счёт присутствия в атоме хлора незанятой орбитали d-подуровня атом хлора может проявлять и другие степени окисления. Схема образования возбуждённых состояний атома:
| Валентность | Возможные степени окисления | Электронное состояние валентного уровня | Пример соединений |
|---|---|---|---|
| I | +1, −1, 0 | 3s2 3p5 | NaCl, NaClO, Cl2 |
| III | +3 | 3s2 3p4 3d1 | NaClO2 |
| V | +5 | 3s2 3p3 3d2 | KClO3 |
| VII | +7 | 3s1 3p3 3d3 | KClO4 |
Также известны соединения хлора, в которых атом хлора формально проявляет валентности IV и VI, например, ClO2 и Cl2O6. Однако оксид хлора(IV) является радикалом, то есть у него есть один неспаренный электрон, а оксид хлора(VI) содержит два атома хлора, имеющих степени окисления +5 и +7.
Взаимодействие с металлами
Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании):
- 2Na + Cl2 → 2NaCl
- 2Sb + 3Cl2 → 2SbCl3
- 2Fe + 3Cl2 → 2FeCl3
Взаимодействие с неметаллами
C неметаллами (кроме углерода, азота, фтора, кислорода и инертных газов) образует соответствующие хлориды.
- 5Cl2 + 2P → 2PCl5 ,
- 2S + Cl2 → S2Cl2
или
- S + Cl2 → SCl2
На свету или при нагревании активно реагирует (иногда со взрывом) с водородом по радикально-цепному механизму. Смеси хлора с водородом, содержащие от 5,8 до 88,3 % водорода, взрываются при облучении с образованием хлороводорода. Смесь хлора с водородом в небольших концентрациях горит бесцветным или жёлто-зелёным пламенем. Максимальная температура водородно-хлорного пламени 2200 °C.
- H2 + Cl2 → 2HCl
С кислородом хлор образует оксиды (см. статью Оксиды хлора), в которых он проявляет степень окисления от +1 до +7: Cl2O, ClO2, Cl2O5, Cl2O7. Они имеют резкий запах, термически и фотохимически нестабильны, склонны к взрывному распаду. Напрямую хлор с кислородом не реагирует. При реакции с фтором образуется не хлорид, а фториды:
- Cl2 + F2 → 2ClF
- Cl2 + 3F2 → 2ClF3
- Cl2 + 5F2 → 2ClF5
Известны фторид хлора(I), фторид хлора(III) и фторид хлора(V) (ClF, ClF3 и ClF5), Могут быть синтезированы из элементов, степень окисления хлора меняется в зависимости от условий синтеза. Все они представляют собой при комнатной температуре бесцветные ядовитые тяжёлые газы с сильным раздражающим запахом. Сильные окислители, реагируют с водой и стеклом. Используются как фторирующие агенты.
Другие свойства
Хлор вытесняет бром и йод из их соединений с водородом и металлами:
- Cl2 + 2HBr → Br2 + 2HCl
- Cl2 + 2NaI → I2 + 2NaCl
При реакции с монооксидом углерода образуется фосген:
- Cl2 + CO → COCl2
При растворении в воде или щелочах, хлор диспропорционирует, образуя хлорноватистую (а при нагревании хлорноватую) и соляную кислоты, либо их соли:
- Cl2+ H2O ⇄ HCl + HClO
- Cl2 + 2NaOH → NaCl + NaClO + H2O
- 3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании)
Хлорированием сухого гидроксида кальция получают хлорную известь:
- Cl2 + Ca(OH)2 → CaCl(OCl) + H2O
Действием хлора на аммиак можно получить трихлорид азота:
- 4NH3 + 3Cl2 → NCl3 + 3NH4Cl
Окислительные свойства хлора
Хлор — очень сильный окислитель:
- Cl2 + H2S → 2HCl + S
Раствор хлора в воде используется для отбеливания тканей и бумаги.
Реакции с органическими веществами
С насыщенными соединениями:
- CH3-CH3 + Cl2 → C2H5Cl + HCl
- CH4 + Cl2 → CH3Cl + HCl (получение хлороформа, реакция идет многоступенчато с образованием тетрахлорметана CCl4)
Присоединяется к ненасыщенным соединениям по кратным связям:
- CH2=CH2 + Cl2 → Cl-CH2-CH2-Cl
Ароматические соединения замещают атом водорода на хлор в присутствии катализаторов (например, AlCl3 или FeCl3):
- C6H6 + Cl2 → C6H5Cl + HCl
Способы получения
Химические методы
Химические методы получения хлора малоэффективны и затратны. На сегодняшний день имеют в основном историческое значение.
Метод Шееле
Первоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции пиролюзита с соляной кислотой:
- MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
Метод Дикона
В 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Процесс Дикона в настоящее время используется при рекуперации хлора из хлороводорода, являющегося побочным продуктом при промышленном хлорировании органических соединений.
- 4HCl + O2 → 2H2O + 2Cl2↑
Современные лабораторные методы
Ввиду доступности хлора в лабораторной практике обычно используется сжиженный хлор в баллонах. Хлор можно получить действием кислоты на гипохлорит натрия:
- 4NaOCl + 4CH3COOH = 4NaCH3COO + 2Cl2↑ + O2↑ + 2H2O
При этом также выделяется кислород. Если использовать соляную кислоту, то реакция выглядит по-другому:
- NaOCl + 2HCl = NaCl + Cl2↑ + H2O
Для получения хлора в небольших количествах обычно используются процессы, основанные на окислении хлороводорода сильными окислителями (например, оксидом марганца (IV), перманганатом калия, хлоритом кальция, хроматом калия, дихроматом калия, диоксидом свинца, бертолетовой солью и т. п.), обычно используется диоксид марганца или перманганат калия:
- 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
При невозможности использования баллонов и химических методов получения хлора могут быть использованы электрохимические — при помощи небольших электролизеров с обычным или вентильным электродом для получения хлора.
Электрохимические методы
Сегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли, основные процессы которого можно представить суммарной формулой:
- 2NaCl + 2H2O + 2e− → 2NaOH + Cl2↑ + H2↑
Применяется три варианта электрохимического метода получения хлора. Два из них — электролиз с твердым катодом: диафрагменный и мембранный методы, третий — электролиз с жидким ртутным катодом (ртутный метод производства). Качество хлора, получаемого электрохимическими методами, отличается мало:
| Ртутный метод | Диафрагменный метод | Мембранный метод | |
|---|---|---|---|
| Выход хлора % | 99 | 96 | 98,5 |
| Электроэнергия (кВт·ч) | 3 150 | 3 260 | 2 520 |
| Чистота хлора | 99,2 | 98 | 99,3 |
| Массовая доля O2 в хлоре, % | 0,1 | 1—2 | 0,3 |
Диафрагменный метод

Схема старинного диафрагменного электролизера для получения хлора и щелоков: А — анод, В — изоляторы, С — катод, D — пространство, заполненное газами (над анодом — хлор, над катодом — водород), М — диафрагма
Наиболее простым, из электрохимических методов, в плане организации процесса и конструкционных материалов для электролизера, является диафрагменный метод получения хлора.
Раствор соли в диафрагменном электролизере непрерывно подается в анодное пространство и протекает через, как правило, насаженную на стальную катодную сетку асбестовую диафрагму, в которую иногда добавляют небольшое количество полимерных волокон.
Насасывание диафрагмы производится путём прокачивания через электролизер пульпы из асбестовых волокон, которые, застревая в сетке катода, образуют слой асбеста, играющий роль диафрагмы.
Во многих конструкциях электролизеров катод полностью погружен под слой анолита (электролита из анодного пространства), а выделяющийся на катодной сетке водород отводится из-под катода при помощи газоотводных труб, не проникая через диафрагму в анодное пространство благодаря противотоку.
Противоток — очень важная особенность устройства диафрагменного электролизера. Именно благодаря противоточному потоку, направленному из анодного пространства в катодное через пористую диафрагму, становится возможным раздельное получение щелоков и хлора. Противоточный поток рассчитывается так, чтобы противодействовать диффузии и миграции OH— ионов в анодное пространство. Если величина противотока недостаточна, тогда в анодном пространстве в больших количествах начинает образовываться гипохлорит-ион (ClO—), который затем может окисляться на аноде до хлорат-иона ClO3—. Образование хлорат-иона серьёзно снижает выход по току хлора и является основным побочным процессом в этом методе. Так же вредит и выделение кислорода, которое, к тому же, ведёт к разрушению анодов и, если они из углеродных материалов, попадания в хлор примесей фосгена.
- Анод:
- 2Cl− − 2e− → Cl2↑ — основной процесс
- 2H2O − 4e− → O2↑ + 4H+
- 12ClO− + 6H2O − 12e− → 4ClO3− + 8Cl− + 3O2↑ + 6H+
- Катод:
- 2H2O + 2e− → H2↑ + 2OH− — основной процесс
- ClO− + H2O + 2e− → Cl− + 2OH−
- ClO3− + 3H2O + 6e− → Cl− + 6OH−
В качестве анода в диафрагменных электролизерах может использоваться графитовый или угольный электроды. На сегодня их в основном заменили титановые аноды с окисно-рутениево-титановым покрытием (аноды ОРТА) или другие малорасходуемые.
Поваренная соль, сульфат натрия и другие примеси при повышении их концентрации в растворе выше их предела растворимости выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или продолжают стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией.
Обратную, то есть кристаллизовавшуюся в осадок поваренную соль возвращают назад в процесс, приготавливая из неё так называемый обратный рассол. От неё, во избежание накапливания примесей в растворах, перед приготовлением обратного рассола отделяют примеси.
Убыль анолита восполняют добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов галита, бишофита и других минералов, содержащих хлорид натрия, а также растворением их в специальных ёмкостях на месте производства. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния.
Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Благодаря относительной простоте и дешевизне диафрагменный метод получения хлора до сих пор широко используется в промышленности.
- Схема диафрагменного электролизера.
Мембранный метод
Мембранный метод производства хлора наиболее энергоэффективен, однако сложен в организации и эксплуатации.
С точки зрения электрохимических процессов мембранный метод подобен диафрагменному, но анодное и катодное пространства полностью разделены непроницаемой для анионов катионообменной мембраной. Поэтому в мембранном электролизере, в отличие от диафрагменного, не один поток, а два.
В анодное пространство поступает, как и в диафрагменном методе, поток раствора соли. А в катодное — деионизированная вода. Из анодного пространства вытекает поток обеднённого анолита, содержащего также примеси гипохлорит- и хлорат-ионов и выходит хлор, а из катодного — щелока и водород, практически не содержащие примесей и близкие к товарной концентрации, что уменьшает затраты энергии на их упаривание и очистку.
Однако питающий раствор соли (как свежий, так и оборотный) и вода предварительно максимально очищаются от любых примесей. Такая тщательная очистка определяется высокой стоимостью полимерных катионообменных мембран и их уязвимостью к примесям в питающем растворе.
Кроме того, ограниченная геометрическая форма, а также низкая механическая прочность и термическая стойкость ионообменных мембран, во многом определяют сравнительно сложные конструкции установок мембранного электролиза. По той же причине мембранные установки требуют наиболее сложных систем автоматического контроля и управления.
- Схема мембранного электролизера.
Ртутный метод с жидким катодом
В ряду электрохимических методов получения хлора ртутный метод позволяет получать самый чистый хлор.
- Схема ртутного электролизера.
Установка для ртутного электролиза состоит из электролизёра, разлагателя амальгамы и ртутного насоса, объединённых между собой ртутепроводящими коммуникациями.
Катодом электролизёра служит поток ртути, прокачиваемой насосом. Аноды — графитовые, угольные или малоизнашивающиеся (ОРТА, ТДМА или другие). Вместе с ртутью через электролизёр непрерывно течёт поток питающего раствора поваренной соли.
На аноде происходит окисление ионов хлора из электролита, и выделяется хлор:
- 2Cl− − 2e− → Cl2↑ — основной процесс
- 2H2O − 2e− → O2↑ + 4H+
- 12ClO− + 6H2O − 12e− → 4ClO3− + 8Cl− + 3O2↑ + 12H+
Хлор и анолит отводится из электролизёра. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесённые с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают растворённый в нём хлор.
Растущие требования к экологической безопасности производств и дороговизна металлической ртути ведут к постепенному вытеснению ртутного метода методами получения хлора с твердым катодом.
Хранение хлора
Производимый хлор хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — защитный цвет c зелёной полосой. Следует отметить, что при длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый трихлорид азота, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота.
Стандарты качества хлора
Согласно ГОСТ 6718-93 «Хлор жидкий. Технические условия» производятся следующие сорта хлора:
| Наименование показателя ГОСТ 6718-93 | Высший сорт | Первый сорт |
|---|---|---|
| Объемная доля хлора, не менее, % | 99,8 | 99,6 |
| Массовая доля воды, не более, % | 0,01 | 0,04 |
| Массовая доля треххлористого азота, не более, % | 0,002 | 0,004 |
| Массовая доля нелетучего остатка, не более, % | 0,015 | 0,10 |
Применение
Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:

Оконный профиль, изготовленный из хлорсодержащих полимеров

Основным компонентом отбеливателей является Лабарракова вода (гипохлорит натрия)
- В производстве поливинилхлорида, пластикатов, синтетического каучука, из которых изготавливают: изоляцию для проводов, оконный профиль, упаковочные материалы, одежду и обувь, линолеум и грампластинки, лаки, аппаратуру и пенопласты, игрушки, детали приборов, строительные материалы. Поливинилхлорид производят полимеризацией винилхлорида, который сегодня чаще всего получают из этилена сбалансированным по хлору методом через промежуточный 1,2-дихлорэтан.
- Отбеливающие свойства хлора известны с давних времен. Хлор разрушает многие органические красители, делая их бесцветными, однако это происходит лишь в присутствии жидкой или газообразной воды, поскольку «отбеливает» не сам хлор, а атомарный кислород, который образуется при распаде хлорноватистой кислоты:
-
- Cl2 + H2O → HCl + HOCl
- HOCl → HCl + O
Этот старинный способ отбеливания тканей, бумаги, картона.
- Производство хлорорганических инсектицидов — веществ, убивающих вредных для посевов насекомых, но безопасных для растений. На получение средств защиты растений расходуется значительная часть производимого хлора. Один из самых важных инсектицидов — гексахлорциклогексан (часто называемый гексахлораном). Это вещество впервые синтезировано ещё в 1825 г. Фарадеем, но практическое применение нашло только через 100 с лишним лет — в 30-х годах XX столетия.
- Использовался как боевое отравляющее вещество, а также для производства других боевых отравляющих веществ: иприт, фосген.
- Для обеззараживания воды — «хлорирования». Наиболее распространённый способ обеззараживания питьевой воды; основан на способности свободного хлора и его соединений угнетать ферментные системы микроорганизмов, катализирующие окислительно-восстановительные процессы. Для обеззараживания питьевой воды применяют: хлор, двуокись хлора, хлорамин и хлорную известь. СанПиН 2.1.4.1074-01 [1] устанавливает следующие пределы (коридор) допустимого содержания свободного остаточного хлора в питьевой воде централизованного водоснабжения 0,3 — 0,5 мг/л. Ряд учёных и даже политиков в России критикуют саму концепцию хлорирования водопроводной воды. Альтернативой является озонирование. Материалы, из которых изготовлены водопроводные трубы, по-разному взаимодействуют с хлорированной водопроводной водой. Свободный хлор в водопроводной воде существенно сокращает срок службы трубопроводов на основе полиолефинов: полиэтиленовых труб различного вида, в том числе сшитого полиэтилена, больше известного как ПЕКС (PEX, PE-X). В США для контроля допуска трубопроводов из полимерных материалов к использованию в водопроводах с хлорированной водой вынуждены были принять 3 стандарта: ASTM F2023 применительно к трубам из сшитого полиэтилена (PEX) и горячей хлорированной воде, ASTM F2263 применительно к полиэтиленовым трубам всем и хлорированной воде и ASTM F2330 применительно к многослойным (металлополимерным) трубам и горячей хлорированной воде. В части долговечности при взаимодействии с хлорированной водой положительные результаты демонстрируют медные водопроводные трубы.
- В пищевой промышленности зарегистрирован в качестве пищевой добавки E925.
- В химическом производстве соляной кислоты, хлорной извести, бертолетовой соли, хлоридов металлов, ядов, лекарств, удобрений.
- В металлургии для производства чистых металлов: титана, олова, тантала, ниобия.
- Как индикатор солнечных нейтрино в хлор-аргонных детекторах.
Многие развитые страны стремятся ограничить использование хлора в быту, в том числе потому, что при сжигании хлорсодержащего мусора образуется значительное количество диоксинов.
Биологическая роль
Хлор относится к важнейшим биогенным элементам и входит в состав всех живых организмов в виде соединений.
У животных и человека ионы хлора участвуют в поддержании осмотического равновесия, хлорид-ион имеет оптимальный радиус для проникновения через мембрану клеток. Именно этим объясняется его совместное участие с ионами натрия и калия в создании постоянного осмотического давления и регуляции водно-солевого обмена. Под воздействием ГАМК (нейромедиатор) ионы хлора оказывают тормозящий эффект на нейроны путём снижения потенциала действия. В желудке ионы хлора создают благоприятную среду для действия протеолитических ферментов желудочного сока. Хлорные каналы представлены во многих типах клеток, митохондриальных мембранах и скелетных мышцах. Эти каналы выполняют важные функции в регуляции объёма жидкости, трансэпителиальном транспорте ионов и стабилизации мембранных потенциалов, участвуют в поддержании рН клеток. Хлор накапливается в висцеральной ткани, коже и скелетных мышцах. Всасывается хлор, в основном, в толстом кишечнике. Всасывание и экскреция хлора тесно связаны с ионами натрия и бикарбонатами, в меньшей степени с минералокортикоидами и активностью Na+/K+ — АТФ-азы. В клетках аккумулируется 10-15 % всего хлора, из этого количества от 1/3 до 1/2 — в эритроцитах. Около 85 % хлора находятся во внеклеточном пространстве. Хлор выводится из организма в основном с мочой (90—95 %), калом (4-8 %) и через кожу (до 2 %). Экскреция хлора связана с ионами натрия и калия, и реципрокно (взаимно) с гидрокарбонат-ионами HCO3− (кислотно-щелочной баланс).
Человек потребляет 5—10 г NaCl в сутки. Минимальная потребность человека в хлоре составляет около 800 мг в сутки. Младенец получает необходимое количество хлора через молоко матери, в котором содержится 11 ммоль/л хлора. NaCl необходим для выработки в желудке соляной кислоты, которая способствует пищеварению и уничтожению болезнетворных бактерий. В настоящее время участие хлора в возникновении отдельных заболеваний у человека изучено недостаточно хорошо, главным образом из-за малого количества исследований. Достаточно сказать, что не разработаны даже рекомендации по норме суточного потребления хлора. Мышечная ткань человека содержит 0,20—0,52 % хлора, костная — 0,09 %; в крови — 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3—6 г хлора, что с избытком покрывает потребность в этом элементе.
Ионы хлора жизненно необходимы растениям. Хлор участвует в энергетическом обмене у растений, активируя окислительное фосфорилирование. Он необходим для образования кислорода в процессе фотосинтеза изолированными хлоропластами, стимулирует вспомогательные процессы фотосинтеза, прежде всего те из них, которые связаны с аккумулированием энергии. Хлор положительно влияет на поглощение корнями кислорода, соединений калия, кальция, магния. Чрезмерная концентрация ионов хлора в растениях может иметь и отрицательную сторону, например, снижать содержание хлорофилла, уменьшать активность фотосинтеза, задерживать рост и развитие растений.
Но существуют растения, которые в процессе эволюции либо приспособились к засолению почв, либо в борьбе за пространство заняли пустующие солончаки, на которых нет конкуренции. Растения, произрастающие на засоленных почвах, называются галофитами. Они накапливают хлориды в течение вегетационного сезона, а потом избавляются от излишков посредством листопада или выделяют хлориды на поверхность листьев и веток и получают двойную выгоду, притеняя поверхности от солнечного света.
Среди микроорганизмов также известны галофилы — галобактерии, — которые обитают в сильносоленых водах или почвах.
Токсичность
Хлор — токсичный удушающий газ, сильный ирритант, при попадании в лёгкие вызывает ожог лёгочной ткани (в результате образования в них хлорноватистой и соляной кислоты), удушье.
Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе уже от 1 до 6 мг/м³ (что близко к порогу восприятия запаха хлора), при 12 мг/м³ переносится с трудом, концентрации больше 100 мг/м³ опасны для жизни (смерть от остановки дыхания наступает через 5—25 минут, при высоких концентрациях — мгновенно).
Предельно допустимая концентрация хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³.
При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
Хлор был одним из первых химических отравляющих веществ, использованных Германией в Первую мировую войну, впервые применен в 1915 году во время битвы при Ипре.
| Периодическая система химических элементов Д. И. Менделеева | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ХЛОР (лат. Chlorum), Cl, химич. элемент VII группы короткой формы (17-й группы длинной формы) периодич. системы; относится к галогенам; ат. н. 17, ат. м. 35,453. В природе два стабильных нуклида 35Cl (75,78%) и 37Cl (24,22%); искусственно получены радионуклиды с массовыми числами 22–51, наиболее долгоживущий 36Cl (T1/2 301 тыс. лет; β-распад и электронный захват).
Историческая справка
Газообразный Х. впервые выделен К. Шееле в 1774 окислением соляной кислоты пиролюзитом MnO2. Элементарную природу Х. установил в 1810 Г. Дэви и предложил в 1811 соответствующее окраске назв. «Х.» (от греч. χλωρός – жёлто-зелёный).
Распространённость в природе
Содержание Х. в земной коре 0,017% по массе, в вулканич. газах – до 1,3%. Вследствие высокой химич. активности в свободном виде не встречается. Входит в состав мн. минералов. Собств. минералы Х. – в осн. природные хлориды (см. в ст. Галогениды природные): каменная соль (галит) NaCl, сильвин KCl, карналлит KCl·MgCl2·6H2O, каинит KCl·MgSO4·3H2O, бишофит MgCl2·6H2O. Гл. роль в распространении Х. в земной коре играет водная миграция. Х. в виде иона Cl– содержится в морской воде (18,83 г/дм3), подземных рассолах, соляных озёрах и др. Ионы Cl– важны для всех живых организмов (участвуют в регулировании водного обмена и др.); в составе тканей человека 0,25% по массе Х. (в плазме крови 0,32–0,37%), содержание Х. в тканях растений зависит от вида растения (напр., в табаке – 2,3%, в моркови – 1,5%, в зерновых – 0,05%).
Свойства
Конфигурация внешней электронной оболочки атома Х. 3s23р5; в соединениях проявляет степени окисления –1 (хлориды), +1 (гипохлориты), +3 (хлориты), +5 (хлораты) и +7 (перхлораты); электроотрицательность по Полингу 3,16; атомный радиус 99 пм; ионный радиус Сl– 184 пм. Молекула двухатомна, энергия диссоциации Cl2 239,24 кДж/моль.
При нормальных условиях Х. – жёлто-зелёный негорючий газ с резким удушающим запахом; tпл –100,98 °С, tкип –33,97 °С; плотность сухого газа 3,209 кг/м3 (0 °С), жидкого Х. 1558,9 кг/м3 (–33,97 °С). Хорошо растворим в неполярных жидкостях (напр., TiCl4, SiCl4, SnCl4, гексане, CCl4), умеренно – в воде (образуется «хлорная вода»). При темп-ре ниже 9,6 °С в водных растворах образует гидраты переменного состава Cl2·nH2O (n=6–8). Жидкий Х. – растворитель (TiCl4, SiCl4 и др.).
Х. – один из наиболее химически активных элементов; непосредственно взаимодействует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании) и неметаллами (реакции Х. с кислородом, азотом, инертными газами требуют спец. методов активации), образуя соответствующие хлориды. Замещает водород в насыщенных углеводородах и присоединяется к олефинам. Вытесняет бром и иод из их соединений с водородом и металлами (из соединений Х. с водородом и металлами вытесняется фтором). Смесь Х. с водородом горит при 2200 °С бесцветным или жёлто-зелёным пламенем с образованием хлороводорода (цепная реакция). Смеси Х. с водородом, содержащие 5,8–88,5% Н2, взрывоопасны. С кислородом Х. образует ряд оксидов (наиболее важны Cl2O, ClO2, Cl2O6 и Cl2O7); все оксиды Х. нестабильны и взрывоопасны. Бинарный хлорид азота NCl3, получаемый хлорированием аммиака или солей аммония, чрезвычайно взрывчат. С др. галогенами Х. образует межгалогенные соединения. О взаимодействии Х. с органич. веществами см. Галогенирование. Причина высокой химич. активности Х. – в сравнит. лёгкости образования атомов Cl из молекул Cl2, высоком сродстве атома Cl к электрону (348,7 кДж/моль – самое высокое среди химич. элементов) и высокой энергии связи Х. с большинством элементов.
Получение
Практически весь производимый Х. получают электролизом водных растворов NaCl (реже KCl); др. продукты электролиза – щёлочь (1,13 т NaOH на 1 т Cl2) и водород. Используют 3 метода электролиза: с ртутным катодом (Х. выделяется на твёрдом аноде, электродные пространства не разделены); диафрагменный (оба электрода твёрдые, анодное и катодное пространства разделены фильтрующей диафрагмой); мембранный (анодное и катодное пространства разделены катионообменной мембраной). Первые два метода существуют св. 100 лет, третий применяют в пром-сти с 1975. Мембранный метод позволяет достичь выхода по току 95–97% при концентрации щёлочи 32–35%, экологически менее опасен, требует меньшего расхода энергии (2000–2100 кВт·ч/т продукта) и меньших капиталовложений по сравнению с др. методами, поэтому доля Х., получаемого этим методом, непрерывно возрастает – по состоянию на 2015 св. 60% производств Х. в мире используют мембранную технологию. Материал мембран, пропускающих лишь ионы Na+ и K+, – как правило, фторсодержащие полимеры (срок службы – до 5 лет). Мировое произ-во Х. 53–55 млн. т/год (2015).
Применение
Х. используют для произ-ва окислительно-отбеливающих веществ – кальция гипохлорита, натрия гипохлорита, хлорной извести, хлоридов мн. элементов, ряда хлорорганич. продуктов (поливинилхлорида, хлоропренового каучука, дихлорэтана, хлороформа, эпихлоргидрина и др.), для водоочистки. В мире на произ-во хлорсодержащих органич. продуктов расходуется 60–75% производимого Х., неорганических – 10–15%, в целлюлозно-бумажной пром-сти – 5–15%.
Токсичен, раздражает слизистые оболочки, дыхательные пути и лёгкие. Х. – первое боевое отравляющее вещество, использованное во время 1-й мировой войны (см. в ст. Ипр).