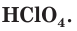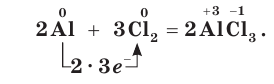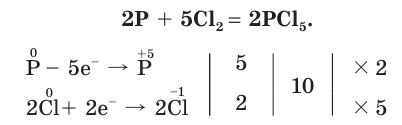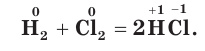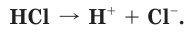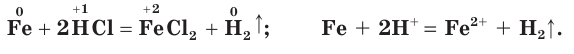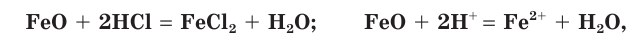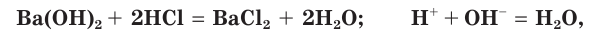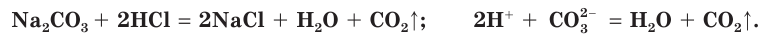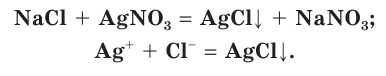ÐÑомами из благоÑоднÑÑ ÑлеменÑов ÑвлÑÑÑÑÑ Ð½Ð°Ð¸Ð±Ð¾Ð»ÐµÐµ ÑÑабилÑнÑми аÑомами из — за полноÑÑ Ð¸Ñ Ð²Ð½ÐµÑнего ÑÑÐ¾Ð²Ð½Ñ ÑнеÑгии Ñ ÑлекÑÑонами , Ñо аÑомÑ дÑÑÐ³Ð¸Ñ Â ÑлеменÑов , как пÑавило, Ð²Ñ Ð¾Ð´ÑÑ Ð²Â Ñ Ð¸Ð¼Ð¸ÑеÑÐºÐ¸Ñ ÑеакÑиÑÑ Â Ð´Ð»Ñ Ð´Ð¾ÑÑÐ¸Ð¶ÐµÐ½Ð¸Ñ ÑоÑÑоÑÐ½Ð¸Ñ ÑÑабилÑного , ÑÑÐ¾Ð±Ñ ÑÑаÑÑ Ð¸Ñ Ð²Ð½ÐµÑними ÑнеÑгеÑиÑеÑкими ÑÑовнÑми , ÑкомплекÑованнÑе ÑлекÑÑонами , поÑеÑÑв кÑайние ÑлекÑÑонÑ, как в меÑÐ°Ð»Ð»Ð°Ñ Â , за ÑÑÐµÑ Ð¿Ð¾Ð»ÑÑÐµÐ½Ð¸Ñ Ð¸Ð»Ð¸ обмена Ñ ÑлекÑÑонами, Ñакими как немеÑаллÑ , ÑÑо колиÑеÑÑво ÑлекÑÑонов извеÑÑно как валенÑноÑÑÑ .
ЧÑо Ñакое валенÑноÑÑÑ?
ÐаленÑноÑÑÑ — ÑÑо колиÑеÑÑво ÑлекÑÑонов, коÑоÑÑе аÑом пÑиобÑеÑаеÑ, ÑеÑÑÐµÑ Ð¸Ð»Ð¸ даже ÑазделÑÐµÑ Ð²Ð¾ вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии . ÐаленÑноÑÑÑ благоÑоднÑÑ Ð³Ð°Ð·Ð¾Ð²Â Ñавна нÑлÑ, поÑÐ¾Ð¼Ñ ÑÑо Ð¸Ñ Ð²Ð½ÐµÑний ÑнеÑгеÑиÑеÑкий ÑÑÐ¾Ð²ÐµÐ½Ñ Ð¿Ð¾Ð»Ð½Ð¾ÑÑÑÑ Ð·Ð°Ð¿Ð¾Ð»Ð½ÐµÐ½Â ÑлекÑÑонами [Ð¸Ð¼ÐµÐµÑ 8 ÑлекÑÑонов, кÑоме (He) Ð¸Ð¼ÐµÐµÑ 2 ÑлекÑÑона ], валенÑноÑÑÑ из ÑлеменÑа опÑеделÑеÑÑÑ Ð²Â ÑооÑвеÑÑÑвии Ñ ÑиÑлом ÑлекÑÑонов в наÑÑжном ÑнеÑгеÑиÑеÑком ÑÑовне его аÑома.
- ÐаÑÑий ( 11N a) ÑвлÑеÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑм (1), поÑÐ¾Ð¼Ñ ÑÑо он ÑеÑÑÐµÑ Ð¾Ð´Ð¸Ð½Â ÑлекÑÑон во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии .
- Ð¥Ð»Ð¾Ñ ( 17Cl) ÑвлÑеÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑм (1), поÑÐ¾Ð¼Ñ ÑÑо он пÑиобÑеÑÐ°ÐµÑ Ð¸Ð»Ð¸ делиÑÑÑ Ñ Ð¾Ð´Ð½Ð¸Ð¼Â ÑлекÑÑоном во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии .
- ÐиÑлоÑод( 8 O) ÑвлÑеÑÑÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм (2) , поÑколÑÐºÑ Ð¾Ð½Ð° полÑÑÐ°ÐµÑ Ð¸Ð»Ð¸ акÑий двÑÑ Â ÑлекÑÑонов в Ñ Ð¾Ð´ÐµÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии .
- Ðагний ( 12Mg) двÑÑ Ð²Ð°Ð»ÐµÐ½Ñен (2), поÑÐ¾Ð¼Ñ ÑÑо он ÑеÑÑÐµÑ Ð´Ð²Ð°Â ÑлекÑÑона во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии .
- ÐлÑминий ( 13Al) ÑвлÑеÑÑÑ ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм (3), поÑÐ¾Ð¼Ñ ÑÑо он ÑеÑÑÐµÑ ÑÑи ÑлекÑÑона во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии .
- ÐÑгон ( 18Ar) Ñавен нÑлÑ, поÑÐ¾Ð¼Ñ ÑÑо он не ÑеÑÑеÑ, не полÑÑÐ°ÐµÑ Ð¸ не делиÑÑÑ Ñ ÑлекÑÑонами из-за полноÑÑ Ð¸Ñ Ð²Ð½ÐµÑÐ½Ð¸Ñ ÑнеÑгеÑиÑеÑÐºÐ¸Ñ ÑÑовней Ñ ÑлекÑÑонами .
ÐаленÑноÑÑи некоÑоÑÑÑ Ð¼ÐµÑаллиÑеÑÐºÐ¸Ñ ÑлеменÑов
- ÐиÑий (Li), калий (K), наÑÑий (Na) и ÑеÑебÑо (Ag) ÑвлÑÑÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑми (1).
- ÐалÑÑий (Ca), магний (Mg), ÑÐ²Ð¸Ð½ÐµÑ (Pb), ÑÑÑÑÑ (Hg) и Ñинк (Zn) двÑÑ Ð²Ð°Ð»ÐµÐ½ÑÐ½Ñ (2).
- ÐлÑминий (Al) и золоÑо (AU) ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½ÑÐ½Ñ (3).
ÐекоÑоÑÑе меÑаллиÑеÑкие ÑлеменÑÑ имеÑÑ Ð±Ð¾Ð»ÐµÐµ одной валенÑноÑÑи :
- ÐÐµÐ´Ñ (Cu): ÐÐµÐ´Ñ Î (одноваленÑнаÑ) (1) и ÐÐµÐ´Ñ IÎ (двÑÑ Ð²Ð°Ð»ÐµÐ½ÑнаÑ) (2).
- Ðелезо (Fe): двÑÑ Ð²Ð°Ð»ÐµÐ½Ñное железо IÎ ( двÑÑ Ð²Ð°Ð»ÐµÐ½Ñное Fe +2) и ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½Ñное железо IIÎ ( ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½Ñное железо Fe +3 ) (3).
ÐаленÑноÑÑи некоÑоÑÑÑ Ð½ÐµÐ¼ÐµÑаллиÑеÑÐºÐ¸Ñ ÑлеменÑов
- ÐодоÑод (H), Ñ Ð»Ð¾Ñ (Cl), ÑÑÐ¾Ñ (F), бÑом (Br) и йод (I) ÑвлÑÑÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑми (1).
- ÐиÑлоÑод(O) двÑÑ Ð²Ð°Ð»ÐµÐ½Ñен.
- УглеÑод (C) ÑеÑÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½Ñен.
ÐекоÑоÑÑе немеÑаллиÑеÑкие ÑлеменÑÑ, коÑоÑÑе имеÑÑ Ð±Ð¾Ð»ÐµÐµ одной валенÑноÑÑи, напÑимеÑ:
- СеÑа (S) бÑÐ²Ð°ÐµÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½Ñной (2), ÑеÑÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½Ñной (4) и ÑеÑÑиваленÑной (6).
- ÐÐ·Ð¾Ñ (N) бÑÐ²Ð°ÐµÑ ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм (3) и пÑÑиваленÑнÑм (5).
- ФоÑÑÐ¾Ñ (P) бÑÐ²Ð°ÐµÑ ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм (3) и пÑÑиваленÑнÑм (5).
ÐÑÐ¾Ð¼Ð½Ð°Ñ Ð³ÑÑппа
ÐÑÐ¾Ð¼Ð½Ð°Ñ Ð³ÑÑппа (ÑадикалÑнаÑ) пÑедÑÑавлÑÐµÑ Ñобой набоÑ аÑомов ÑазлиÑнÑÑ Â ÑлеменÑов, обÑединеннÑÑ Ð²Ð¼ÐµÑÑе и ведÑÑÐ¸Ñ ÑÐµÐ±Ñ ÐºÐ°Ðº один аÑом во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑкой ÑеакÑии , Ð¸Ð¼ÐµÑ ÑÐ²Ð¾Ñ ÑобÑÑвеннÑÑ валенÑноÑÑÑ и не ÑÑÑеÑÑвÑÐµÑ Ð¾ÑделÑно (индивидÑалÑно), валенÑноÑÑÑ аÑомной гÑÑÐ¿Ð¿Ñ Ñавна колиÑеÑÑÐ²Ñ Ð¾Ð±Ð²Ð¸Ð½ÐµÐ½Ð¸Ñ, коÑоÑÑе он неÑеÑ.
ÐÑимеÑ: бикаÑбонаÑÐ½Ð°Ñ Ð³ÑÑппа (HCO 3 ) — , ее валенÑноÑÑÑ одноваленÑнаÑ, она ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· 5 аÑомов 3 ÑлеменÑов , одного аÑома водоÑода (H), одного аÑома ÑглеÑода (C), ÑÑÐµÑ Ð°Ñомов киÑлоÑодного ÑлеменÑа (O). .
ÐаленÑноÑÑи некоÑоÑÑÑ Ð°ÑомнÑÑ Ð³ÑÑпп
- ÐидÑокÑид (OH —), бикаÑÐ±Ð¾Ð½Ð°Ñ (HCO 3 ) — , ниÑÑÐ°Ñ (NO 3 ) — , ниÑÑÐ¸Ñ (NO 2 ) — , аммоний (NH 4 ) + ÑвлÑÑÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑми (1).
- ÐаÑÐ±Ð¾Ð½Ð°Ñ (CO 3) -2 , ÑÑлÑÑÐ°Ñ (SO 4 ) -2 двÑÑ Ð²Ð°Ð»ÐµÐ½ÑÐ½Ñ (2).
- ФоÑÑÐ°Ñ (PO 4) -3 ÑвлÑеÑÑÑ ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм (3).
ХимиÑеÑÐºÐ°Ñ ÑоÑмÑла
СоÑÑавнÑе молекÑÐ»Ñ Ð¾Ð±ÑазÑÑÑÑÑ Ð² ÑезÑлÑÑаÑе комбинаÑии аÑомов ÑазнÑÑ Â ÑлеменÑов вмеÑÑе. ÐÑ Ð¼Ð¾Ð¶ÐµÐ¼ вÑÑазиÑÑ Ð¼Ð¾Ð»ÐµÐºÑÐ»Ñ Ñ Ð¸Ð¼Ð¸ÑеÑкого ÑÐ¾ÐµÐ´Ð¸Ð½ÐµÐ½Ð¸Ñ Ñ Ð¿Ð¾Ð¼Ð¾ÑÑÑ Ð¾Ð¿Ñеделенной ÑоÑмÑлÑ, извеÑÑной как Ñ Ð¸Ð¼Ð¸ÑеÑÐºÐ°Ñ ÑоÑмÑла.Â Ñ Ð¸Ð¼Ð¸ÑеÑÐºÐ°Ñ ÑоÑмÑла — ÑÑо ÑоÑмÑла, коÑоÑÐ°Ñ Ð¿ÑедÑÑавлÑÐµÑ ÐºÐ¾Ð»Ð¸ÑеÑÑво и Ñип аÑомов в молекÑле .
ÐолекÑла водÑ (H 2 O) ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· двÑÑ Ð°Ñомов водоÑода (H) и одного аÑома киÑлоÑода (O), молекÑла Ñ Ð»Ð¾Ñида наÑÑÐ¸Ñ (NaCl) ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· одного аÑома наÑÑÐ¸Ñ (Na) и одного аÑома Ñ Ð»Ð¾Ñа. (Cl).
Ðак можно напиÑаÑÑ Ñ Ð¸Ð¼Ð¸ÑеÑкÑÑ ÑоÑмÑÐ»Ñ ÑоединениÑ?
- ÐапиÑиÑе название ÑÐ¾ÐµÐ´Ð¸Ð½ÐµÐ½Ð¸Ñ Ð¿ÑопиÑÑÑ.
- ÐапиÑиÑе Ñимвол каждого ÑлеменÑа или аÑомной гÑÑÐ¿Ð¿Ñ Ð´Ð¾ его имени.
- ÐапиÑиÑе валенÑноÑÑÑкаждого Ñимвола или аÑомной гÑÑÐ¿Ð¿Ñ Ð¸Â Ð¿Ð¾Ð¼ÐµÐ½ÑйÑе валенÑноÑÑи .
- УпÑоÑÑиÑе валенÑноÑÑи(макÑималÑно ÑокÑаÑиÑе Ð¸Ñ ), вам не нÑжно пиÑаÑÑ ÐµÐ´Ð¸Ð½Ð¸ÑÑ (1), в ÑлÑÑае аÑомнÑÑ Ð³ÑÑпп, еÑли ÑиÑло не (1), помеÑÑиÑе аÑомнÑÑ Ð³ÑÑÐ¿Ð¿Ñ Ð² Ñкобки и запиÑиÑе ÑиÑло пÑÑмо вниз к немÑ.
ФоÑмÑла ÑÐ¾ÐµÐ´Ð¸Ð½ÐµÐ½Ð¸Ñ Ð½Ð°ÑинаеÑÑÑ Ñлева Ñимволом меÑалла, водоÑода или положиÑелÑной аÑомной гÑÑппÑ, заканÑиваеÑÑÑ ÑпÑава Ñимволом немеÑалла или оÑÑиÑаÑелÑной аÑомной гÑÑппÑ. Слово окÑид ознаÑÐ°ÐµÑ ÐºÐ¾Ð¼Ð±Ð¸Ð½Ð°ÑиÑ меÑаллиÑеÑкого ÑлеменÑа или немеÑаллиÑеÑкий ÑлеменÑ Ñ киÑлоÑоднÑм ÑлеменÑом.
ÐиÑлоÑода аÑом ÑоединÑÐµÑ Ð´Ð²Ð°Â Ð°Ñома наÑÑÐ¸Ñ Ð¿Ñи Ñоздании одной молекÑÐ»Ñ Ð¾ÐºÑида наÑÑÐ¸Ñ (Na 2 O) , поÑÐ¾Ð¼Ñ ÑÑо киÑлоÑод ÑвлÑеÑÑÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм, в Ñо вÑÐµÐ¼Ñ ÐºÐ°Ðº наÑÑий одноваленÑного, ХимиÑеÑÐºÐ°Ñ ÑоÑмÑла каÑбонаÑа наÑÑÐ¸Ñ (Na 2 CO 3 ) , Ñак как наÑÑий одноваленÑного, в Ñо вÑÐµÐ¼Ñ ÐºÐ°Ðº каÑÐ±Ð¾Ð½Ð°Ñ ÑвлÑеÑÑÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½Ñной гÑÑппой.
Ðалий ( 19 K) ÑвлÑеÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑм, в Ñо вÑÐµÐ¼Ñ ÐºÐ°ÐºÂ ÐºÐ¸ÑлоÑод ( 8 O) ÑвлÑеÑÑÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм, поÑÐ¾Ð¼Ñ ÑÑо во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑÐºÐ¸Ñ ÑеакÑий аÑом ÐºÐ°Ð»Ð¸Ñ ÑеÑÑÐµÑ Ð¾Ð´Ð¸Ð½Â ÑлекÑÑон , в Ñо вÑÐµÐ¼Ñ ÐºÐ°ÐºÂ ÐºÐ¸ÑлоÑод полÑÑÐ°ÐµÑ Ð¸Ð»Ð¸ делиÑÑÑ Ñ Ð´Ð²ÑмÑ ÑлекÑÑонами, ÑÑÐ¾Ð±Ñ Ð·Ð°Ð²ÐµÑÑиÑÑ ÑÐ²Ð¾Ñ Ð²Ð½ÐµÑнÑÑ Ð¾Ð±Ð¾Ð»Ð¾ÑкÑ. Ðагний ( 12 Mg) двÑÑ Ð²Ð°Ð»ÐµÐ½Ñен, а алÑминий ( 13 Al) ÑÑÐµÑ Ð²Ð°Ð»ÐµÐ½Ñен, поÑÐ¾Ð¼Ñ ÑÑо в Ñ Ð¾Ð´ÐµÂ Ñ Ð¸Ð¼Ð¸ÑеÑÐºÐ¸Ñ ÑеакÑий аÑом Ð¼Ð°Ð³Ð½Ð¸Ñ ÑеÑÑÐµÑ Ð´Ð²Ð°Â ÑлекÑÑона , а аÑом алÑÐ¼Ð¸Ð½Ð¸Ñ ÑеÑÑÐµÑ ÑÑи ÑлекÑÑона .
РнаÑÑий ( 11 Na), и Ñ Ð»Ð¾Ñ ( 17 Cl) ÑвлÑÑÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑми, Ñ Ð¾ÑÑ Ñ Ð½Ð¸Ñ ÑазнÑе аÑомнÑе номеÑа, поÑÐ¾Ð¼Ñ ÑÑо во вÑемÑÂ Ñ Ð¸Ð¼Ð¸ÑеÑÐºÐ¸Ñ ÑеакÑий аÑом наÑÑÐ¸Ñ ÑеÑÑÐµÑ Ð¾Ð´Ð¸Ð½ ÑлекÑÑон, а аÑом Ñ Ð»Ð¾Ñа полÑÑÐ°ÐµÑ Ð¾Ð´Ð¸Ð½Â ÑлекÑÑон или делиÑÑÑ Ñ Ð½Ð¸Ð¼, ÑÑÐ¾Ð±Ñ Ð·Ð°Ð²ÐµÑÑиÑÑ ÑÐ²Ð¾Ñ Ð²Ð½ÐµÑнÑÑ Ð¾Ð±Ð¾Ð»Ð¾ÑкÑ.
ÐаленÑноÑÑÑ из благоÑоднÑÑ Ð³Ð°Ð·Ð¾Ð²Â Ñавна нÑÐ»Ñ , Ñак ÐºÐ°ÐºÂ Ð¸Ñ Ð²Ð½ÐµÑние ÑнеÑгеÑиÑеÑкие ÑÑовни полноÑÑÑÑ Ð·Ð°Ð¿Ð¾Ð»Ð½ÐµÐ½Ñ ÑлекÑÑонами , поÑÑомÑ, они не ÑеÑÑÑÑ, или полÑÑиÑÑ Ð´Ð¾Ð»Ñ Ñ Ð»ÑбÑми ÑлекÑÑонами . ÐиÑлоÑода аÑом ÑоединÑÐµÑ Ð´Ð²Ð°Â Ð°Ñома наÑÑÐ¸Ñ Ð¿Ñи Ñоздании одной молекÑÐ»Ñ Ð¾ÐºÑида наÑÑÐ¸Ñ , поÑÐ¾Ð¼Ñ ÑÑо киÑлоÑод ÑвлÑеÑÑÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½ÑнÑм, в Ñо вÑÐµÐ¼Ñ ÐºÐ°Ðº наÑÑий одноваленÑнÑй.
РниÑÑаÑнаÑ, и каÑбонаÑÐ½Ð°Ñ Ð³ÑÑÐ¿Ð¿Ñ Ð¸Ð¼ÐµÑÑ Ð¾Ð´Ð¸Ð½Ð°ÐºÐ¾Ð²Ð¾Ðµ колиÑеÑÑво аÑомов, но ÑазлиÑаÑÑÑÑ Ð¿Ð¾ Ñвоей валенÑноÑÑи, поÑÐ¾Ð¼Ñ ÑÑо ниÑÑаÑÐ½Ð°Ñ Ð³ÑÑппа (NO 3 ) — ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· ÑеÑÑÑÐµÑ Ð°Ñомов и ÑвлÑеÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½Ñной гÑÑппой, Ñогда как каÑбонаÑÐ½Ð°Ñ Ð³ÑÑппа (CO 3 ) -2 ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· ÑеÑÑÑÐµÑ Ð°Ñомов, но она ÑвлÑеÑÑÑ Ð´Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½Ñной гÑÑппой. Ðбе ниÑÑиÑнÑе и ниÑÑаÑнÑе гÑÑÐ¿Ð¿Ñ ÑазлиÑаÑÑÑÑ ÑиÑлом аÑомов и имеÑÑ Ð¾Ð´Ð¸Ð½Ð°ÐºÐ¾Ð²ÑÑ Ð²Ð°Ð»ÐµÐ½ÑноÑÑÑ, поÑколÑÐºÑ Ð¾Ð±Ðµ ÑвлÑÑÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑми, но ниÑÑаÑÐ½Ð°Ñ (NO 3 ) — гÑÑппа ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· 4 аÑомов , а ниÑÑиÑÐ½Ð°Ñ (NO 2 ) — гÑÑппа ÑоÑÑÐ¾Ð¸Ñ Ð¸Ð· 3 аÑомов.
ХимиÑеÑÐºÐ°Ñ ÑоÑмÑла каÑбонаÑа наÑÑÐ¸Ñ (Na 2 CO 3 ), поÑÐ¾Ð¼Ñ ÑÑо наÑÑий ÑвлÑеÑÑÑ Ð¾Ð´Ð½Ð¾Ð²Ð°Ð»ÐµÐ½ÑнÑм, а каÑÐ±Ð¾Ð½Ð°Ñ — двÑÑ Ð²Ð°Ð»ÐµÐ½Ñной гÑÑппой, поÑÑÐ¾Ð¼Ñ Ð´Ð²Ð°Â Ð°Ñома наÑÑÐ¸Ñ ÑоединÑÑÑÑÑ Ñ Ð¾Ð´Ð½Ð¸Ð¼ аÑомом каÑбонаÑной гÑÑппÑ. ХимиÑеÑÐºÐ°Ñ ÑоÑмÑла водÑ — (H 2 O), поÑÐ¾Ð¼Ñ ÑÑо киÑлоÑод двÑÑ Ð²Ð°Ð»ÐµÐ½Ñен, а водоÑод одноваленÑен, поÑÑÐ¾Ð¼Ñ Ð´Ð²Ð° аÑома водоÑода ÑоединÑÑÑÑÑ Ñ Ð¾Ð´Ð½Ð¸Ð¼ аÑомом киÑлоÑода .
Всем известная хлорка и хлорсодержащие моющие средства – ничто иное как опасный токсин. Его также можно встретить в составе инсектицидов, некоторых медикаментов, растворителей и ядохимикатов. Хлорные таблетки – самое дешевое средство для дезинфекции бассейнов. При этом признаки отравления хлором у человека зависят как от степени тяжести (концентрации токсина), так и от способа, которым яд попал в организм.
Источник: https://medvisor.ru/articles/otravleniya/otravlenie-khlorom/
Что такое хлор и как им можно отравиться
Хлор (Cl) – элемент Периодической таблицы с атомным номером 17. Он относится к группе галогенов и в наиболее простой своей форме представляет собой удушающий газ желтовато-зеленоватого цвета. Он тяжелее воздуха, потому стелется по земле, имеет характерный запах, а при вдыхании провоцирует приступ асфиксии.
Разумеется, газообразная форма хлора практически нигде не встречается (разве что в химическом оружии). Чаще всего это более инертные соединения в жидкой или твердой форме. К примеру, всем известный хлорный отбеливатель «Белизна» – это гипохлорит натрия (соединение натриевой соли и хлорноватистой кислоты).
У хлора есть и биологическая роль, то есть в некоторой мизерной концентрации он присутствует в живых клетках растений, животных и человека, участвуя в обменных процессах:
-
Поддержание осмотического баланса и регуляция объема жидкости в клетках;
-
Тормозящий эффект в возбуждении нейронов;
-
Выработка протеолитических ферментов желудочного сока.
Самая распространенная сфера применения хлора – это обеззараживание воды, поскольку он чрезвычайно эффективен против микробов. Также в быту им пользуются для отбеливания тканей, уборки и дезинфекции помещений
Отравление хлором – это по большому счету отравление его парами. Наиболее типичное место – общественные бассейны, где и по сей день хлорными таблетками пользуются для дезинфекции. Испарения от воды становятся токсичными, если превышена предельно допустимая концентрация хлора.
Такие печальные случаи происходят с завидной регулярностью. В качестве примера можно назвать
смертельное отравление хлором, которое произошло с российскими туристами в Албании. В сауне местного отеля насмерть задохнулось четверо человек. Предварительной причиной названо хлорсодержащее чистящее средство, которым персонал гостиницы пользовался для мытья бассейна.
Как ещё можно отравиться хлором:
-
Уборка помещений. Хлорсодержащие моющие средства, в частности, уже упомянутый гипохлорит натрия в таблетках, могут послужить причиной отравления, что регулярно случается с уборщицами и санитарками больниц. Причина та же – превышение допустимой концентрации;
-
Лабораторная утечка или авария на предприятии;
-
Применение боевых отравляющих веществ с хлором (крайняя редкость в наши дни);
-
Случайное проглатывание или попытка суицида;
-
Несоблюдение техники безопасности и попадание хлора на слизистые оболочки рта, глаз.
Опаснее всего хлор, безусловно, для маленьких детей. Именно поэтому вся бытовая хлорсодержащая химия должна храниться в недоступных местах

Designed by Cyberchemist/flickr
Каковая смертельная доза хлора?
Все химические отравления принято делить по степени воздействия ядовитого вещества. В случае с хлором она рассчитывается из концентрации токсина в воздухе.
|
| Концентрация Cl на кубический метр воздуха | Признаки отравления хлором |
| Легкая форма | 0,012 г/м3 | Человек остается в сознании, жалуется на одышку, сильный кашель. Госпитализация не требуется, отравление проходит спустя 12–24 часа |
| Средней тяжести | 0,09 г/м3 | Есть признаки интоксикации, ухудшение самочувствия, сознание в норме, жалобы на боль в горле, надсадный кашель. Требуется медицинская помощь. Симптомы, как правило, проходят спустя 72 часа |
| Тяжелая форма | 0,1–0,5 г/м3 | Выраженная дыхательная недостаточность, обструкция дыхательных путей из-за спазма, кома, спустя 3–8 часов наступает отек легких. Медицинская помощь должна быть оказана незамедлительно. |
| Смертельная форма | 0,5–1,2 г/м3 | Пострадавший погибает от удушья спустя 10–15 минут, ларингоспазм снять невозможно. |
| Молниеносная форма | От 1,5 г/м3 | Смерть наступает из-за единомоментного поступления большой дозы хлора. От момента вдыхания до летального исхода проходит 30–60 секунд. |
Таким образом смертельная доза хлора для человека при вдыхании начинается от 0,1 граммов на кубический метр воздуха. И если при такой концентрации пострадавшего ещё можно спасти, то при превышении концентрации в 0,5 граммов на кубометр медицинские манипуляции уже бесполезны.
Симптомы отравления хлором у человека
Интоксикация, если она не произошла внезапно, нарастает постепенно по мере проникновения ядовитого вещества в легкие и кровь.
В легкой форме отравление хлором сопровождается головной болью, першением в горле, умеренным головокружением. Симптомы довольно быстро проходят, но пострадавший всё равно нуждается в медицинском наблюдении
Симптомы отравления хлором у человека могут быть и более выраженными:
-
Надсадный лающий кашель;
-
Слюнотечение и слезотечение;
-
Осиплость голоса;
-
Тошнота, рвота;
-
Боли в животе (эпигастральной области);
-
Хрипы при дыхании;
-
Психомоторное возбуждение;
-
Отечность гортани;
-
Учащенное дыхание.
Симптомы тяжелого отравления хлором также начинаются с приступа удушья и надсадного кашля. Если пострадавший был вовремя эвакуирован из места заражения, довольно быстро начинается период ремиссии, кашель прекращается. Длиться это состояние может до 8 часов, и кажется, что опасность миновала. Однако затем неизбежно начинаются:
-
Хрипы в груди;
-
Тахикардия;
-
Судороги;
-
Пенистая мокрота изо рта;
-
Падение АД;
-
Отек легких.
Вдыхание смертельной дозы хлора довольно быстро заканчивается потерей сознания, конвульсиями. Губы и пальцы пострадавшего синеют, кожные покровы бледнеют, на шее вздуваются вены, зрачки расширены. Всё это проявления ларингоспазма. Снять его при помощи медикаментов невозможно, человек умирает от удушья примерно за 3 минуты.

Designed by brgfx/freepik
Что случится, если съесть или выпить хлорку
Гипохлорит натрия или хлорная известь, несмотря на то, что являются стабильным соединением, не менее смертоносны. Попадая в организм, они неминуемо приводят к ожогу гортани, пищевода и желудка. Почти сразу начинаются:
-
Режущие боли в животе;
-
Рвота с кровью;
-
Диарея, также кровавая;
-
Слабость, головокружение;
-
Тахикардия;
-
Повышение температуры;
-
Изъязвление стенок желудка, сильное внутреннее кровотечение практически неизбежны. При повреждении пищевода кровь остановить очень трудно.
Мучительная гибель может наступить уже спустя 20–30 минут, если пострадавший не был вовремя доставлен в медицинское учреждение. Даже если удастся спасти жизнь, он в большинстве случаев остается инвалидом
Что делать при отравлении хлором
Итак, запомнили: чем дольше человек подвергается воздействию паров хлора, тем тяжелее отравление. Поэтому первым делом следует как можно быстрее выйти из загазованного помещения и вынести пострадавших. В идеале на каждом должен быть противогаз. Однако, если его нет, старайтесь дышать через марлевую повязку или тряпку, пропитанную водой.
При непосредственном контакте с хлором ни в коем случае не трите глаза, нос или рот! Промойте руки под проточной водой и тщательно вымойте их с мылом
Далее нужно в обязательном порядке вызвать МЧС и «скорую помощь» (единый телефон 112). Как помочь человеку с хлорным отравлением до приезда медиков:
-
Расстегните и ослабьте стесняющую одежду;
-
Промойте глаза, помогите прополоскать рот проточной водой, либо раствором пищевой соды;
-
Дайте пострадавшему обильное питье, лучше всего, чтобы это была вода с содой, молоко или минералка с щелочным составом;
-
Успокоить пострадавшего, обеспечить ему комфорт.
Чтобы снять брохноспазм, необходимы ингаляции с сальбутамолом или беродуалом – препаратами, используемыми для лечения бронхиальной астмы. Если таковые есть под рукой, немедленно воспользуйтесь!
Если человек проглотил хлорсодержащее вещество, всё что можно сделать, это как можно скорее промыть желудок. Однако делать это следует, если нет кровавой рвоты, а сам пострадавший находится в сознании.
Помните о том, что любой человек с признаками отравления хлором всегда подлежит госпитализации. Только медучреждении могут грамотно определить степень интоксикации и оказать всю необходимую помощь.
Как лечат отравление парами хлора
В стационаре пациенту понадобится комплексная терапия:
-
Кислородная поддержка и скорее всего перевод на ИВЛ;
-
Предупреждение отека легких;
-
Прием брондиалатаров, спазмолитиков, антибиотиков, отхаркивающих и стероидных противовоспалительных средств;
-
Поддержание водно-солевого баланса.
Практически всегда после хлорного отравления у человека остаются повреждены бронхи и легкие, в ряде случаев повреждения необратимы. Реабилитация может занять от 6 до 12 месяцев. Однако при легком и средней тяжести отравлении прогноз обычно благоприятный.

Designed by James Heilman, MD/wikimedia
Последствия отравления хлором
Самое, пожалуй, опасное осложнение – это стремительно нарастающий отек легких. Им сопровождается примерно 75% тяжелых случаев. В дальнейшем у пострадавшего с большой вероятностью может развиться эмфизема – патологическое расширение легочной ткани. Не менее опасна энцефалопатия – отек мозга, который развивается из-за длительного кислородного голодания.
Перенесшие отравление в легкой и средней тяжести форме могут столкнуться с массой хронических заболеваний:
-
Бронхит, фарингит, трахеит;
-
Хроническая сердечная недостаточность;
-
Бронхоэктатическая болезнь.
-
С нарушенной дыхательной функцией человек становится более уязвимым к тяжелыми инфекционным поражениям легких и бронхов.
Как можно обезопасить себя от отравления хлором
Профилактика отравлений хлором сводится к соблюдению техники безопасности при работе с токсическими веществами:
-
Работать с ними нужно в хорошо вентилируемых помещениях;
-
Работать в перчатках, защитной маске, либо респираторе, особенно если это инсектициды или пестициды;
-
При работе с агрессивными моющими веществами также желательно пользоваться респиратором или по крайней мере ватно-марлевой повязкой;
-
Разводите средство согласно инструкции, не превышая указанную дозировку;
-
Храните хлорсодержащие вещества и бытовую химию в недоступном для детей месте.
Итог
Признаки отравления хлором у человека зависят от степени тяжести. Однако, поскольку это яд удушающего действия, практически все симптомы сосредоточены в органах дыхания. Человека будут мучать сильный кашель, слезотечение, головокружение, боль в горле, хрипы. Даже при легкой степени отравления следует обратиться за медицинской помощью.
Что такое восстановление по химии?
Восстановление, в химии, — это процесс, в результате которого: частица (атом, ион или молекула) принимает один или несколько электронов; происходит понижение степени окисления какого-либо атома в данной частице; органическое вещество теряет атомы кислорода и (или) приобретает атомы водорода.
Как узнать кто окислитель а кто восстановитель?
Окислитель – это вещество, молекулы или ионы которого принимает электроны. Если элемент является окислителем, его степень окисления понижается. Восстановитель – это вещество, молекулы или ионы которого отдают электроны. У восстановителя степень окисления повышается.
Что такое окислитель и восстановитель в химии?
Окислитель – это вещество, которое содержит элемент в максимальной степени окисления. Восстановитель – это вещество, которое содержит элемент в минимальной степени окисления. В окислительно-восстановительной реакции восстановитель отдает электроны, при этом степень окисления повышается.
Что такое окислитель и восстановитель пример?
Вещество, частицы которого содержат окисляющиеся атомы, выполняет в реакции функцию восстановителя. В данном примере восстановитель — сероводород H2S. Вещество, частицы которого содержат восстанавливающиеся атомы, выполняет в реакции функции окислителя. В данном примере окислитель — молекулярный кислород О2.
Что называется окислительно восстановительной реакцией?
Окислительно-восстановительные процессы Окислительно-восстановительными (см. с. 24) (или редокc-реакциями) называются реакции, сопровождающиеся переносом электронов от донора к акцептору (1).
Какие вещества называют окислителями?
Окисли́тель — вещество, в состав которого входят атомы, присоединяющие к себе во время химической реакции электроны. Иными словами, окислитель — это акцептор электронов.
Как определить какой восстановитель сильнее?
Восстановители можно ранжировать по увеличению силы путем ранжирования их восстановительных потенциалов. Восстановитель сильнее, когда он имеет более отрицательный восстановительный потенциал, и слабее, когда он имеет более положительный восстановительный потенциал.
Кто самый сильный восстановитель?
Чем левее стоит металл в ряду стандартных электродных потенциалов, тем более сильным восстановителем он является, самый сильный восстановитель – металлический литий, золото – самый слабый, и, наоборот, ион золото (III) – самый сильный окислитель, литий (I) – самый слабый.
Какие атомы являются окислителями?
Атомы с максимальными значениями степени окисления могут быть только окислителями….Важнейшие окислители:
- галогены F 2 , Cl 2 ;
- кислород O 2 , озон O 3 ;
- соединения марганца KMn O 4 ;
- азотная кислота HN O 3 и её соли KN O 3 ;
- концентрированная серная кислота H 2 S O 4 ;
- ионы металлов.
Какие ионы могут быть только окислителями?
Окислителями могут быть нейтральные атомы и молекулы; положительно Заряженные ионы металлов; сложные ионы и молекулы, содержащие атомы металла в состоянии высокой степени окисления; сложные ионы и молекулы, содержащие атомы неметалла в состоянии положительной степени окисления; положительно заряженные ионы водорода (в …
Какой атом наиболее сильный окислитель?
Самым сильным окислителем из нейтральных атомов является фтор, самым слабым — свинец. Взаимодействуя с более сильными окислителями, вышеперечисленные элементы (за исключением фтора и кислорода), выступают в роли восстановителей, т. е., отдают свои электроны.
Какие важнейшие окислители и восстановители известны?
Краткий перечень важнейших окислителей и восстановителей (подробные перечни — см. ниже):
- Металлы,
- Водород,
- Уголь,
- Окись углерода (II) (CO)
- Сероводород (H2S),
- Оксид серы (IV) (SO2),
- Cернистая кислота H2SO3 и ее соли,
- Галогеноводородные кислоты и их соли,
Какие вещества могут быть только восстановителем?
или только восстановителями (NH3, H2S, галогеноводороды, Na2S2O3 и др.). Вещества, содержащие элементы в промежуточных степенях окисления, могут быть как окислителями, так и восстановителями (HClO, H2O2, H2SO3 и др.).
Какие простые вещества являются только восстановителями?
Среди простых веществ к типичным восстановителям принадлежат активные металлы (щелочные и щёлочноземельные, алюминий, цинк, железо и др.), а также некоторые неметаллы, такие, как водород, углерод (в виде угля или кокса), фосфор, кремний.
Как считать Овр?
Для составления уравнений ОВР используют метод электронного баланса. Метод основан на том, что в ОВР соблюдается правило: общее число электронов, отданных восстановителем, равно общему числу электронов, принятых окислителем.
Что показывает электронный баланс?
Метод электронного баланса используется для расстановки коэффициентов в уравнениях окислительно-восстановительных реакций. Суть метода заключается в том, что количество электронов, отданных восстановителями равно количеству электронов, принятых окислителями. Отдельно суммируем число отданных электронов и принятых.
Как расставить степень окисления?
Для подсчета степеней окисления имеется ряд простых правил: Степень окисления элемента в составе простого вещества принимается равной нулю. Если вещество находится в атомарном состоянии, то степень окисления его атомов также равна нулю. Ряд элементов проявляют в соединениях постоянную степень окисления.
Как определить степень окисления Химия 8 класс?
Степень окисления — условный заряд атома в соединении, если считать, что связь в нём ионная. Степень окисления равна числу электронов, смещённых от атома или к атому. Если электроны смещаются от атома, то его степень окисления положительная.
Как определить низшую степень окисления?
Высшая степень окисления равна номеру группы со знаком «плюс». Низшая определяется, как номер группы минус 8. И промежуточная степень окисления — это почти любое целое число в интервале от низшей степени окисления до высшей.
Что такое валентность и степень окисления?
Понятие валентность используется для количественного выражения электронного взаимодействия в ковалентных соединениях, то есть в соединениях, образованных за счет образования общих электронных пар. Степень окисления используется для описания реакций, которые сопровождаются отдачей или присоединением электронов.
Каковы валентность и степень окисления азота в азотной кислоте?
Строение молекулы Таким образом в целом, азот образует 4 связи. В HNO3 валентность азота равна 4, степень окисления +5, оба атома кислорода связаны с атом азота равноценно.
В чем разница между зарядом и степенью окисления?
Степень окисления — условный заряд одного атома, Заряд иона — обычно реальный заряд иона. Ионы могут состоять из нескольких атомов. Чтобы не путать, принято (обязательно) в заряде иона сначала писать цифру, затем знак, а в степени окисления — сначала знак, потом цифру.
Что такое валентность металлов?
Валентность — это способность атома данного элемента образовывать определенное количество химических связей. Можно сказать иначе: валентность — это способность атома данного элемента присоединять определенное число других атомов.
Что такое валентность простыми словами?
Вале́нтность (от лат. valēns «имеющий силу») — способность атомов химических элементов образовывать определённое число химических связей.
Что такое валентность объясните примерами?
Валентность-способность атомов присоединять и удерживать определенное число атомов химического элемента. Например:CuO Валентность меди по таблице Менделеева 2(см. на номер группы,именно по ней определяется валентность),а валентность кислорода всегда равна 2,т. к в соединениях кислород проявляет низшую валентность.
Как правильно определить валентность химических элементов?
Алгоритм определения валентности по формулам химических элементов.
- Записать формулу химического соединения.
- Обозначить известную валентность элементов.
- Найти наименьшее общее кратное валентности и индекса.
- Найти соотношение наименьшего общего кратного к количеству атомов второго элемента.
Как определить валентность по таблице?
Номер группы, в которой расположен атом в периодической таблице равен его высшей валентности. Низшая валентность определяется разницей между числом восемь и номером группы. Натрий и алюминий имеют только одно значение валентности, равное номеру группы.
Какая может быть валентность у азота?
Высшая валентность атома равна номеру группы, в которой он расположен, а низшая – разнице между числом восемь и номером группы. Азот – элемент второго периода VA группы, следовательно, высшая валентность для него будет равна V, а низшая – III. Кроме указанных, для азота характерны валентности I, II и IV, т.
Какая валентность может быть у хлора?
Наличие трех, пяти и семи неспаренных электронов в возбужденном состоянии свидетельствует о том, что хлор проявляет в своих соединениях валентности III (NaClIIIO2), V (KClVO3) и VI (KClVIIO4, ClVII2O7) (высшая валентность). Формально хлор может проявлять валентности IV (ClO2) и VI (Cl2O6).
Содержание:
Хлор — химический элемент и простое вещество:
Химические элементы с наиболее ярко выраженными неметаллическими свойствами в периодической системе составляют VIIА-группу: фтор F, хлор Cl, бром Br, иод I и очень редко встречающийся в природе астат At. Эти элементы называются галогенами.
Хлор в природе
Наиболее распространенным в природе галогеном является хлор. Его массовая доля в земной коре составляет около 0,2 % — 11-е место по распространенности среди всех элементов. Широко распространены минералы и горные породы, содержащие хлориды, — соли соляной кислоты: галит (каменная или поваренная соль) NaCl, сильвин KCl, карналлит
Хлор — один из химических элементов, без которых немыслимо существование живых организмов. Ионы хлора вместе с ионами натрия и калия регулируют водно-солевой обмен в организме человека. Хлор участвует в энергетическом обмене у растений, положительно влияет на поглощение корнями кислорода, а также соединений калия, кальция, магния.
Химический элемент хлор
Охарактеризуем хлор по плану, который вы применяли в 8-м классе.
Химический знак — Cl, относительная атомная масса — 35,5, атомный номер — 17. Этот элемент находится в третьем периоде в VIIА-группе.
Заряд ядра атома хлора равен 17+, следовательно, ядро содержит 17 протонов, а ядра двух его природных нуклидов 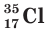
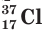
В атоме хлора 17 электронов, которые располагаются на трех электронных слоях: 17Cl 2e– , 8e– , 7e– .
На внешнем (незавершенном) электронном слое у атомов хлора находится по 7 электронов, следовательно, этот элемент относится к неметаллам. Максимальная положительная степень окисления хлора равна +7, формула его высшего оксида — 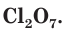
Степень окисления хлора в летучем водородном соединении равна –1, формула этого соединения — HCl.
Простое вещество
Хлор является веществом молекулярного строения. Его молекула состоит из двух атомов — 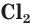
При обычных условиях хлор — желто-зеленый газ с резким запахом. Он в 2,5 раза тяжелее воздуха, ядовит. В Первую мировую войну хлор использовался даже в качестве боевого отравляющего вещества.
Растворимость хлора в воде небольшая: в одном объеме воды при 20 °С растворяется 2,5 объема хлора. Водный раствор хлора называется хлорной водой.
Химические свойства
Хлор является химически активным простым веществом. Он взаимодействует практически со всеми простыми веществами, за исключением кислорода, азота и благородных газов, образуя хлориды. С металлами хлор реагирует при слабом нагревании, а с некоторыми даже при обычных условиях, выступая в качестве окислителя:
Как окислитель хлор реагирует с менее электроотрицательными неметаллами:
Хлор своеобразно реагирует с водородом. При обычной температуре в темноте реакция не происходит, но при сильном освещении или при нагревании смесь хлора и водорода может взорваться.
С большинством сложных веществ хлор также ведет себя как окислитель. Взаимодействуя с растворами бромидов и иодидов металлов, хлор вытесняет из них бром и иод:
Приведенные выше реакции подтверждают, что простое вещество хлор проявляет более сильные окислительные свойства, чем нижестоящие в группе галогены.
Применение хлора
По масштабам промышленного применения хлор намного превосходит все остальные галогены (рис. 36). В больших количествах хлор используется для обеззараживания питьевой воды. Хлор и его соединения применяются для отбеливания льняных и хлопчатобумажных тканей, бумаги, древесины и т. д. Особенно много его расходуется при производстве пластмасс, каучуков, красителей, различных растворителей. Огромны масштабы использования хлора в производстве соляной кислоты.
Хлор является самым распространенным галогеном.
Минимальная отрицательная степень окисления хлора равна –1, максимальная положительная — +7.
При обычных условиях простое вещество хлор — желто-зеленый газ с резким запахом, тяжелее воздух, ядовит.
Хлор взаимодействует непосредственно практически со всеми простыми веществами, за исключением кислорода, азота и благородных газов, а также со многими сложными веществами, выступая обычно в качестве окислителя.
Хлороводород и соляная кислота
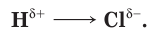
Одним из важнейших соединений хлора является продукт его взаимодействия с водородом — хлороводород HCl. Это бесцветный газ с резким запахом, несколько тяжелее воздуха. Химическая связь в молекуле HCl — ковалентная полярная:
Молекула хлороводорода HCl полярна и представляет собой диполь.
Хлороводород очень хорошо растворяется в воде. Это легко проверить, если цилиндр, заполненный этим газом, опустить в чашку с водой (куда заранее было внесено несколько капель лакмуса). Вода быстро поднимется вверх, при этом раствор окрасится в красный цвет, что является свидетельством образования в цилиндре кислого раствора (рис. 37).
Соляная кислота
Раствор хлороводорода в воде — хлороводородная кислота, которую на практике чаще называют соляной кислотой. Это бесцветная жидкость с резким запахом. В концентрированной кислоте массовая доля HCl составляет около 37 %.
Соляная кислота является сильной одноосновной кислотой, в разбавленном растворе полностью диссоциирует на ионы:
Соляная кислота проявляет характерные для кислот свойства. Она изменяет окраску индикаторов: лакмус и метилоранж в растворе HCl становятся красными. Соляная кислота взаимодействует с теми металлами, которые в ряду активности металлов расположены до водорода:
В этих реакциях ионы водорода выступают в качестве окислителя. Соляная кислота взаимодействует с основными оксидами:
со щелочами и нерастворимыми основаниями:
а также с солями:
Реакции с солями идут только тогда, когда образуются осадок, газ или слабый электролит.
В организме человека соляная кислота вырабатывается клетками слизистой оболочки желудка и входит в состав желудочного сока. Массовая доля HCl в желудочном соке человека равна 0,3 % — 0,5 %. Соляная кислота в составе желудочного сока улучшает пищеварение, уничтожает большинство бактерий, которые попадают с пищей в желудок, что замедляет или даже останавливает гнилостный процесс. Желудок здорового человека вырабатывает до 2,5 дм3 желудочного сока в сутки. Желудочный сок начинает выделяться уже тогда, когда вы начинаете пережевывать пищу. Поэтому жевать жевательную резинку на голодный желудок вредно: в отсутствии пищи соляная кислота разрушительно действует на стенки желудка.
Продуктом взаимодействия хлора с водородом является хлороводород — бесцветный газ с резким запахом, тяжелее воздуха.
Раствор хлороводорода в воде представляет собой кислоту, которая называется хлороводородной или соляной.
Соляная кислота проявляет все типичные свойства кислот: взаимодействует с основаниями, основными оксидами, солями и металлами, стоящими в ряду активности до водорода.
Хлориды
Соли соляной кислоты называются хлоридами. Большинство хлоридов растворимы в воде. Так, например, большая часть растворенных в морской воде солей приходится на хлорид натрия. Объясняется это тем, что соли вымываются из горных пород и выносятся реками в моря и океаны. Но в засушливых и пустынных районах в результате интенсивного испарения воды концентрация солей в воде сильно повышается, и они выделяются в твердом виде. Так образуются солончаки (рис. 38).
Растворы хлоридов — обязательная составная часть живых организмов. В теле взрослого человека содержится примерно 200 г хлорида натрия, причем, около 45 г растворено в крови. Соль поддерживает нормальную деятельность клеток, из которых состоят все ткани и органы. Взрослому человеку необходимо получать в день примерно 5—6 г хлорида натрия, включая и ту соль, которая входит в состав готовых продуктов. Употребление избыточного количества поваренной соли приводит к ухудшению самочувствия: появлению головной боли, отекам, повышению артериального давления.
К практически нерастворимым хлоридам относится хлорид серебра(I) AgCl. Это свойство хлорида серебра(I) используется для обнаружения хлорид ионов в растворе. При добавлении к соляной кислоте или к раствору хлорида натрия раствора нитрата серебра(I) 
Такая реакция является качественной реакцией на ионы хлора, а нитрат серебра(I) служит реактивом на соляную кислоту и ее соли.
Если содержание хлорид-ионов в растворе невелико, то осадок не выпадает, а наблюдается помутнение раствора. Этой реакцией можно пользоваться для проверки наличия хлоридионов в питьевой воде.
Применение соляной кислоты и хлоридов
Соляная кислота и ее соли относятся к тем веществам, которые постоянно сопровождают человека, являясь неотъемлемой частью его жизни. В больших объемах соляная кислота расходуется в самых разнообразных областях практической деятельности человека: в химической, пищевой
и фармацевтической промышленности, для обработки поверхности металлов и др. Как реагент соляная кислота используется во всех химических лабораториях (рис. 40).
Важнейшими солями соляной кислоты являются хлориды натрия и калия. Поваренная соль NaCl известна как пищевая добавка, которая служит консервантом при подготовке пищевых продуктов к длительному хранению.
Поваренная (каменная) соль издавна ценилась очень высоко. Ею вместо денег платили жалованье римским воинам и крестоносцам. В Китае изготавливали соляные монеты, на которых ставилось клеймо правителя. А в Эфиопии еще в XIX в. были в ходу соляные деньги — стандартные бруски каменной соли (см. рис.).
Хлорид натрия используют для профилактики и лечения простудных заболеваний. Посещение соляных пещер, воздух в которых чрезвычайно богат аэрозолем хлорида натрия, оказывает положительное влияние на состояние дыхательных путей и кожи детей и взрослых (рис. 41). Водный раствор хлорида натрия широко применяется в медицине для приготовления различных лекарственных препаратов.
Хлориды натрия и кальция используют для борьбы с гололедицей, а NaCl — в производстве химических препаратов, стекла и бумаги.
Хлорид калия KCl — ценное минеральное удобрение. Это основной экспортный продукт химической промышленности Беларуси (рис. 42). Хлориды других металлов используются в сельском хозяйстве, химической промышленности, медицине.
- Соли соляной кислоты называются хлоридами.
- Реактивом на соляную кислоту и ее соли служит раствор нитрата серебра(I).
- Соляная кислота и хлориды имеют важное значение для жизнедеятельности живых организмов.
ХЛОР, химический элемент VII группы периодической системы, относится к галогенам. Атомный номер 17, относительная атомная масса 35,453. Природный хлор состоит из смеси двух изотопов – хлора-35 (75,77%) и хлора-37 (24,23%).
История получения.
Хлор, вероятно, получали еще алхимики, но его открытие и первое исследование неразрывно связано с именем знаменитого шведского химика Карла Вильгельма Шееле. Шееле открыл пять химических элементов – барий и марганец (совместно с Юханом Ганом), молибден, вольфрам, хлор, а независимо от других химиков (хотя и позже) – еще три: кислород, водород и азот. Это достижение впоследствии не смог повторить ни один химик. При этом Шееле, уже избранный членом Шведской королевской академии наук, был простым аптекарем в Чёпинге, хотя мог занять более почетную и престижную должность. Сам Фридрих II Великий, прусский король, предлагал ему занять пост профессора химии Берлинского университета. Отказываясь от подобных заманчивых предложений, Шееле говорил: «Я не могу есть больше, чем мне нужно, а того, что я зарабатываю здесь в Чёпинге, мне хватает на пропитание».
Многочисленные соединения хлора были известны, конечно, задолго до Шееле. Этот элемент входит в состав многих солей, в том числе и самой известной – поваренной соли. В 1774 Шееле выделил хлор в свободном виде, нагревая черный минерал пиролюзит с концентрированной соляной кислотой: MnO2 + 4HCl ® Cl2 + MnCl2 + 2H2O.
Вначале химики рассматривали хлор не как элемент, а как химическое соединение неизвестного элемента мурия (от латинского muria – рассол) с кислородом. Считалось, что и соляная кислота (ее называли муриевой) содержит химически связанный кислород. Об этом «свидетельствовал», в частности, такой факт: при стоянии раствора хлора на свету из него выделялся кислород, а в растворе оставалась соляная кислота. Однако многочисленные попытки «оторвать» кислород от хлора ни к чему не привели. Так, никому не удалось получить углекислый газ, нагревая хлор с углем (который при высоких температурах «отнимает» кислород от многих содержащих его соединений). В результате подобных опытов, проведенных Гемфри Дэви, Жозеф Луи Гей-Люссаком и Луи Жаком Тенаром, стало ясно, что хлор не содержит кислорода и является простым веществом. К тому же выводу привели и опыты Гей-Люссака, который проанализировал количественное соотношение газов в реакции хлора с водородом.
В 1811 Дэви предложил для нового элемента название «хлорин» – от греч. «хлорос» – желто-зеленый. Именно такой цвет имеет хлор. Этот же корень – в слове «хлорофилл» (от греч. «хлорос» и «филлон» – лист). Спустя год Гей-Люссак «сократил» название до «хлора». Но до сих пор англичане (и американцы) называют этот элемент «хлорином» (chlorine), тогда как французы – хлором (chlore). Приняли сокращенное название и немцы – «законодатели» химии на протяжении почти всего 19 в. (по-немецки хлор – Chlor). В 1811 немецкий физик Иоганн Швейгер предложил для хлора название «галоген» (от греческих «халс» – соль, и «геннао» – рождаю). Впоследствии этот термин закрепился не только за хлором, но и за всеми его аналогами по седьмой группе – фтором, бромом, иодом, астатом.
В 1826 шведский химик Йёнс Якоб Берцелиус, уточнив полученные им же ранее данные, определил для хлора атомную массу 35,41, которая отличается от современной лишь на 0,1%! Это поразительный результат, если учесть качество оборудования, с которым работал знаменитый химик. Основной инструмент для определения атомных масс – весы. Когда-то каждый экземпляр точных аналитических весов изготовлялся мастером вручную, и стоили хорошие весы очень дорого. Поэтому лишь немногие очень богатые химики могли похвастаться такими весами. Сам Берцелиус имел в молодые годы плохо оборудованную лабораторию с довольно грубыми весами, поэтому для получения надежных результатов он был вынужден повторять один и тот же анализ по 20–30 раз! В течение 10 лет Берцелиус опубликовал результаты анализа 2000 соединений, образованных 43 элементами, и труд, затраченный им на эту колоссальную работу, превосходит всякое воображение. Спустя почти столетие другой знаменитый химик, один из первых лауреатов Нобелевской премии по химии Вильгельм Оствальд, увидев в музее оборудование, с которым работал Берцелиус, сказал: «Мне стало совершенно ясно, как мало зависит от прибора и как много от человека, который перед ним сидит».
Хлор в природе.
Хлора в земное коре не очень много – всего 0,017%, причем в свободном состоянии он встречается лишь в небольших количествах в вулканических газах. В списке самых распространенных элементов хлор находится в конце второго десятка. Хлора меньше, чем даже ванадия и циркония (но больше, чем хрома, никеля, цинка, меди и азота). При этом хлор очень сильно распылен: небольшие количества этого элемента входят в состав множества различных минералов и горных пород. Очень высокая химическая активность хлора приводит к тому, что в природе он встречается, как правило, в виде соединений, в сочетании с натрием, калием, магнием, кальцием.
Хлор образует около ста минералов; главным образом это хлориды легких металлов – щелочных и щелочноземельных. Самый распространенный среди них – галит NaCl. Реже встречаются хлориды калия, кальция, магния. Из них наиболее распространены бишофит MgCl2·6H2O, карналлит KCl·MgCl2·6H2O, сильвин KCl, сильвинит NaCl·KCl, каинит KCl·MgSO4·3H2O, тахигидрит CaCl2·2MgCl2·12H2O. В виде таких соединений хлор содержится в соляных пластах, образовавшихся при высыхании древних морей. Особенно мощные залежи образует галит и калийные соли; их запасы оцениваются гигантским числом – более 10 триллионов тонн!
Очень много хлора содержится в морской воде – в среднем 1,9%. Происходит это потому, что хлор вымываемый из пород, нигде не может задержаться (почти все хлориды металлов растворимы) и выносится реками в моря и океаны. Но не следует думать, что попавший в морскую воду хлор уже не может вернуться на материки. В обратной миграции хлора большую роль играет ветер, уносящий соленую пыль с поверхности океанов, морей и соленых озер. Так хлор участвует в круговороте веществ. Но в засушливых и пустынных районах в результате интенсивного испарения воды концентрация хлора в грунтовых водах сильно повышается. Так образуются солончаки, особенно в низинах. Из различных источников ежегодно в мире добывают сотни миллионов тонн хлора.
Растворы хлоридов – обязательная составная часть живых организмов. Содержание хлора в теле человека 0,25%, в плазме крови – 0,35%. В теле взрослого человека содержится более 200 г хлорида натрия, из которых 45 г растворено в крови. В продуктах питания и природной воде часто недостаточно хлора для нормального развития человека, поэтому с древних времен люди подсаливают пищу. Вводят хлор и в подкормку животных. Растения же, в отличие от животных, никогда не испытывают дефицита хлора.
Получение хлора.
Метод Шееле в настоящее время используют редко – разве только во время лекционных демонстраций. В лабораториях для получения хлора используют более сильный окислитель – перманганат калия, который окисляет соляную кислоту уже при комнатной температуре: 2KMnO4 + 16HCl ® 2KCl + 2MnCl2 + 8H2O + 5Cl2. Этот способ был предложен немецким химиком Карлом Гребе. Аналогично идет реакция и с дихроматом калия:
K2Cr2O7 + 14HCl ® 2KCl + 2CrCl3 + 3Cl2 + 7H2O. Хлор выделяется также при действии соляной кислоты на хлорную известь: Ca(OCl)Cl + 2HCl ® CaCl2 + Cl2 + H2O. Можно окислить соляную кислоту до свободного хлора и концентрированным раствором пероксида водорода – пергидролем (реакция лучше идет на ярком свету). В 1867 английский технолог Генри Дикон разработал непрерывный способ получения хлора путем каталитического окисления хлороводорода кислородом воздуха над медным катализатором (диконовский процесс): 4HCl + O2® 2Cl2 + 2H2O. Сейчас этот метод имеет лишь историческое значение.
После того, как Алессандро Вольта создал в 1799 первый химический источник постоянного тока (вольтов столб), многие ученые начали изучать действие этого источника на различные вещества. Оказалось, что при пропускании тока через раствор поваренной соли можно получить хлор и гидроксид натрия. Однако промышленное значение этот метод приобрел только после 1872, когда для производства дешевой электроэнергии начали использовать изобретенные бельгийским мастером З.Т.Граммом динамо-машины. В настоящее время практически весь хлор получают электролизом водных растворов хлорида натрия: 2NaCl + 2H2O ® Cl2 + 2NaOH + H2. При этом хлор выделяется на аноде, тогда как на катоде также образуются ценные вещества – водород и гидроксид натрия. Путем повышения давления хлор сжижают и заливают в стальные баллоны, где он хранится под давлением около 6 атм. Чтобы выделяющийся при электролизе хлор не разрушал аноды, их делают из титановых сплавов и покрывают оксидами титана и рутения. Производство это энергоемкое – на тонну хлора расходуется в среднем 3000 кВт-ч электроэнергии. В развитых странах на производство хлора затрачивается около 2% всей вырабатываемой электроэнергии! Но одновременно получают и другие ценные продукты – едкий натр и водород. Получают свободный хлор в огромных количествах. Так, к началу 21 в. только в США его ежегодно производили в количестве более 11 млн. тонн!
Свойства хлора.
Хлор – тяжелый (в 2,5 раза тяжелее воздуха) желто-зеленый газ. Молекулы Cl2 легко диссоциируют на атомы при поглощении кванта света, а также при высокой температуре. При 730° С степень диссоциации составляет около 0,02%, а при 1730° С – уже почти 35%. При невысоких давлениях хлор близок к идеальным газам: 1 моль хлора при нормальных условиях занимает объем 22,06 л. При охлаждении до –34° С хлор сжижается, а при –101° С он затвердевает. Температуру сжижения газообразного хлора легко повысить, если увеличить давление; так при давлении 5 атм хлор кипит уже при +10,3° С.
Хлор неплохо растворяется в воде: при 10° С в 1 л воды растворяется 3,15 л хлора, при 20° С – 2,3 л. Образующийся раствор обычно называют хлорной водой. Если насытить хлором при атмосферном давлении холодную (ниже 9,6° С) воду, из раствора выделяются желтоватые кристаллы состава Cl2·6H2O. Такие же кристаллы гидрата хлора образуются при охлаждении влажного газообразного хлора. Нагревая гидрат хлора в одном колене запаянной изогнутой трубки и охлаждая второе колено льдом, Фарадей в 1823 получил жидкий хлор. Хлор хорошо растворяется во многих органических растворителях; так, в 100 г холодного бензола растворяется около 35 г хлора.
Химически хлор очень активен. Он реагирует почти со всеми веществами, даже с платиной (при температурах выше 560° С). А в хлорной воде растворяется и золото. В 1869 профессор химии в Эдинбурге Джемс Альфред Уанклин заметил, что хорошо высушенный хлор не действует на железо и некоторые другие металлы. В результате появилось возможность хранить безводный жидкий хлор в стальных баллонах. Промышленное производство жидкого хлора было налажено в 1888 немецкой фирмой БАСФ.
Высокую химическую активность хлора используют для демонстрации эффектных лекционных опытов. Так, при высыпании в колбу с хлором тонкого порошка металлической сурьмы он вспыхивает на лету красивыми белыми искорками, одновременно образуется белый дым SbCl3. Если в сосуд с хлором внести тонкую оловянную фольгу, она также самовоспламеняется, а на дно падает «огненный дождь»; в этой реакции образуются капли тяжелой дымящейся жидкости – SnCl4. Нагретые железные стружки горят в хлоре красноватым пламенем с образованием рыжего дыма FeCl3. Красный фосфор, внесенный в хлор, горит слабым зеленоватым пламенем. Очень энергично реагирует с хлор с рядом органических соединений. Так, если в цилиндр с хлором бросить комок ваты, смоченной скипидаром, он сразу же загорается, а из цилиндра вырывается пламя и облако сажи. Эффектно горит желтым пламенем в хлоре натрий, образуя на стенках сосуда белый налет соли. Этот опыт в молодости провел будущий академик, лауреат Нобелевской премии по химии Н.Н.Семенов. Собрав со стенок сосуда белый налет, он посыпал им кусок черного хлеба и смело съел; химия не подвела: из ядовитого газа и щелочного металла действительно получилась поваренная соль!
Хлор активно и с выделением значительного количества тепла реагирует с водородом:
Cl2 + H2® 2HCl + 184 кДж. Реакция идет по цепному механизму, и если скорость ее инициирования велика (сильное освещение ультрафиолетовым или сине-фиолетовым светом, нагрев до высокой температуры), смесь газов (если хлора в ней содержится более 11,5 и менее 95%) взрывается (см. также ЦЕПНЫЕ РЕАКЦИИ).
Интересна демонстрация горения водорода в атмосфере хлора: иногда во время опыта возникает необычный побочный эффект: раздается гудение. Чаще всего пламя гудит, когда тонкую трубку, по которой подается водород, опускают в заполненный хлором сосуд конической формы; то же справедливо для сферических колб, а вот в цилиндрах пламя обычно не гудит. Это явление назвали «поющим пламенем».
В водном растворе хлор частично и довольно медленно реагирует с водой; при 25° С равновесие: Cl2 + H2O HClO + HCl устанавливается в течение двух суток. Хлорноватистая кислота на свету разлагается: HClO ® HCl + O. Именно атомарному кислороду приписывают отбеливающий эффект (абсолютно сухой хлор такой способностью не обладает).
Хлор в своих соединениях может проявлять все степени окисления – от –1 до +7. С кислородом хлор образует ряд оксидов, все они в чистом виде нестабильны и взрывоопасны: Cl2O – желто-оранжевый газ, ClO2 – желтый газ (ниже 9,7о С – яркокрасная жидкость), перхлорат хлора Cl2O4 (ClO–ClO3, светло-желтая жидкость), Cl2O6 (O2Cl–O–ClO3, ярко-красная жидкость), Cl2O7 – бесцветная очень взрывчатая жидкость. При низких температурах получены нестабильные оксиды Cl2O3 и ClO3. Оксид ClO2 производится в промышленном масштабе и используется вместо хлора для отбеливания целлюлозы и обеззараживания питьевой воды и сточных вод. С другими галогенами хлор образует ряд так называемых межгалогенных соединений, например, ClF, ClF3, ClF5, BrCl, ICl, ICl3.
Хлор и его соединения с положительной степенью окисления – сильные окислители. В 1822 немецкий химик Леопольд Гмелин путем окисления хлором получил из желтой кровяной соли красную: 2K4[Fe(CN)6] + Cl2® K3[Fe(CN)6] + 2KCl. Хлор легко окисляет бромиды и хлориды с выделением в свободном виде брома и иода.
Хлор в разных степенях окисления образует ряд кислот: HCl – хлороводородная (соляная, соли – хлориды), HClO – хлорноватистая (соли – гипохлориты), HClO2 – хлористая (соли – хлориты), HClO3 – хлорноватая (соли – хлораты), HClO4 – хлорная (соли – перхлораты). В чистом виде из кислородных кислот устойчива только хлорная. Из солей кислородных кислот практическое применение имеют гипохлориты, хлорит натрия NaClO2 – для отбеливания тканей, для изготовления компактных пиротехнических источников кислорода («кислородные свечи»), хлораты калия (бертолетова соль), кальция и магния (для борьбы с вредителями сельского хозяйства, как компоненты пиротехнических составов и взрывчатых веществ, в производстве спичек), перхлораты – компоненты взрывчатых веществ и пиротехнических составов; перхлорат аммония – компонент твердых ракетных топлив.
Хлор реагирует со многими органическими соединениями. Он быстро присоединяется к непредельным соединениям с двойными и тройными углерод-углеродными связями (реакция с ацетиленом идет со взрывом), а на свету – и к бензолу. При определенных условиях хлор может замещать атомы водорода в органических соединениях: R–H + Cl2® RCl + HCl. Эта реакция сыграла значительную роль в истории органической химии. В 1840-х французский химик Жан Батист Дюма обнаружил, что при действии хлора на уксусную кислоту с удивительной легкостью идет реакция
СН3СООН + Cl2® CH2ClCOOH + HCl. При избытке хлора образуется трихлоруксусная кислота ССl3СООН. Однако многие химики отнеслись к работе Дюма недоверчиво. Ведь согласно общепринятой тогда теории Берцелиуса положительно заряженные атомы водорода не могли заместиться отрицательно заряженными атомами хлора. Этого мнения придерживались в то время многие выдающиеся химики, среди которых были Фридрих Вёлер, Юстус Либих и, конечно, сам Берцелиус.
Чтобы высмеять Дюма, Вёлер передал своему другу Либиху статью от имени некоего Ш.Виндлера (Schwindler – по-немецки мошенник) о новом удачном приложении якобы открытой Дюма реакции. В статье Вёлер с явной издёвкой написал о том, как в уксуснокислом марганце Mn(CH3COO)2 удалось все элементы, в соответствии с их валентностью, заместить на хлор, в результате чего получилось желтое кристаллическое вещество, состоящее из одного только хлора. Далее говорилось, что в Англии, последовательно замещая в органических соединениях все атомы на атомы хлора, обычные ткани превращают в хлорные, и что при этом вещи сохраняют свой внешний вид. В сноске было указано, что лондонские лавки бойко торгуют материалом, состоящим из одного хлора, так как этот материал очень хорош для ночных колпаков и теплых подштанников.
Либиху шутка понравилась, и он опубликовал ее (на французском языке) от имени Ш.Виндлера всего через несколько страниц после статьи Дюма. Намек получился очень прозрачным. Тем не менее прав оказался все же Дюма.
Реакция хлора с органическими соединениями приводит к образованию множества хлорорганических продуктов, среди которых – широко применяющиеся растворители метиленхлорид CH2Cl2, хлороформ CHCl3, четыреххлористый углерод CCl4, трихлорэтилен CHCl=CCl2, тетрахлорэтилен C2Cl4. В присутствии влаги хлор обесцвечивает зеленые листья растений, многие красители. Этим пользовались еще в XVIII в. для отбеливания тканей.
Хлор как отравляющий газ.
Получивший хлор Шееле отметил его очень неприятный резкий запах, затруднение дыхания и кашель. Как потом выяснили, человек чувствует запах хлора даже в том случае, если в одном литре воздуха содержится лишь 0,005 мг этого газа, и при этом он уже оказывает раздражающее действие на дыхательные пути, разрушая клетки слизистой оболочки дыхательных путей и легких. Концентрация 0,012 мг/л переносится с трудом; если же концентрация хлора превышает 0,1 мг/л, он становится опасным для жизни: дыхание учащается, становится судорожным, а затем – все более редким, и уже через 5–25 минут происходит остановка дыхания. Предельно допустимой в воздухе промышленных предприятий считается концентрация 0,001 мг/л, а в воздухе жилых районов – 0,00003 мг/л.
Петербургский академик Товий Егорович Ловиц, повторяя в 1790 опыт Шееле, случайно выпустил значительное количество хлора в воздух. Вдохнув его, он потерял сознание и упал, потом в течение восьми дней страдал от мучительной боли в груди. К счастью, он выздоровел. Чуть не умер, отравившись хлором, и знаменитый английский химик Дэви. Опыты даже с небольшим количеством хлора опасны, так как могут вызвать сильное поражение легких. Рассказывают, что немецкий химик Эгон Виберг одну из своих лекций о хлоре начал словами: «Хлор – ядовитый газ. Если я отравлюсь во время очередной демонстрации, вынесите меня, пожалуйста, на свежий воздух. Но лекцию при этом придется, к сожалению, прервать». Если же выпустить в воздух много хлора, он становится настоящим бедствием. Это испытали на себе во время Первой мировой войны англо-французские войска. Утром 22 апреля 1915 германское командование решило провести первую в истории войн газовую атаку: когда ветер подул в сторону противника, на небольшом шестикилометровом участке фронта в районе бельгийского городка Ипр были одновременно открыты вентили 5730 баллонов, каждый из которых содержал 30 кг жидкого хлора. В течение 5 минут образовалось огромное желто-зеленое облако, которое медленно уходило от немецких окопов в сторону союзников. Английские и французские солдаты оказались полностью беззащитными. Газ проникал через щели во все укрытия, от него не было спасения: ведь противогаз еще не был изобретен. В результате было отравлено 15 тысяч человек, из них 5 тысяч – насмерть. Через месяц, 31 мая немцы повторили газовую атаку на восточном фронте – против русских войск. Это произошло в Польше у города Болимова. На фронте 12 км из 12 тысяч баллонов было выпущено 264 тонны смеси хлора со значительно более ядовитым фосгеном (хлорангидридом угольной кислоты COCl2). Царское командование знало о том, что произошло при Ипре, и тем не менее русские солдаты не имели никаких средств защиты! В результате газовой атаки потери составили 9146 человек, из них только 108 – в результате ружейного и артиллерийского обстрела, остальные были отравлены. При этом почти сразу же погибло 1183 человека.
Вскоре химики указали, как спасаться от хлора: надо дышать через марлевую повязку, пропитанную раствором тиосульфата натрия (это вещество применяется в фотографии, его часто называют гипосульфитом). Хлор очень быстро реагирует с раствором тиосульфата, окисляя его:
Na2S2O3 + 4Cl2 + 5H2O ® 2H2SO4 + 2NaCl + 6HCl. Конечно, серная кислота тоже не безвредное вещество, но ее разбавленный водный раствор намного менее опасен, чем ядовитый хлор. Поэтому у тиосульфата в те годы появилось еще одно название – «антихлор», но первые тиосульфатные противогазы были мало эффективны.
В 1916 русский химик, будущий академик Николай Дмитриевич Зелинский изобрел действительно эффективный противогаз, в котором ядовитые вещества задерживали слоем активированного угля. Такой уголь с очень развитой поверхностью мог задержать значительно больше хлора, чем пропитанная гипосульфитом марля. К счастью, «хлорные атаки» остались лишь трагическим эпизодом в истории. После мировой войны у хлора остались только мирные профессии. См. также ХИМИЧЕСКОЕ И БИОЛОГИЧЕСКОЕ ОРУЖИЕ.
Применение хлора.
Ежегодно во всем мире получают огромные количества хлора – десятки миллионов тонн. Только в США к концу 20 в. ежегодно путем электролиза получали около 12 млн. тонн хлора (10-е место среди химических производств). Основная его масса (до 50%) расходуется на хлорирование органических соединений – для получения растворителей, синтетического каучука, поливинилхлорида и других пластмасс, хлоропренового каучука, пестицидов, лекарственных средств, многих других нужных и полезных продуктов. Остальное потребляется для синтеза неорганических хлоридов, в целлюлозно-бумажной промышленности для отбеливания древесной пульпы, для очистки воды. В сравнительно небольших количествах хлор используют в металлургической промышленности. С его помощью получают очень чистые металлы – титан, олово, тантал, ниобий. Сжиганием водорода в хлоре получают хлороводород, а из него – соляную кислоту. Хлор применяют также для производства отбеливающих веществ (гипохлоритов, хлорной извести) и обеззараживания воды хлорированием.
Илья Леенсон