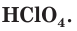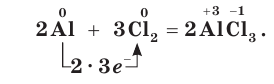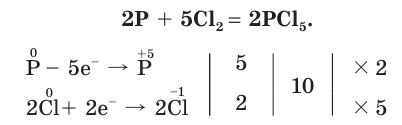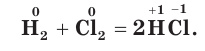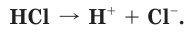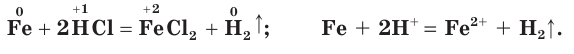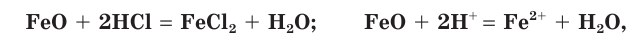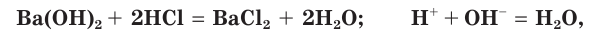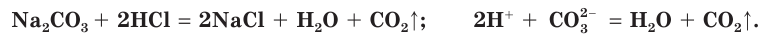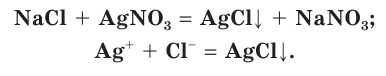Хлористый водород — что это такое? Хлороводород — это бесцветный газ, обладающий резким запахом. Он легко растворяется в воде, образуя соляную кислоту. Химическая формула хлористого водорода — HCl. Он состоит из атома водорода и хлора, соединенных ковалентной полярной связью. Хлороводород легко диссоциирует в полярных растворителях, что обеспечивает хорошие кислотные свойства данного соединения. Длина связи составляет 127,4 нм.
Физические свойства
Как было сказано выше, в нормальном состоянии хлороводород — это газ. Он несколько тяжелее воздуха, а также обладает гигроскопичностью, т. е. притягивает пары воды прямо из воздуха, образуя при этом густое облака пара. По этой причине говорят, что хлористый водород «дымит» на воздухе. Если охлаждать данный газ, то на отметке -85 °С он сжижается, а к -114 °C становится твердым веществом. При температуре 1500 °С разлагается на простые вещества (исходя из формулы хлористого водорода, на хлор и водород).
Раствор HCl в воде называют соляной кислотой. Она представляет собой бесцветную едкую жидкость. Иногда имеет желтоватый оттенок из-за примесей хлора или железа. Из-за гигроскопичности максимальная концентрация при 20 °С — 37-38 % по массе. От нее же зависят и другие физические свойства: плотность, вязкость, температуры плавления и кипения.
Химические свойства
Сам хлороводород обычно в реакции не вступает. Лишь только при высокой температуре (более 650 °С) он реагирует с сульфидами, карбидами, нитридами и боридами, а также оксидами переходных металлов. В присутствии кислот Льюиса может взаимодействовать с гидридами бора, кремния и германия. А вот ее водный раствор гораздо более химически активен. По своей формуле хлористый водород — это кислота, поэтому он обладает некоторыми свойствами кислот:
- Взаимодействие с металлами (которые стоят в электрохимическом ряду напряжений до водорода):
Fe + 2HCl = FeCl2 + H2
- Взаимодействие с амфотерными и основными оксидами:
BaO + 2HCl = BaCl2 + H2O
- Взаимодействие со щелочами:
NaOH + HCl = NaCl + H2O
Взаимодействие с некоторыми солями:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2
- При взаимодействии с аммиаком образуется соль хлорида аммония:
NH3 + HCl = NH4Cl
Но соляная кислота не взаимодействует со свинцом из-за пассивации. Это обусловлено образованием на поверхности металла слоя хлорида свинца, который нерастворим в воде. Таким образом, этот слой защищает металл от дальнейшего взаимодействия с соляной кислотой.
В органических реакциях она может присоединятся по кратным связям (реакция гидрогалогенирования). Также она может реагировать с белками или аминами, образуя органические соли — хлоргидраты. Искусственные волокна, типа бумаги, при взаимодействии с соляной кислотой разрушаются. В окислительно-восстановительных реакциях с сильными окислителями хлороводород восстанавливается до хлора.
Смесь концентрированной соляной и азотной кислоты (3 к 1 по объему) называют «царской водкой». Она является крайне сильным окислителем. Из-за образования в этой смеси свободного хлора и нитрозила царская водка может растворять даже золото и платину.
Получение
Ранее в промышленности соляную кислоту получали путем взаимодействия хлорида натрия с кислотами, обычно с серной:
2NaCl + H2SO4 = 2HCl + Na2SO4
Но этот способ недостаточно эффективен, а чистота получаемого продукта невысока. Сейчас используется другой способ получения (из простых веществ) хлористого водорода по формуле:
H2 + Cl2 = 2HCl
Для реализации такого способа существуют специальные установки, где оба газа подаются непрерывным потоком на пламя, в котором происходит взаимодействие. Водород подается в небольшом избытке для того, чтобы прореагировал весь хлор и не загрязнял получаемый продукт. Далее хлороводород растворяют в воде и получают соляную кислоту.
В лаборатории возможны более разнообразные способы получения, например гидролиз галогенидов фосфора:
PCl5 + H2O = POCl3 + 2HCl
Получить соляную кислоту можно и путем гидролиза кристаллогидратов некоторых хлоридов металлов при повышенной температуре:
AlCl3·6H2O = Al(OH)3 + 3HCl + 3H2O
Также хлороводород является побочным продуктом реакций хлорирования многих органических соединений.
Применение
Сам хлороводород на практике применения не находит, так как очень быстро впитывает воду из воздуха. Почти весь произведенный хлористый водород идет на производство соляной кислоты.
Применяется в металлургии для очистки поверхности металлов, а также для получения чистых металлов из их руд. Это происходит путем перевода их в хлориды, которые легко восстанавливаются. Так, например, получают титан и цирконий. Широкое применение кислота получила в органическом синтезе (реакции гидрогалогенирования). Также из соляной кислоты иногда получают чистый хлор.
Находит применение и в медицине как лекарство в смеси с пепсином. Его принимают при недостаточной кислотности желудка. Соляная кислота используется в пищевой промышленности в качестве добавки Е507 (регулятор кислотности).
Техника безопасности
При высоких концентрациях соляная кислота — это едкое вещество. Попадая на кожу, она вызывает химические ожоги. Вдыхание газообразного хлороводорода вызывает кашель, удушье, а в тяжелых случаях даже отек легких, который может привести к смерти.
По ГОСТу имеет второй класс опасности. Хлористый водород по стандарту NFPA 704 имеет третью категорию опасности из четырех. Кратковременное воздействие может привести к серьезным временным или умеренным остаточным последствиям.
Первая помощь
При попадании соляной кислоты на кожу рана должна быть обильно промыта водой и слабым раствором щелочи или ее соли (например, содой).
При попадании паров хлороводорода внутрь дыхательных путей пострадавшего необходимо вынести на свежий воздух и сделать ингаляцию кислородом. После этого следует прополоскать горло, промыть глаза и нос 2 % раствором гидрокарбоната натрия. Если соляная кислота попала в глаза, то после этого стоит закапать их раствором новокаина и дикаина с адреналином.
Содержание:
Хлор — химический элемент и простое вещество:
Химические элементы с наиболее ярко выраженными неметаллическими свойствами в периодической системе составляют VIIА-группу: фтор F, хлор Cl, бром Br, иод I и очень редко встречающийся в природе астат At. Эти элементы называются галогенами.
Хлор в природе
Наиболее распространенным в природе галогеном является хлор. Его массовая доля в земной коре составляет около 0,2 % — 11-е место по распространенности среди всех элементов. Широко распространены минералы и горные породы, содержащие хлориды, — соли соляной кислоты: галит (каменная или поваренная соль) NaCl, сильвин KCl, карналлит
Хлор — один из химических элементов, без которых немыслимо существование живых организмов. Ионы хлора вместе с ионами натрия и калия регулируют водно-солевой обмен в организме человека. Хлор участвует в энергетическом обмене у растений, положительно влияет на поглощение корнями кислорода, а также соединений калия, кальция, магния.
Химический элемент хлор
Охарактеризуем хлор по плану, который вы применяли в 8-м классе.
Химический знак — Cl, относительная атомная масса — 35,5, атомный номер — 17. Этот элемент находится в третьем периоде в VIIА-группе.
Заряд ядра атома хлора равен 17+, следовательно, ядро содержит 17 протонов, а ядра двух его природных нуклидов 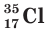
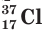
В атоме хлора 17 электронов, которые располагаются на трех электронных слоях: 17Cl 2e– , 8e– , 7e– .
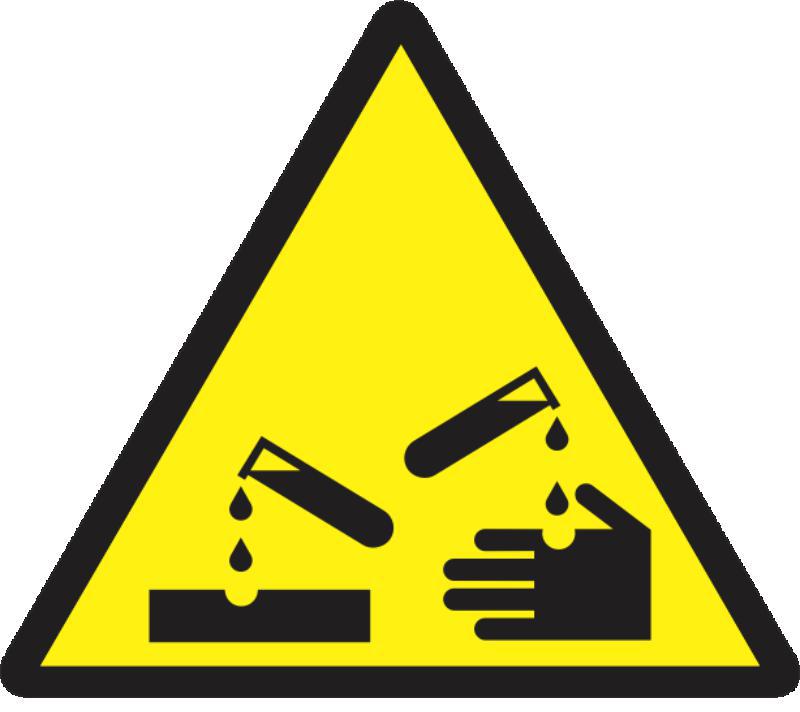
На внешнем (незавершенном) электронном слое у атомов хлора находится по 7 электронов, следовательно, этот элемент относится к неметаллам. Максимальная положительная степень окисления хлора равна +7, формула его высшего оксида — 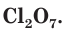
Степень окисления хлора в летучем водородном соединении равна –1, формула этого соединения — HCl.
Простое вещество
Хлор является веществом молекулярного строения. Его молекула состоит из двух атомов — 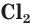
При обычных условиях хлор — желто-зеленый газ с резким запахом. Он в 2,5 раза тяжелее воздуха, ядовит. В Первую мировую войну хлор использовался даже в качестве боевого отравляющего вещества.
Растворимость хлора в воде небольшая: в одном объеме воды при 20 °С растворяется 2,5 объема хлора. Водный раствор хлора называется хлорной водой.
Химические свойства
Хлор является химически активным простым веществом. Он взаимодействует практически со всеми простыми веществами, за исключением кислорода, азота и благородных газов, образуя хлориды. С металлами хлор реагирует при слабом нагревании, а с некоторыми даже при обычных условиях, выступая в качестве окислителя:
Как окислитель хлор реагирует с менее электроотрицательными неметаллами:
Хлор своеобразно реагирует с водородом. При обычной температуре в темноте реакция не происходит, но при сильном освещении или при нагревании смесь хлора и водорода может взорваться.
С большинством сложных веществ хлор также ведет себя как окислитель. Взаимодействуя с растворами бромидов и иодидов металлов, хлор вытесняет из них бром и иод:
Приведенные выше реакции подтверждают, что простое вещество хлор проявляет более сильные окислительные свойства, чем нижестоящие в группе галогены.
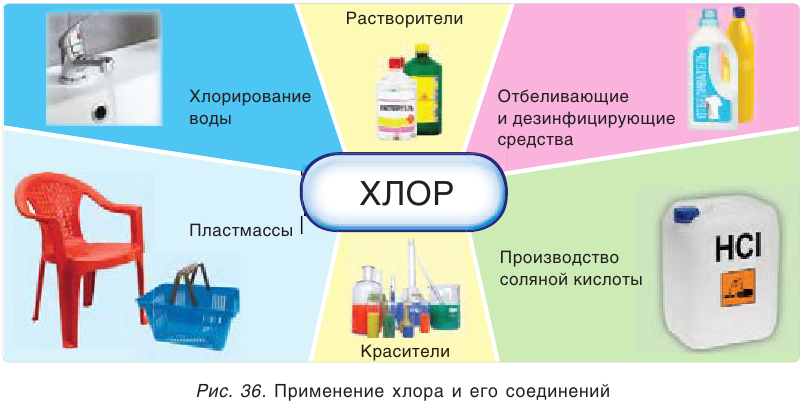
Применение хлора
По масштабам промышленного применения хлор намного превосходит все остальные галогены (рис. 36). В больших количествах хлор используется для обеззараживания питьевой воды. Хлор и его соединения применяются для отбеливания льняных и хлопчатобумажных тканей, бумаги, древесины и т. д. Особенно много его расходуется при производстве пластмасс, каучуков, красителей, различных растворителей. Огромны масштабы использования хлора в производстве соляной кислоты.
Хлор является самым распространенным галогеном.
Минимальная отрицательная степень окисления хлора равна –1, максимальная положительная — +7.
При обычных условиях простое вещество хлор — желто-зеленый газ с резким запахом, тяжелее воздух, ядовит.
Хлор взаимодействует непосредственно практически со всеми простыми веществами, за исключением кислорода, азота и благородных газов, а также со многими сложными веществами, выступая обычно в качестве окислителя.
Хлороводород и соляная кислота
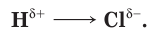
Одним из важнейших соединений хлора является продукт его взаимодействия с водородом — хлороводород HCl. Это бесцветный газ с резким запахом, несколько тяжелее воздуха. Химическая связь в молекуле HCl — ковалентная полярная:
Молекула хлороводорода HCl полярна и представляет собой диполь.
Хлороводород очень хорошо растворяется в воде. Это легко проверить, если цилиндр, заполненный этим газом, опустить в чашку с водой (куда заранее было внесено несколько капель лакмуса). Вода быстро поднимется вверх, при этом раствор окрасится в красный цвет, что является свидетельством образования в цилиндре кислого раствора (рис. 37).
Соляная кислота
Раствор хлороводорода в воде — хлороводородная кислота, которую на практике чаще называют соляной кислотой. Это бесцветная жидкость с резким запахом. В концентрированной кислоте массовая доля HCl составляет около 37 %.
Соляная кислота является сильной одноосновной кислотой, в разбавленном растворе полностью диссоциирует на ионы:
Соляная кислота проявляет характерные для кислот свойства. Она изменяет окраску индикаторов: лакмус и метилоранж в растворе HCl становятся красными. Соляная кислота взаимодействует с теми металлами, которые в ряду активности металлов расположены до водорода:
В этих реакциях ионы водорода выступают в качестве окислителя. Соляная кислота взаимодействует с основными оксидами:
со щелочами и нерастворимыми основаниями:
а также с солями:
Реакции с солями идут только тогда, когда образуются осадок, газ или слабый электролит.
В организме человека соляная кислота вырабатывается клетками слизистой оболочки желудка и входит в состав желудочного сока. Массовая доля HCl в желудочном соке человека равна 0,3 % — 0,5 %. Соляная кислота в составе желудочного сока улучшает пищеварение, уничтожает большинство бактерий, которые попадают с пищей в желудок, что замедляет или даже останавливает гнилостный процесс. Желудок здорового человека вырабатывает до 2,5 дм3 желудочного сока в сутки. Желудочный сок начинает выделяться уже тогда, когда вы начинаете пережевывать пищу. Поэтому жевать жевательную резинку на голодный желудок вредно: в отсутствии пищи соляная кислота разрушительно действует на стенки желудка.
Продуктом взаимодействия хлора с водородом является хлороводород — бесцветный газ с резким запахом, тяжелее воздуха.
Раствор хлороводорода в воде представляет собой кислоту, которая называется хлороводородной или соляной.
Соляная кислота проявляет все типичные свойства кислот: взаимодействует с основаниями, основными оксидами, солями и металлами, стоящими в ряду активности до водорода.
Хлориды
Соли соляной кислоты называются хлоридами. Большинство хлоридов растворимы в воде. Так, например, большая часть растворенных в морской воде солей приходится на хлорид натрия. Объясняется это тем, что соли вымываются из горных пород и выносятся реками в моря и океаны. Но в засушливых и пустынных районах в результате интенсивного испарения воды концентрация солей в воде сильно повышается, и они выделяются в твердом виде. Так образуются солончаки (рис. 38).
Растворы хлоридов — обязательная составная часть живых организмов. В теле взрослого человека содержится примерно 200 г хлорида натрия, причем, около 45 г растворено в крови. Соль поддерживает нормальную деятельность клеток, из которых состоят все ткани и органы. Взрослому человеку необходимо получать в день примерно 5—6 г хлорида натрия, включая и ту соль, которая входит в состав готовых продуктов. Употребление избыточного количества поваренной соли приводит к ухудшению самочувствия: появлению головной боли, отекам, повышению артериального давления.
К практически нерастворимым хлоридам относится хлорид серебра(I) AgCl. Это свойство хлорида серебра(I) используется для обнаружения хлорид ионов в растворе. При добавлении к соляной кислоте или к раствору хлорида натрия раствора нитрата серебра(I) 
Такая реакция является качественной реакцией на ионы хлора, а нитрат серебра(I) служит реактивом на соляную кислоту и ее соли.
Если содержание хлорид-ионов в растворе невелико, то осадок не выпадает, а наблюдается помутнение раствора. Этой реакцией можно пользоваться для проверки наличия хлоридионов в питьевой воде.
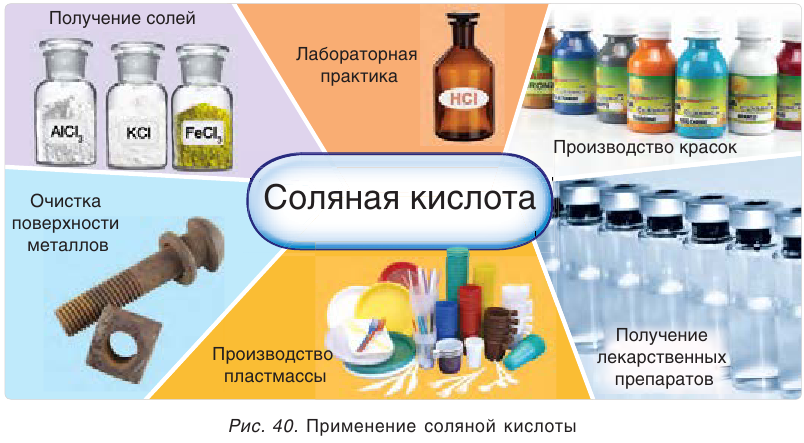
Применение соляной кислоты и хлоридов
Соляная кислота и ее соли относятся к тем веществам, которые постоянно сопровождают человека, являясь неотъемлемой частью его жизни. В больших объемах соляная кислота расходуется в самых разнообразных областях практической деятельности человека: в химической, пищевой
и фармацевтической промышленности, для обработки поверхности металлов и др. Как реагент соляная кислота используется во всех химических лабораториях (рис. 40).
Важнейшими солями соляной кислоты являются хлориды натрия и калия. Поваренная соль NaCl известна как пищевая добавка, которая служит консервантом при подготовке пищевых продуктов к длительному хранению.
Поваренная (каменная) соль издавна ценилась очень высоко. Ею вместо денег платили жалованье римским воинам и крестоносцам. В Китае изготавливали соляные монеты, на которых ставилось клеймо правителя. А в Эфиопии еще в XIX в. были в ходу соляные деньги — стандартные бруски каменной соли (см. рис.).
Хлорид натрия используют для профилактики и лечения простудных заболеваний. Посещение соляных пещер, воздух в которых чрезвычайно богат аэрозолем хлорида натрия, оказывает положительное влияние на состояние дыхательных путей и кожи детей и взрослых (рис. 41). Водный раствор хлорида натрия широко применяется в медицине для приготовления различных лекарственных препаратов.
Хлориды натрия и кальция используют для борьбы с гололедицей, а NaCl — в производстве химических препаратов, стекла и бумаги.
Хлорид калия KCl — ценное минеральное удобрение. Это основной экспортный продукт химической промышленности Беларуси (рис. 42). Хлориды других металлов используются в сельском хозяйстве, химической промышленности, медицине.
- Соли соляной кислоты называются хлоридами.
- Реактивом на соляную кислоту и ее соли служит раствор нитрата серебра(I).
- Соляная кислота и хлориды имеют важное значение для жизнедеятельности живых организмов.
Химическое название
Хлороводородная кислота
Химические свойства
Хлороводородная кислота, хлористый водород или хлористоводородная кислота – раствор НСl в воде. Согласно Википедии, вещество относят у группе неорганических сильных одноосновных к-т. Полное название соединения на латинском: Hydrochloricum acid.
Формула Соляной Кислоты в химии: HCl. В молекуле атомы водорода соединяются с атомами галогена – Cl. Если рассмотреть электронную конфигурацию этих молекул, то можно отметить, что в образовании молекулярных орбиталей соединения принимают участие 1s-орбитали водорода и обе 3s и 3p-орбитали атома Cl. В химической формуле Соляной Кислоты 1s-, 3s- и 3р-атомные орбитали перекрываются и образуют 1 , 2 , 3 -орбитали. При этом 3s-орбиталь не носит связывающий характер. Наблюдается смещение электронной плотности к атому Cl и снижается полярность молекулы, но увеличивается энергия связи молекулярных орбиталей (если рассматривать ее в ряду с другими галогеноводородами).
Физические свойства хлористого водорода. Это прозрачная бесцветная жидкость, обладающая способностью дымиться при соприкосновении с воздухом. Молярная масса химического соединения = 36,6 грамма на моль. При стандартных условиях, при температуре воздуха 20 градусов Цельсия, максимальная концентрация вещества составляет 38% по массе. Плотность концентрированной хлороводородной к-ты в такого рода растворе составляет 1,19 г/см³. В целом же, физические свойства и такие характеристики, как плотность, молярность, вязкость, теплоемкость, температура кипения и pН , сильно зависят от концентрации раствора. Эти величины подробнее рассматриваются в таблице плотностей. Например, плотность Соляной Кислоты 10% = 1,048 кг на литр. При затвердевании вещество образует кристаллогидраты разных составов.
Химические свойства Соляной Кислоты. С чем реагирует Соляная Кислота? Вещество вступает во взаимодействие с металлами, которые стоят в ряду электрохимических потенциалов перед водородом (железо, магний, цинк и другие). При этом образуются соли и выделяется газообразный H. С Соляной Кислотой не реагирует свинец, медь, золото, серебро и другие металлы правее водорода. Вещество вступает в реакцию с оксидами металлов, при этом образуя воду и растворимую соль. Гидроксид натрия под действием к-ты образует хлорид натрия и воду. Реакция нейтрализации характерна для данного соединения.
Разбавленная Соляная Кислота реагирует с солями металлов, которые образованы более слабыми к-ами. Например, пропионовая кислота слабее, чем соляная. Вещество не взаимодействует с более сильными кислотами. Карбонат кальция и карбонат натрия будут образовывать после реакции с HCl хлорид, угарный газ и воду.
Для химического соединения характерны реакции с сильными окислителями, с диоксидом марганца, перманганатом калия: 2KMnO4 + 16HCl = 5Cl2 + 2MnCl2 + 2KCl + 8H2O. Вещество реагирует с аммиаком, при этом образуется густой белый дым, который состоит из очень мелких кристаллов хлорида аммония. Минерал пиролюзит с Соляной Кислотой также вступает в реакцию, так как содержит диоксид марганца: MnO2+4HCl=Cl2+MnO2+2H2O (реакция окисления).
Существует качественная реакция на хлороводородную кислоту и ее соли. При взаимодействии вещества с нитратом серебра выпадает белый осадок хлорида серебра и образуется азотная к-та. Уравнение реакции взаимодействия метиламина с хлористым водородом выглядит следующим образом: HCl + CH3NH2 = (CH3NH3)Cl.
Вещество реагирует со слабым основанием анилином. После растворения анилина в воде к смеси прибавляют Соляную Кислоту. В результате основание растворяется и образует солянокислый анилин (хлорид фениламмония): (С6Н5NH3)Cl. Реакция взаимодействия карбида алюминия с хлористоводородной к-ой: Al4C3+12HCL=3CH4+4AlCl3. Уравнение реакции карбоната калия с к-той выглядит следующим образом: K2CO3 + 2HCl = 2KCl + H2O + CO2.
Получение соляной кислоты
Чтобы получить синтетическую Соляную Кислоту сжигают водород в хлоре, а затем полученный газообразный хлороводород растворяется в воде. Также распространено производство реактива из абгазов, которые образуются в виде побочных продуктов при хлорировании углеводородов (абгазная Соляная Кислота). При производстве данного химического соединения применяют ГОСТ 3118 77 – на реактивы и ГОСТ 857 95 – для технической синтетической хлористоводородной кислоты.
В лабораторных условиях можно применять давний способ, при котором поваренная соль подвергается действию концентрированной серной к-ты. Также средство можно получить с помощью реакции гидролиза хлорида алюминия или магния. Во время реакции могут образоваться оксихлориды переменного состава. Для определения концентрации вещества применяют стандарт титры, которые выпускаются в запаянных ампулах, чтобы в последствии можно было получить стандартный раствор известной концентрации и использовать его для определения качества другого титранта.
У вещества имеется достаточно широкая область применения:
- его используют в гидрометаллургии, при декапировании и травлении;
- при очистке металлов при лужении и пайке;
- в качестве реактива для получения хлорида марганца, цинка, железа и других металлов;
- при изготовлении смесей с ПАВ-ами для очистки металлических и керамических изделий от инфекции и грязи (применяется Кислота Соляная ингибированная);
- в качестве регулятора кислотности E507 в пищевой промышленности, в составе содовой воды;
- в медицине при недостаточной кислотности желудочного сока.
Данное химическое соединение имеет высокий класс опасности – 2 (по ГОСТу 12Л.005). При работе с кислотой требуется спец. защита кожи и глаз. Достаточно едкое вещество при попадании на кожу или в дыхательные пути вызывает химические ожоги. Для ее нейтрализации применяют растворы щелочи, чаще всего – питьевую соду. Пары хлороводорода образуют с молекулами воды в воздухе едкий туман, который раздражает дыхательные пути и глаза. Если вещество вступает в реакцию с хлорной известью, перманганатом калия и прочими окислителями, то образуется токсичный газ — хлор. На территории РФ ограничен оборот Соляной Кислоты с концентрацией более 15%.
Фармакологическое действие
Повышает кислотность желудочного сока.
Фармакодинамика и фармакокинетика
Что такое кислотность желудочного сока? Это характеристика концентрации Соляной Кислоты в желудке. Кислотность выражается в рН. В норме в составе желудочного сока должна вырабатываться кислота и принимать активное участие в процессах пищеварения. Формула хлороводородной кислоты: HCl. Ее продуцируют париетальные клетки, расположенные в фундальных железах, с участием Н+/К+-АТФазы. Эти клетки выстилают дно и тело желудка. Кислотность желудочного сока сама по себе изменчива и зависит от числа париетальых клеток и интенсивности процессов нейтрализации вещества щелочными компонентами желудочного сока. Концентрация продуцируемой к-ты стабильна и равняется 160 ммоль/л. У здорового человека в норме должно вырабатываться не более 7 и не менее 5 ммоль вещества в час.
При недостаточной или избыточной выработке Соляной Кислоты возникают заболевания пищеварительного тракта, ухудшается способность усваивать некоторые витамины и микроэлементы, например, железо. Средство стимулирует выделение желудочного сока, снижает рН. Активирует пепсиноген, переводит его в активный фермент пепсин. Вещество благоприятно воздействует на кислотный рефлекс желудка, замедляет переход не до конца переваренной пищи в кишечник. Замедляются процессы брожения содержимого пищеварительного тракта, исчезает боль, изжога и отрыжка, лучше усваивается железо.
После приема внутрь средство частично метаболизируется слюной и желудочной слизью, содержимым 12-перстной кишки. Несвязанное вещество проникает в 12-перстную кишку, где полностью нейтрализуется ее щелочным содержимым.
Показания к применению
Вещество входит в состав синтетических моющих средств, концентрата для полоскания ротовой полости ухода за контактными линзами. Разбавленная Соляная Кислота назначается при заболеваниях желудка, сопровождающихся пониженной кислотностью, при гипохромной анемии в сочетании с препаратами железа.
Противопоказания
Лекарство нельзя применять при аллергии на синтетическое вещество, при болезнях пищеварительного тракта, ассоциированных с повышенной кислотностью, при остром гастрите.
Побочные действия
Концентрированная Соляная Кислота при попадании на кожу, в глаза и дыхательные пути может вызывать сильные ожоги. В составе различных лек. препаратов используют разбавленное вещество, при длительном применении больших дозировок может возникнуть ацидоз, ухудшение состояния эмали зубов.
Инструкция по применению (Способ и дозировка)
Хлороводородную кислоту применяют в соответствии с инструкцией.
Внутрь лекарство назначают, предварительно растворив в воде. Обычно используют 10-15 капель препарата на пол стакана жидкости. Лекарство принимают во время еды, 2-4 раза в день. Максимальная разовая дозировка составляет 2 мл (около 40 капель). Суточная доза – 6 мл (120 капель).
Передозировка
Случаи передозировки не описаны. При бесконтрольном приеме вещества внутрь в больших количествах возникают язвы и эрозии в пищеварительном тракте. Следует обратиться за помощью к врачу.
Взаимодействие
Вещество часто используют в комбинации с пепсином и прочими лек. препаратами. Химическое соединение в пищеварительном тракте вступает во взаимодействие с основаниями и некоторыми веществами (см. химические свойства).
Особые указания
При лечении препаратами Соляной Кислоты необходимо четко придерживаться рекомендаций в инструкции.
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня:
Для промышленных целей используют Кислоту Соляную ингибированную (22-25%). В медицинских целях применяют раствор: Хлористоводородная кислота разведенная. Также вещество содержится в концентрате для полоскания ротовой полости Паронтал, в растворе для ухода за мягкими контактными линзами Биотру.
Отзывы
В Интернете часто можно встретить вопросы, как сделать Соляную Кислоту в домашних условиях и где взять Соляную Кислоту? Вещество часто приобретают для хим. лабораторий и промышленных целей. Отзывов о применении средства внутрь мало.
- “… С возрастом стала беспокоить проблема с желудком и проблемы с пищеварением. Поставили диагноз – гастрит и атрофия слизистой желудка. Врачи назначили пить ферментные лекарства с Соляной Кислотой. Сейчас я прохожу курс лечения, есть первые улучшения в состоянии”;
- “… Мне назначали это лекарство при пониженной кислотности. Но я решила, что буду лечиться более щадящими методами. Пью настой из перечной мяты, мед, растворенный в воде”.
Цена Соляной кислоты, где купить
Где купить Соляную Кислоту ингибированную? Где можно купить Соляную Кислоту в Москве? Купить в розницу данное вещество для технических целей может быть достаточно сложно. На рынке предлагают приобрести средство по приблизительной цене за литр – 20 рублей, но в больших объемах. Указать стоимость препарата для приема внутрь на данный момент невозможно.
Статья из Википедии, бесплатной энциклопедии.
«HCl» перенаправляется сюда. Для других значений см. HCL .
Эта статья о чистом теле. Для раствора хлористого водорода см. Соляная кислота .
| Хлористый водород | |||||
 | |||||
 | |||||
| Идентификация | |||||
|---|---|---|---|---|---|
| Название ИЮПАК | соляная кислота хлористый водород | ||||
| Н о CAS | 7647-01-0 | ||||
| N о ИК | 100 028 723 | ||||
| N о ЕС | 231-595-7 | ||||
| Появление | газ бесцветный, с резким запахом. | ||||
| Химические свойства | |||||
| Грубая формула | H Cl [изомеры] | ||||
| Молярная масса | 36,461 ± 0,002 г / моль H 2,76%, Cl 97,23%, | ||||
| pKa | -4 | ||||
| Диполярный момент | 1,1086 ± 0,0003 Д | ||||
| Физические свойства | |||||
| Т ° плавления | −114 ° С | ||||
| T ° кипения | при 101,3 кПа : −85 ° C | ||||
| Растворимость | в воде при 20 ° C : 720 г · л -1 | ||||
| Объемная масса | 1.00045 г · л -1 (газ) | ||||
| Давление насыщающего пара | |||||
| Критическая точка | 51,35 ° C , 8,26 МПа | ||||
| Тройная точка | 160 К ( -114 ° C ), 13,8 кПа | ||||
| Скорость звука | 296 м · с -1 ( 0 ° C , 1 атм ) | ||||
| Термохимия | |||||
| S 0 газ, 1 бар | 186,90 Дж · К -1 · моль -1 | ||||
| Δ f H 0 газ | -92,31 кДж · моль -1 | ||||
| Δ vap H ° | 16,15 кДж · моль -1 ( 1 атм , -85 ° C ); 9,08 кДж · моль -1 ( 1 атм , 25 ° C ) | ||||
| C p | 29,14 Дж / моль К ( 25 ° C ) | ||||
| Меры предосторожности | |||||
| SGH | |||||
|
H314, H331, | |||||
| WHMIS | |||||
   А, Д1А, Е, | |||||
| NFPA 704 | |||||
|
2 3 1
| |||||
| Транспорт | |||||
| Согласно главе 2.2.2.2.2, хлористый водород в охлажденном сжиженном виде не разрешен к перевозке в соответствии с ДОПОГ | |||||
| Вдыхание | вывести на свежий воздух, возможно, сердечно-легочная реанимация | ||||
| Кожа | снять грязную одежду, промыть большим количеством воды, показать врачу | ||||
| Глаза | промыть большим количеством воды, держа веки открытыми, показать офтальмологу | ||||
| Проглатывание | не пить, не вызывать рвоту, обратиться к врачу. | ||||
| Экотоксикология | |||||
| Порог запаха | низкое: 0,25 промилле высокое: 10,06 промилле | ||||
| | |||||
| Единицы СИ и СТП, если не указано иное. | |||||
| редактировать | |||||
Хлористый водород , химический символ Н Cl , представляет собой орган , состоящий из хлора и водорода , бесцветный, токсичных и сильно коррозийной . В условиях окружающей среды при температуре и давлении это газ, который образует белые пары при контакте с влажностью . Эти пары состоят из соляной кислоты , ионного раствора хлористого водорода в воде.
Хлористый водород, как и соляная кислота , является важным химическим веществом в химии , промышленности или науке. Название HCl иногда неправильно относится к соляной кислоте вместо чистого хлористого водорода. Химики иногда называют газообразную или безводную соляную кислоту хлороводородом.
История
Хлористый водород известен со времен средневековья , когда алхимики знали, что соляная кислота (тогда известная как спирт соли или acidum salis ) при определенных обстоятельствах была связана с парами, называемыми морским кислотным газом .
К XVII — го века , Глаубер использовал соль ( хлорид натрия ) и серную кислоту с получением сульфата натрия , с хлористым водородом вторичного продукта реакции:
- 2 NaCl + H 2 SO 4 → 2 HCl + Na 2 SO 4.
Это открытие иногда приписывают Карлу Вильгельму Шееле , который также провел эту реакцию в 1772 году. Джозеф Пристли получил чистый хлористый водород в 1772 году, а в 1818 году Хэмфри Дэви продемонстрировал, что этот газ состоит из водорода и хлора .
Во время промышленной революции потребность в щелочных веществах , в частности карбонате натрия, становилась все более важной. Николя Леблан разработал новый промышленный процесс производства карбоната натрия . В процессе Леблана соль ( хлорид натрия ) превращается в карбонат натрия с использованием серной кислоты , мела и древесного угля с вторичным образованием хлористого водорода. До принятия в Великобритании Закона о щелочах в 1863 году последний был выпущен в воздух. Производители карбоната натрия затем должны были растворить его в воде , что позволило производить соляную кислоту в промышленных масштабах. Позже был разработан процесс Харгривза , аналогичный процессу Леблана, за исключением того, что серная кислота заменяется диоксидом серы , водой и воздухом . В начале XX — го века , процесс Леблан был заменен на процесс Solvay , который не производит хлористый водород. Однако хлористый водород по-прежнему является этапом производства соляной кислоты .
Химия
Изменение цвета индикатора pH показывает, что газообразный хлористый водород является кислым.
Молекула хлористого водорода хлористого двухатомная молекула , состоящая из одного атома из водорода Н и атома хлора Cl, связанного с помощью одинарной связи . Поскольку хлор гораздо более электроотрицателен, чем водород, связь поляризована. В результате молекула обладает большим дипольным моментом с отрицательным частичным зарядом δ -, переносимым атомом хлора, и положительным частичным зарядом δ +, переносимым атомом водорода. Следовательно, хлористый водород — полярная молекула . Он хорошо растворяется в воде и полярных растворителях .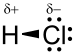
При контакте с водой хлористый водород ионизируется с образованием анионов хлорида Cl — и катионов гидроксония H 3 O + ( сольватированные H + ):
- HCl + H 2 O → H 3 O + + Cl —
Раствор, полученный в результате реакции, называется соляной кислотой . Это сильная кислота, что означает, что константа кислотности K a (которая связана со скоростью диссоциации молекулы HCl) очень высока: хлористый водород почти полностью диссоциирует в воде.
Даже в отсутствие воды хлористый водород по-прежнему действует как кислота . Например, HCl может растворяться в других растворителях, таких как метанол и протонат- ионы или молекулы, действуя как кислота- катализатор для определенных химических реакций, для которых требуются безводные условия (полное отсутствие воды):
- HCl + CH 3 OH → CH 3 O + H 2 + Cl —(протонирование HCl молекулы метанола CH 3 OH)
Из — за его кислую природу, хлористый водород являются коррозионными газами , особенно в присутствии влаги ( 2 — 5 частей на миллион воды достаточно).
Производство
Большая часть производимого в промышленности хлористого водорода используется для производства соляной кислоты .
Распространенным методом производства хлористого водорода в промышленности является «печь HCl», в которой дигидроген и газообразный хлор вступают в экзотермическую реакцию с образованием хлористого водорода:
Cl 2 + H 2 → 2 HCl
Эта реакция используется для получения очень чистого продукта, предназначенного, в частности, для пищевой промышленности.
Хлористый водород также может быть получен из хлора и соединений, содержащих водород, например углеводородов . Хлорирование органических соединений может привести к образованию хлористого водорода:
RH + Cl 2 → R-Cl + HCl
При реакции хлорированных продуктов с фтористым водородом с образованием фторированных соединений также образуется хлористый водород:
R-Cl + HF → RF + HCl
Когда эти реакции происходят в безводной среде (в отсутствие воды), образуется газообразный HCl.
Хлористый водород также может производиться в промышленных масштабах из хлорида натрия (NaCl) и серной кислоты :
2 NaCl + H 2 SO 4 → 2 HCl + Na 2 SO 4 .
Синтез хлороводорода
Хлористый водород можно синтезировать путем медленного добавления воды (или кислоты ) к некоторым хлорированным избыточным реагентам, таким как хлорид фосфора , тионилхлорид (SOCl 2 ) или ацилхлориды . Добавление слишком большого количества воды может привести к растворению образовавшегося хлористого водорода и образованию соляной кислоты . Например, медленное добавление холодной воды к пентахлориду фосфора приводит к образованию следующей HCl:
PCl 5 + H 2 O → POCl 3 + 2 HCl
Добавление горячей воды позволяет получить больше HCl путем гидролиза PCl 5 до фосфорной кислоты . В результате химической реакции между водой и трихлоридом фосфора PCl 3 также образуется HCl.
Реакция тионилхлорида с водой дает HCl, а также диоксид серы SO 2 . Для реакций тионилхлорида или ацилхлоридов с водой см. Тионилхлорид и ацилхлорид .
Генератор HCl
Можно приготовить небольшие количества HCl для использования в лаборатории с помощью генератора HCl различными методами:
- освобождают от концентрированной соляной кислоты с помощью концентрированной серной кислоты .
- освобождение от концентрированной соляной кислоты с помощью безводного хлорида кальция .
- путем реакции серной кислоты и хлорида натрия следующим образом: NaCl + H 2 SO 4 → NaHSO 4 + HCl ↑
Обычно к реагенту в колбе по каплям добавляют соляную или серную кислоту. HCl можно высушить, пропустив ее через концентрированную серную кислоту.
Использует
Исторические использование хлористого водорода в течение XX — го века включает гидрохлорировании из алкин для производства мономеров хлорированных хлоропреновые и винилхлорид , которые затем полимеризуются , чтобы сделать полихлоропрен ( неопрен ) и поливинилхлорид (ПВХ). Для производства винилхлорида к ацетилену (C 2 H 2 ) добавляется HCl по тройной связи с образованием винилхлорида.
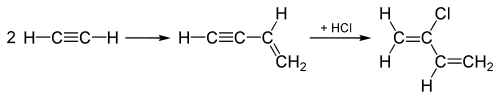
«Ацетиленовый процесс», используемый с 1960-х годов для производства хлоропрена, начинается с реакции двух молекул ацетилена . Полученный промежуточный продукт подвергается присоединению HCl по тройной связи, что приводит к хлоропрену:
Процесс ацетилена был заменен процессом, в котором Cl 2 присоединяется к одной из двойных связей 1,3- бутадиена с последующим удалением, в результате которого образуется хлоропрен и HCl.
В настоящее время основными областями применения хлористого водорода являются:
- в основном производство соляной кислоты
- гидрохлорирование резины
- производство винилхлорида и алкилхлорида
- переработка хлопка
- полупроводниковая промышленность .
Влияние на здоровье
Хлороводород образует соляную кислоту при контакте с тканями тела. Его вдыхание может вызвать кашель, удушье, воспаление носовых стенок, горла и дыхательной системы. В самых тяжелых случаях это может привести к отеку легких , отказу сердечно-сосудистой системы и смерти. Хлористый водород может вызвать серьезные ожоги глаз и необратимые повреждения глаз. Его следует использовать только в хорошо проветриваемом помещении и с маской.
Смотрите также
- соляная кислота
- хлористый
- фтороводород
- бромистый водород
- йодистый водород
Примечания и ссылки
- ↑ a b c d и e ХЛОРИД ВОДОРОДА , паспорт (-ы) безопасности Международной программы по химической безопасности , проверено 9 мая 2009 г.
- ↑ (in) Дэвид Р. Лид, Справочник по химии и физике , Бока-Ратон, CRC,, 89- е изд. , 2736 с. ( ISBN 978-1-4200-6679-1 ) , стр. 9-50
- ↑ рассчитывается молекулярная масса от « атомных весов элементов 2007 » на www.chem.qmul.ac.uk .
- ↑ a b и c (ru) Роберт Х. Перри и Дональд В. Грин , Perry’s Chemical Engineers ‘Handbook , США, McGraw-Hill,, 7- е изд. , 2400 с. ( ISBN 0-07-049841-5 ) , стр. 2-50
- ↑ (in) Клотц, Ирвинг М. / Розенберг, Роберт М., Химическая термодинамика, основные концепции и методы , Wiley-VCH Verlag GmbH & Co. KGaA,, 564 с. ( ISBN 978-0-471-78015-1 и 0-471-78015-4 ) , стр. 98
- ↑ (in) У. М. Хейнс, Справочник по химии и физике , CRC, 2010-2011 91- е изд. , 2610 с. ( ISBN 978-1-4398-2077-3 ) , стр. 14-40
- ↑ (in) Дэвид Р. Лид, Справочник CRC по химии и физике , CRC Press,, 90- е изд. , 2804 с. , Твердый переплет ( ISBN 978-1-4200-9084-0 )
- ↑ «Хлористый водород» , на ESIS , по состоянию на 19 февраля 2009 г.
- ↑ Индексный номер 017-002-00-2 в таблице 3.1 приложения VI Постановления ЕС № 1272/2008 (16 декабря 2008 г.)
- ↑ « Хлористый водород » в базе данных химических продуктов Reptox в CSST (организации Квебека , ответственного за охрану труда и здоровья), доступ к 25 апреля 2009
- ↑ « Хлористый водород », на hazmap.nlm.nih.gov (по состоянию на 14 ноября 2009 г. )
- ↑ « Хлористый водород » , о химической компании Франции ,(по состоянию на 4 июля 2016 г. )
Химический портал
Алф. указатель:
1-9
A-Z
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Щ
Э
Я
Внешний вид:
бесцветн. газ
Кристаллические модификации, цвет растворов и паров:
В жидком виде — бесцветная легко подвижная жидкость. Кристаллизуется в кубической решетке, ниже -174,15 С существует ромбическая модификация.
Брутто-формула (система Хилла): HCl
Молекулярная масса (в а.е.м.): 36,46
Температура плавления (в °C): -114,2
Температура кипения (в °C): -85,08
Температура разложения (в °C): 1500
Температурные константы смесей:
108,584 °C (температура кипения азеотропа, давление 1 атм) вода 79,778% хлороводород 20,222%
-74,7 °C (температура плавления эвтектической смеси) вода 77% хлороводород 23%
Растворимость (в г/100 г или характеристика):
бензол: растворим 1,9 (20°C)
вода: 96 (-18,3°C)
вода: 93,31 (-15°C)
вода: 89,79 (-10°C)
вода: 82,3 (0°C)
вода: 78,7 (10°C)
вода: 72,47 (20°C)
вода: 67,3 (30°C)
вода: 63,3 (40°C)
вода: 59,6 (50°C)
вода: 56,1 (60°C)
диэтиловый эфир: растворим 33,2 (20°C)
метанол: 88,7 (20°C)
серная кислота концентрированная: 0,4015 (25°C)
этанол: растворим
этанол абсолютный: 69,5 (20°C)
Вкус, запах, гигроскопичность:
запах: резкий
Плотность:
0,0016391 (0°C, г/см3)
1,187 (-85,1°C, г/см3)
1,045 (-155°C, г/см3)
1,469 (-166°C, г/см3)
1,48 (-154,79°C, г/см3)
Показатель преломления (для D-линии натрия):
1,0004456 (0°C)
1,256 (-85,1°C)
Плотность растворов (г/см3):
1,01 (2.36%, 20°C, растворитель — вода)
1,03 (6.43%, 20°C, растворитель — вода)
1,05 (10.52%, 20°C, растворитель — вода)
1,06 (12.51%, 20°C, растворитель — вода)
1,07 (14.49%, 20°C, растворитель — вода)
1,08 (16.47%, 20°C, растворитель — вода)
1,1 (20.39%, 20°C, растворитель — вода)
1,155 (31.14%, 20°C, растворитель — вода)
1,198 (40%, 20°C, растворитель — вода)
Показатель диссоциации:
pKa (1) = -7 (25 C, вода)
Диэлектрическая проницаемость:
1,0046 (25°C)
14,2 (-114,02°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
-91,8 (г)
Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль):
-94,79 (г)
Стандартная энтропия образования S (298 К, Дж/моль·K):
186,8 (г)
Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K):
29,13 (г)
Энтальпия плавления ΔHпл (кДж/моль):
1,99
Энтальпия кипения ΔHкип (кДж/моль):
16,15
Симптомы острого отравления:
Животные. При высоких концентрациях — некроз слизистых, главным образом носа и подлежащих тканей, помутнение роговицы. Дыхание иногда замедлено. Общее состояние тяжелое. Поздними следствиями могут быть воспалительные заболевания легких. При смертельном исходе иа вскрытии — отек и гиперемия легких, иногда кровоизлияния в желудке. Вдыхание 6,40 мг/л в течение 30 мин вызывает у кроликов и морских свинок быструю смерть (спазм и отек гортани, отек легкого). Вдыхание 5,0 мг/л в течение 1,5 ч приводит кроликов и морских свинок к смерти через 2-6 дней. При невысоких концентрациях — раздражение слизистой носа, слюнотечение; 0,45 мг/л при воздействии в течение 6 ч вызывают катар дыхательных путей, легкое поражение роговицы. У кошек и кроликов вдыхание 0,15-0,21 мг/л по 6 ч в день в течение 50 дней вызывает лишь беспокойство, раздражение, небольшое уменьшение содержания гемоглобина в крови. 12 экспозиций по 6 ч при 0,05 мг/л не вызывают видимого заболевания у обезьян и других животных (Machle et al.). Интратрахеальное введение 2 или 3 мл/кг 0,1 н. HCl вызывает нарушение дыхания и сердцебиения, гибель собак (Greenfield et al.).
Человек. При высоких концентрациях — раздражение слизистых, в особенности носа; конъюнктивит; помутнение роговицы. Охриплость, чувство удушья, покалывание в груди, насморк, кашель, иногда кровь в мокроте. Концентрации 0,05-0,075 мг/л переносятся с трудом, хотя «привычные» люди выносят в течение нескольких минут даже концентрации 1-2 мг/л. Хроническое отравление вызывает катары дыхательных путей; разрушение зубов; изъязвления слизистой носа и даже прободение носовой перегородки; желудочно-кишечные расстройства; возможны воспалительные заболевания кожи. Описай случай тяжелого отравления: сильное исхудание, слабость; горячая, сухая, землистая кожа; кашель, учащенное дыхание, мелкопузырчатые хрипы; мокрота отхаркивается о большим трудом; сердечная деятельность нормальная, но по нескольку раз в день сильные сердцебиения. Пульс — 70-80. Острые боли в области желудка, рвота желтоватой слизью. По весьма совпадающим данным разных авторов, предельная безвредная при постоянной работе концентрация — 0,015 мг/л. Наблюдается якобы привыкание к хлороводороду, причина которого пока неясна.
Действие на кожу. Туман соляной кислоты, образующийся при нагревании растворов для травления, вызывает резкую болезненность кожи лица. Ожоги в большинстве случаев не столь тяжелы, как при действии серной и азотной кислот. Обычно возникает чисто серозное воспаление с пузырями. Изъязвления развиваются лишь при более длительном воздействии (если, например, после попадания на кожу кислота сразу не отмыта). Тем не менее у травильщиков на руках иногда наблюдаются значительные изъязвления.
Лечение отравлений:
Немедленно вынести пострадавшего на свежий воздух, освободить от стесняющей дыхание одежды. Ингаляция кислорода. Промывание глаз, носа, полоскание 2% раствором соды. При затруднении дыхания через нос — 2-3% раствор эфедрина 3-4 раза в день по 4-5 капель, подкожно атропин (1 мл 0,1% раствора). Тепло на область шеи. При кашле — кодеин, дионин, тепловлажные ингаляции 2-3% раствора соды (2-3 раза в день по 10 мин). В дальнейшем — отхаркивающие средства, горчичники на область трахеи, теплое молоко с боржомом или содой, маслом или медом. В более тяжелых случаях для профилактики и лечения пневмонии — ингаляции аэрозолей антибиотиков, курс лечения антибиотиками и сульфаниламидами.
При поражении глаз после промывания впустить в глаза по 1 капле 2% раствора новокаина или 0,5% раствора дикаина с адреналином (1:1000) с последующей инсталляцией стерильного вазелинового или персикового масла в конъюнктивальный мешок. Очки-консервы. В дальнейшем — 30% раствор альбуцида, гидрокортизоновая мазь. При попадании кислоты в глаза промывать их водой, а не нейтрализующими (щелочными) растворами.
При попадании крепкой кислоты на кожу — немедленное обмывание ее водой, лучше под давлением (например, из гидранта в течение 5-10 мин. В здравпункте наложить на обожженную поверхность кашицу из соды.
Критическая температура (в °C):
51,4
Критическое давление (в МПа):
8,26
Критическая плотность (в г/см3):
0,42
Применение:
Водный раствор используется для получения хлоридов, для травления металлов, очистки поверхности сосудов, скважин от карбонатов, обработки руд, при производстве каучуков, глутамината натрия, соды, хлора и других продуктов.
Дополнительная информация:
Химия безводного хлороводорода и его водного раствора различны.
Безводный хлороводород сильно дымит во влажном воздухе. Безводный хлороводород химически пассивен: не реагирует с серой, фосфором, углем, многими металлами. С нитридами, карбидами, боридами и сульфидами реагирует выше 650 С, с гидридами кремния, германия и бора — в присутствии хлорида алюминия, с оксидами переходных металлов — при 300 С и выше. Окисляется кислородом и азотной кислотой до хлора, с триоксидом серы дает хлорсульфоновую кислоту.
Водный раствор называется соляная кислота. Это бесцветная жидкость с резким запахом, сильная кислота, химически активна. Растворяет с выделением водорода все металлы имеющие отрицательный нормальный потенциал, со многими оксидами и гидроксидами дает хлориды, вытесняет более слабые кислоты (фосфорную, борную и т.д.) из их солей.
Производство 31%-ной соляной кислоты в СССР составляло 1 520 000 т. (1986).
- «Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей» 7-е изд. т.3 Л.:Химия 1976 стр. 41-42
- «Справочник химика» т.3, Л.-М.: Химия, 1965 стр. 80, 322
- «Химическая энциклопедия» т.4 М.: Советская энциклопедия, 1995 стр. 381-383
- Лурье Ю.Ю. «Справочник по аналитической химии» М.:Химия, 1979 стр. 91
- Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 110
Источники информации:
Алф. указатель:
1-9
A-Z
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Щ
Э
Я