сульфат алюминия неорганическая соль алюминия формулы Al2(SO4)3, это обычно выглядит как белое твердое вещество с блестящими кристаллами. Цвет соединения будет зависеть от его концентрации железа и любых других примесей. Существует два основных типа сульфата алюминия: A и B.
На нижнем изображении показаны белые кристаллы гидратированного сульфата алюминия. Можно отметить отсутствие коричневых окрасок, указывающих на ионы железа в кристаллической решетке..
Сульфат алюминия — это соль, которая очень хорошо растворяется в воде, и в природе редко можно найти ее в безводной форме. Обычно гидратируется в форме октадекагидрата сульфата алюминия [Al2(SO4)3.18H2O] или гексадекагидрат [Al2(SO4)3.16H2O].
Кроме того, он может образовывать двойные соли с калием и аммонием, соединения, известные как квасцы. Частично это может быть связано со сродством воды в гидратах удерживать другие ионы, кроме алюминия.
Сульфат алюминия может разлагаться под действием воды в гидроксиде алюминия и серной кислоте. Это свойство позволило использовать его в качестве подкислителя почв.
Это также токсичное соединение, особенно при контакте с его порошком. Тем не менее, он имеет бесконечное число применений и применений, которые идут от очистки воды с помощью метода коагуляции, происходящего через его использование в нескольких отраслях промышленности, до его использования в терапевтических целях..
индекс
- 1 структура
- 2 Для чего это (использует)
- 2.1 Коагуляция или флокуляция воды
- 2.2 Использование в качестве протравы чернил и при разработке бумаги
- 2.3 Промышленное использование
- 2.4 Лекарственное и терапевтическое использование
- 2.5 Другое использование
- 3 Производство сульфата алюминия
- 4 Типа
- 5 Токсичность
- 6 Ссылки
структура
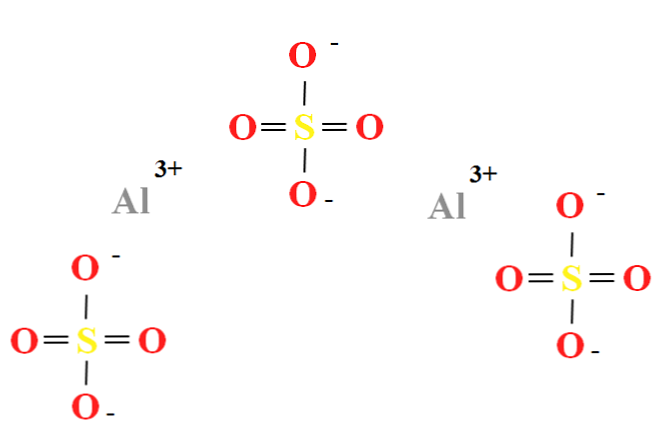
Сульфат алюминия имеет соотношение двух катионов Al3+ на каждые три аниона ТАК42- (верхнее изображение), что можно наблюдать непосредственно в его химической формуле Al2(SO4)3.
Обратите внимание, что Аль3+ они сероватые, а ТАК42- они желтые (для атома серы) и красные (для атомов кислорода).
Проиллюстрированная структура соответствует безводной форме Al2(SO4)3, так как ни одна молекула воды не взаимодействует с ионами. В ваших гидратах, однако, вода может быть привлечена к положительным центрам Al3+, или отрицательным SO тетраэдров42- через водородные связи (HOH-O-SO32-).
Аль2(SO4)3H 18H2Или, например, он содержит 18 молекул воды в своей твердой структуре. Некоторые из них могут находиться в прямом контакте с Алом3+ или с SO42-. Другими словами: сульфат алюминия может иметь внутреннюю или внешнюю координационную воду.
Кроме того, его структура может вместить другие катионы, такие как Fe3+, не доступно+, К+, и т.д. Но для этого необходимо присутствие большего количества анионов ТАК42-. Для чего? Для нейтрализации увеличения положительных зарядов за счет металлических примесей.
Сульфат алюминия может иметь много структур, хотя его гидраты имеют тенденцию принимать моноклинную кристаллическую систему.
Физико-химические свойства
внешний вид
Он выглядит как твердое вещество с блестящими белыми кристаллами, гранулами или порошком.
Молекулярный вес
342,31 г / моль (безводный).
запах
Без запаха
аромат
Сладкий вкус умеренно вяжущий.
Точка плавления
770ºС безводная форма (86,5ºС октадекагидратада)
Растворимость в воде
31,2 г / 100 мл при 0 ° С; 36,4 г / 100 мл при 20 ° С и 89 г / 100 мл при 100 ° С.
плотность
От 2,67 до 2,71 г / см3.
растворимость
Слабо растворим в этиловом спирте.
Давление пара
По сути ноль.
стабильность
Стабильный в воздухе.
разложение
При нагревании примерно до точки плавления он может разлагаться, выделяя, в частности, оксид серы, токсичный газ..
коррозионная активность
Растворы сульфата алюминия вызывают коррозию алюминия. Также соединение может разъедать металлы в присутствии влаги.
рКа
3,3 до 3,6. И его pH составляет 2,9 или более в 5% водном растворе.
Для чего это (использует)
Коагуляция или флокуляция воды
-При смешивании с водой (пригодной для питья, подачи или отходов) сульфат алюминия вызывает образование гидроксида алюминия, который образует комплексы с соединениями и частицами в растворе, ускоряя их осаждение, что в отсутствие обработки сульфатом алюминия может привести к долгое время.
-Сульфат алюминия также используется при очистке воды в бассейне, что делает его более привлекательным для использования.
-Благодаря использованию сульфата алюминия вода получается без мутности и цвета, что повышает ее способность к обработке за счет облегчения очистки воды. К сожалению, этот метод очистки может привести к незначительному увеличению концентрации алюминия в воде..
-Алюминий является очень токсичным металлом, который накапливается в коже, мозге и легких, вызывая серьезные нарушения. Кроме того, неизвестно, какую функцию он выполняет в живых существах..
-Европейский Союз требует, чтобы максимально допустимый предел содержания алюминия в воде не превышал 0,2 мг / л. Между тем, Агентство по охране окружающей среды США требует, чтобы максимальный предел загрязнения воды алюминием не превышал 0,05-0,2 мг / л..
-Очистка сточных вод или использование сульфата алюминия позволяет экономно удалять или уменьшать содержание фосфора в них..
Использование в качестве протравы чернил и при разработке бумаги
-Сульфат алюминия использовался в качестве протравы для красителей или чернил, помогая закрепиться на красящем материале. Его фиксирующее действие обусловлено Al (OH)3, чья желатиновая консистенция способствует адсорбции красителей на текстиле.
-Хотя он использовался примерно с 2000 г. до н.э. для описанной цели, только органические красители требуют морилки. Синтетические красители, с другой стороны, не требуют протравы для выполнения своей функции.
-Это было вытеснено из производства бумаги, но это все еще используется в производстве бумажной массы. Удаляет примеси, а также используется для связывания материалов, нейтрализации зарядов и калибровки канифоли.
Промышленное использование
-Он используется в строительной промышленности для ускорения схватывания бетона. Кроме того, он используется в гидроизоляции зданий.
-В производстве мыла и жиров он используется в производстве глицерина.
-Он используется в нефтяной промышленности при производстве синтетических катализаторов, которые используются во время эксплуатации.
-Он используется в фармацевтической промышленности в качестве вяжущего при приготовлении лекарств и косметики.
-Вмешивается в производство красителей, таких как кармин. Он также используется в качестве красителя при производстве синтетических каучуков бутадиен-стирола..
-В сахарной промышленности его используют в качестве очистителя мелассы для сахарного тростника..
-Используется при изготовлении дезодорантов. Почему? Потому что это вызывает сужение протоков потовых желез, ограничивая тем самым накопление пота, необходимой среды для роста бактерий, вызывающих запах.
-Используется при дублении кожи, необходим процесс его использования. Кроме того, он используется в производстве удобрений.
-Используется в качестве добавки при приготовлении красок, адгезивов и герметиков, а также в средствах для чистки и ухода за мебелью..
Лечебное и терапевтическое использование
-Сульфат алюминия является иммунологическим адъювантом. Следовательно, он выполняет функцию обработки антигенов таким образом, что при высвобождении в месте их действия они производят большую продукцию антител к антигенам, которые были инокулированы..
-Адъювант Фрейнда и БЦЖ, а также другие адъюванты, в том числе эндогенные, такие как интерлейкины, неспецифичны для антигенов, что позволяет увеличить радиус действия иммунитета. Это позволило разработать вакцины против многочисленных заболеваний.
-Коагулирующее действие сульфата алюминия позволило устранить многочисленные вирусы в очищенной воде, среди прочего: Q бета, MS2, T4 и P1. Результаты показывают, что обработка воды сульфатом алюминия приводит к инактивации таких вирусов..
-Сульфат алюминия используется в форме карандаша или в виде порошка при лечении мелких поверхностных ран или ссадин, возникающих при бритье.
-Он используется в производстве ацетата алюминия, соединения, используемого при лечении некоторых заболеваний уха. Он также использовался без особого успеха для смягчения последствий укусов муравьев..
-Растворы сульфата алюминия используются в концентрации от 5 до 10% при местном лечении язв, что позволяет контролировать их секрецию.
-Вяжущее действие сульфата алюминия сокращает поверхностные слои кожи, коагулируя белки и заживляя раны.
Другое использование
-Сульфат алюминия помогает контролировать чрезмерный рост водорослей в прудах, озерах и в потоках воды. Он также используется для удаления моллюсков, в том числе испанского слизняка.
-Садовники применяют это соединение для подкисления щелочных почв. При контакте с его водой сульфат алюминия разлагается на гидроксид алюминия и разбавленную серную кислоту. Затем гидроксид алюминия выпадает в осадок, оставляя серную кислоту в растворе.
-Подкисление почв из-за серной кислоты визуализируется очень творчески, благодаря наличию растения под названием гортензия, чьи цветы становятся синими в присутствии кислой почвы; то есть они чувствительны и реагируют на изменения pH.
-Сульфат алюминия участвует в производстве пены для борьбы с огнем и борьбы с ним. Как? Реагирует с бикарбонатом натрия с выделением СО2. Этот газ блокирует доступ O2 до места сгорания материала; и, следовательно, прекращение огня, которое развивалось.
Производство сульфата алюминия
Сульфат алюминия синтезируется путем взаимодействия обогащенного алюминием соединения, такого как бокситовая руда, с серной кислотой при повышенных температурах. Следующее химическое уравнение представляет реакцию:
в2О3 + H2SW4 -> Ал2(SO4)3 + 3 ч2О
Сульфат алюминия также может образовываться в результате реакции нейтрализации между гидроксидом алюминия и серной кислотой в соответствии со следующей реакцией:
2 Al (OH)3 + 3 ч2SW4 + 12 ч2O -> Al2(SO4)3.18H2О
Серная кислота вступает в реакцию с алюминием, образуя сульфат аммония и выделяя молекулы водорода в виде газа. Реакция схематизируется следующим образом:
2 Al + 3 H2SW4 -> Ал2(SO4)3 + 3 ч2
тип
Сульфат алюминия подразделяется на два типа: тип A и тип B. В сульфате алюминия типа A твердые вещества имеют белый цвет и имеют концентрацию железа менее 0,5%..
В сульфате алюминия типа B твердые вещества коричневые и имеют концентрацию железа менее 1,5%..
Есть отрасли, производящие сульфат алюминия, которые имеют различные критерии для их классификации. Так, промышленность сообщает, что для его приготовления сульфата алюминия типа А максимальная концентрация железа составляет 0,1% в виде оксида железа. В то время как для типа B они указывают максимальную концентрацию железа 0,35%.
токсичность
-Сульфат алюминия — это соединение, которое оказывает токсическое действие при контакте с пылью, вызывая раздражение кожи, а в случаях частого контакта — дерматит..
-В глазах это вызывает сильное раздражение, даже вызывает постоянные травмы..
-Вдыхание вызывает раздражение носа и горла, что может вызвать кашель и сыпь.
-Его прием вызывает раздражение желудка, тошноту и рвоту.
-Существуют токсические эффекты, которые, хотя они не связаны непосредственно с сульфатом алюминия, косвенно связаны с их использованием. Это случай определенных токсических эффектов алюминия, вызванных использованием сульфата алюминия при очистке воды..
-Пациенты, которые подвергаются хроническому диализу с использованием солей, приготовленных в очищенной воде, с использованием сульфата алюминия, испытывают очень серьезные нарушения здоровья. Среди этих нарушений у нас есть анемия, деменция при диализе и рост заболеваний костей..
ссылки
- Wikipedia. (2018). Сульфат алюминия Взято из: en.wikipedia.org
- Арис Индастриал Раствор сульфата алюминия типа А и В. Взято с сайта: aris.com.pe
- Кристофер Бойд (9 июня 2014 г.) Лучшие промышленные применения для сульфата алюминия. Взято из: chemservice.com
- PubChem. (2018). Сульфат алюминия безводный. Взято из: pubchem.ncbi.nlm.nih.gov
- Andesia Chemicals (20 августа 2009 г.) Лист безопасности из сульфата алюминия. [PDF]. Взято из: andesia.com
- Химическая Книга. (2017). Сульфат алюминия. Взято из: chemicalbook.com
- Сульфа́т алюми́ния — сложное неорганическое соединение, соль алюминия и серной кислоты с химической формулой Al2(SO4)3. Выглядит как бесцветные кристаллы, может образовывать кристаллогидраты с различным содержанием воды. Применяется при очистке воды, крашении тканей, дублении кож, как реактив в фотографии, для получения квасцов.
Источник: Википедия
Связанные понятия
Сульфид натрия, устар. сернистый натрий, — сложное неорганическое вещество с химической формулой Na2S.
Гидрокси́д алюми́ния — вещество с формулой Al(OH)3 (а также H3AlO3) — соединение оксида алюминия с водой. Белое студенистое вещество, плохо растворимое в воде, обладает амфотерными свойствами.
Хроматы — соли хромовой кислоты H2CrO4. Устойчивы в нейтральной и щелочной среде, в кислой среде обратимо переходят в дихроматы — соли дихромовой кислоты H2Cr2O7.
Карбона́т ба́рия — химическое соединение, бариевая соль угольной кислоты. Химическая формула BaCO3. В природе встречается в виде минерала витерита.
Упоминания в литературе
В качестве коагулянта применяется сульфат алюминия. Для улучшения коагуляции используются высокомолекулярные флокулянты: щелочной крахмал, активизированная кремниевая кислота и другие синтетические препараты.
Коагуляция заключается в добавлении к воде коагулянта – чаще всего алюминия сульфата. В процессе коагуляции образуются гидрооксиды, которые адсорбируют загрязнители и быстро выпадают в осадок в виде хлопьев, освобождая воду от взвешенных частиц.
Является эффективным материалом для нейтрализации кислотности почвы и снабжения культур кальцием. Примесей в ней очень мало. Овощи более других культур отзывчивы на известкование, даже на слабокислых почвах. Наибольший эффект от извести бывает при внесении ее с осени, при оптимуме в почве калия, равномерности распределения в корнеобитаемой зоне растений, добавке золы. Быстроту взаимодействия извести с почвой обеспечивает ее тонкий помол. Известь действует на почву химически и механически, закрепляет в почве органические вещества. Навоза при известковании требуется вносить меньше. Коэффициент использования азота от наличия извести повышается в 2–2,4 раза из сульфата алюминия и в 1,3–1,5 раз из аммиачной селитры.
Связанные понятия (продолжение)
Сульфи́т на́трия (сернистокислый натрий) — неорганическое соединение, соль натрия и сернистой кислоты…
Гидроксид цезия (CsOH) — химическое соединение, содержащее атом цезия и гидроксильную группу.
Карбонат аммония, углекислый аммоний, (NH4)2CO3 — аммониевая соль угольной кислоты.
Хлори́д ка́льция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным.
Хлорид лития — химическое соединение щелочного металла лития и хлора с формулой LiCl.
Тиосульфа́т на́трия (антихлор, гипосульфит, сульфидотриоксосульфат натрия, натрий серноватистокислый) — Na2S2O3 или Na2SO3S, соль натрия и тиосерной кислоты, образует кристаллогидрат Na2S2O3·5H2O.
Аминосульфоновая кислота (Сульфаминовая кислота, моноамид серной кислоты, амидосерная кислота) — кислота, формула которой NH2SO2OH (также NH2SO3H). Производные этой кислоты называют сульфаматами.
Ионообменные смолы — синтетические органические иониты — высокомолекулярные синтетические соединения с трехмерной гелевой и макропористой структурой, которые содержат функциональные группы кислотной или основной природы, способные к реакциям ионного обмена.
Абиетиновая кислота (от лат. abies — ель), сист. 13-изопропилподокарпа-7,13-диен-15-овая кислота — одна из смоляных кислот, наиболее известная. В природе имеет растительное происхождение, входит в состав смолы хвойных, основной компонент канифоли и янтаря. Её относят к дитерпеновой трициклической группе природных соединений (соединения, полученные из четырёх изопреновых фрагментов). Это аморфное или кристаллическое вещество насыщенно-желтого цвета. Растворима в большинстве популярных неполярных растворителей…
Тетрабора́т на́трия («бура́», «боракс» (от лат. borax)) — неорганическое соединение, натриевая соль борной кислоты с химической формулой Na2B4O7, наиболее распространённое и используемое соединение бора, образует несколько кристаллогидратов, широко применяется в промышленности.
Перекристаллиза́ция — метод очистки вещества, основанный на различии растворимости вещества в растворителе при различных температурах (обычно интервал температур от комнатной до температуры кипения растворителя, если растворитель — вода, или до какой-то более высокой температуры). Перекристаллизация подразумевает плохую растворимость вещества в растворителе при низких температурах, и хорошую— при высоких. При нагревании колбы вещество растворяется. После стадии адсорбции примесей (если это необходимо…
Гидрокси́д ба́рия (е́дкий бари́т) — неорганическое соединение, проявляющее сильные основные свойства. Химическая формула — Ba(OH)2. Насыщенный водный раствор гидроксида бария называется баритовой водой.
Ацетат кальция — кальциевая соль уксусной кислоты. Бесцветное кристаллическое или аморфное вещество, хорошо растворимое в воде. Технический моногидрат может быть в форме гранул или некрупных игл. Обладает слабым вкусом и запахом уксуса. Химическая формула — Ca(CH3COO)2, однако чаще получают его моногидрат Ca(CH3COO)2•H2O.
Тиосульфа́ты — соли и сложные эфиры тиосерной кислоты, H2S2O3. Тиосульфаты неустойчивы, поэтому в природе не встречаются. Наиболее широкое применение имеют тиосульфат натрия и тиосульфат аммония.
Хлори́д ба́рия (хлористый барий) — бинарное неорганическое вещество, относящееся к классу солей. Химическая формула — BaCl2.
Оксид бария — соединение бария с кислородом, имеющее химическую формулу BaO. Является основным оксидом. При стандартных условиях представляет собой бесцветные кристаллы с кубической решёткой.
Хлорид аммония (хлористый аммоний; техническое название — нашаты́рь; NH4Cl) — соль аммония, белый кристаллический слегка гигроскопичный порошок без запаха.
Иоди́д ка́лия (иодистый калий) — неорганическое соединение, калиевая соль иодоводородной кислоты с химической формулой KI. Бесцветная кристаллическая соль, желтеющая на свету. Широко используется в качестве источника иодид-ионов. Менее гигроскопична чем иодид натрия. Применяется в медицине как лекарственное средство, в сельском хозяйстве как удобрение, а также в фотографии и аналитической химии.
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Молекулярные сита — кристаллические алюмосиликаты, имеющие трёхмерную структуру из тетраэдров оксида кремния и оксида алюминия и характеризующиеся точным и однородным размером пор. Поры в молекулярных ситах достаточно велики, чтобы пропускать небольшие молекулы, но в то же время они задерживают более крупные молекулы, что определило их использование в качестве осушителей и адсорбентов.
Окси́д на́трия — бинарное неорганическое вещество, имеющее формулу Na2O и относящееся к классу основных оксидов.
Метилацета́т (метиловый эфир уксусной кислоты, метиловый эфир этановой кислоты, уксуснометиловый эфир, MeOAc) CH3COOCH3 — органическое вещество класса сложных эфиров.
Хлорат калия (бертолетова соль, калий хлорноватокислый) — KClO3, калиевая соль хлорноватой кислоты (HClO3).
Оксид кадмия (англ. Cadmium oxide) — химическое соединение с формулой CdO. CdO — основное сырьё для производства других соединений кадмия. Редко встречается в природе в минерале монтепоните. Оксид кадмия может образовывать кристаллическую структуру, сходную с решёткой NaCl. Вещество может образовывать бесцветный порошок или кристаллы красно-бурого цвета. Оксид кадмия является полупроводником n-типа.
Циклогексанон — органическое соединение, алициклический кетон, бесцветная маслянистая жидкость с запахом ацетона и мяты.
Сульфа́т ба́рия (сернокислый барий) — сернокислая соль бария. Химическая формула — BaSO4.
Диметиланилин (N,N-диметиланилин) — органическое соединение, принадлежащее классу третичных аминов. Формально является производным аммиака, в котором атомы водорода замещены на фенильный и два метильных радикала.
Аммиака́ты (амми́ны, аммѝноко́мплексы) — продукты взаимодействия солей с аммиаком, комплексные соединения, содержащие в качестве лигандов молекулы аммиака. Лиганды NH3 связаны в аммиакатах с центральным атомом металла через азот.
Нитрат магния Mg(NO3)2 — бесцветные гигроскопичные кристаллы с кубической решеткой (а = 0,748 нм, пространств. группа Ра3); температура плавления 426 °C (с разложением); С°р 141,9 Дж/(моль. К); DH0обр −792,8 кДж/моль, DG0обр −591,4 кДж/моль. Выше 300 °C начинает разлагаться на MgO и оксиды азота. Растворимость в воде (г в 100 г): 73,3 (20 °C), 81,2 (40 °C), 91,9 (60 °C). Растворим также в этаноле, метаноле, жидком NH3. Из водных растворов в зависимости от концентрации кристаллизуются нона-, гекса…
Хлорбензол (фенилхлорид) — ароматическое органическое соединение, имеющее формулу C6H5Cl, бесцветная горючая жидкость с характерным запахом.
Амиловый спирт C5H11OH и его изомеры — предельные одноатомные спирты. Известны все 8 изомерных амиловых спиртов.
Нитри́т ка́лия (азотистокислый калий) — калиевая соль азотистой кислоты с формулой KNO2.
Дихрома́т на́трия (бихромат натрия, натриевый хромпик) — неорганическое химическое соединение, натриевая соль дихромовой кислоты. Существует дигидрат дихромата натрия( Na2Cr2O7·2H2O) и безводная соль.
Алюмогидрид лития (аланат лития) — неорганическое соединение, комплексный смешанный гидрид лития и алюминия с формулой Li, белые кристаллы.
Иониты — твердые нерастворимые вещества, способные обменивать свои ионы на ионы из окружающего их раствора. Обычно это синтетические органические смолы, имеющие кислотные или щелочные группы. Иониты разделяются на катиониты, поглощающие катионы, аниониты, поглощающие анионы и амфотерные иониты, обладающие обоими этими свойствами. Широко применяются иониты для опреснения вод, в аналитической химии для разделения веществ методом хроматографии, в химической технологии. Иониты распространены в природе…
Хлорсульфо́новая кислота, HSO3Cl — монохлорангидрид серной кислоты, бесцветная, дымящая на воздухе и резко пахнущая жидкость.
Омыление — гидролиз сложного эфира с образованием спирта и кислоты (или её соли, когда для омыления берут раствор щёлочи)…
Термолиз (от греч. ϑέρμη — «тепло» и λύσις — «распад») — процесс разложения химических соединений под воздействием температуры без применения катализаторов.
Сульфа́т аммо́ния (аммоний серноки́слый, лат. ammonium sulphate), (NH4)2SO4 — неорганическое бинарное соединение, аммонийная соль серной кислоты. Это бесцветные прозрачные кристаллы (или белый порошок) без запаха. Получают сульфат аммония действием серной кислоты на раствор аммиака и обменными реакциями с другими солями. Применяется в качестве удобрения, при производстве вискозы, в пищевой промышленности, при очистке белков в биохимии, в качестве добавки при хлорировании водопроводной воды. Токсичность…
Ами́д на́трия — неорганическое вещество с формулой NaNH2, производное аммиака. Представляет собой твёрдое вещество, которое реагирует с водой. Применяется в органическом синтезе.
Пирогалло́л (пирогалловая кислота, 1,2,3-тригидроксибензол) — органическое соединение, трехатомный фенол с химической формулой C6H6O3, бесцветные кристаллы, темнеющие на воздухе. Применяется в органическом синтезе как восстановитель, также используется в промышленности как полупродукт в производстве красителей, в фотографии как проявляющее вещество.
Иодиды — бинарные соединения иода с менее электроотрицательными элементами. Иодиды металлов могут рассматриваться как соли иодоводородной кислоты HI.
Монохлоруксусная кислота CH2ClCOOH — уксусная кислота, в которой один атом водорода метильной группы замещён на атом хлора, бесцветные кристаллы.
Реакция ионного обмена — один из видов химических реакций, протекающих в полярных растворителях между ионами исходных компонентов. Обратимые реакции ионного обмена приводят к наличию в растворах продуктов перекрестного синтеза, например, из смеси растворов хлорида натрия и бромида калия при выпаривании кристаллизуются четыре вещества. Необратимые реакции ионного обмена сводятся к образованию из ионов нерастворимых соединений с их выделением в виде воды, газа или осадка.
Адипи́новая кислота́ (гександио́вая кислота) НООС(СН2)4СООН — двухосновная предельная карбоновая кислота. Обладает всеми химическими свойствами, характерными для карбоновых кислот.
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Сернокислый алюминий — это сложное неорганическое вещество, соль белого цвета с серым или голубым оттенком. Вещество может иметь розовый оттенок.
Востребованная соль алюминия.
Соль Al₂(SO₄)₃ очень гигроскопична. Отличается быстрой растворимостью в воде. Вещество плавится при температуре +700 °C, плотность его равняется 1,62–2,67 г/см³.
Сернокислый алюминий — это самый распространенный коагулянт, применяемый для очистки воды от коллоидных частиц (наиболее мелких размеров). Это свойство сульфата алюминия связано с легкостью его получения и невысокой стоимостью.
Способы получения сульфата алюминия.
Соль выпускают 3 сортов. Продукт высшего сорта востребован в пищевой и фармацевтической промышленности, а соль 1 и 2 сорта подходит для технических целей. Сернокислый алюминий получают несколькими способами:
металлическая мебель https://www.safe24.ru/
- Соль высшего сорта получают в результате реакции замещения между гидроксидом алюминия и серной кислотой высокой концентрации. В результате этого процесса алюминий, отличающийся большей активностью, занимает место водорода в составе кислоты. По окончании реакции получают 1 молекулу соли сульфата алюминия и 6 молекул воды. Полученный коагулянт имеет высокий процент чистоты с минимальной долей примесей.
- Получить соль технического качества можно в результате обработки серной кислотой бокситов или глиноземов. Этот метод также основан на реакции по замене молекул водорода алюминием. В результате метода получают соль 1–2 сорта. Высвобожденный водород поднимается в атмосферу. Этот метод является промежуточным процессом для получения чистого алюминия из бокситов.
- Еще один способ — это получить коагулянт из оксида, обработанного серной кислотой.
Получить соль алюминия в домашних условиях можно, используя серную кислоту и кусочек алюминиевой фольги. При проведении реакции следует быть очень осторожным и соблюдать правила безопасности по работе с кислотами. Проводить реакцию нужно в хорошо проветриваемом помещении. Серная кислота разной концентрации продается в хозяйственных магазинах.
Для получения кристаллов коагулянта ее нужно развести до 10% концентрации дистиллированной водой. Фольга растворяется в течение 7 дней. Полученный раствор фильтруют через бумажный фильтр. Остаток воды испаряется на открытом воздухе. Ускорить процесс можно выпариванием на электроплитке, перелив раствор в термостойкий стакан.
Очень важное замечание: при разведении серной кислоты и других кислот следует кислоту лить в воду, а не наоборот. Фольгу замачивают в растворе кислоты, накрывают салфеткой и оставляют для прохождения химической реакции.
Соль высшего качества имеет сыпучую консистенцию, производится в виде образований размером до 20 мм. Соль для технических целей выпускают крупными кристаллами-пластинами или большими кусками весом до 10 кг.
Попадание сернокислого алюминия в организм человека может нанести ему непоправимый ущерб. Вещество может привести к ожогу носоглотки. Попадание на кожу или в глаза вызывает покраснение, зуд, боль, ожог. Попадание в желудочно-кишечный тракт может вызывать болевые приступы в желудке, рвоту и диарею.
Первая помощь при отравлении химикатом:
- промыть глаза и открытые участки кожи;
- организовать доступ свежего воздуха или вывести пострадавшего на улицу;
- напоить пострадавшего молоком и вызвать рвоту;
- обратиться в медицинское учреждение.
Применение сульфата алюминия в очистке водопроводной воды.
Полученное из глиноземов или бокситов вещество применяют как сильный коагулянт для очистки воды от коллоидных частиц. Данные частицы обладают отрицательным электрическим зарядом. К коллоидным частицам присоединяются ионы из окружающего их раствора с положительным зарядом. Это создает на их поверхности двойной электрический слой. В результате коллоидные частицы начинают отталкиваться друг от друга. У них небольшой удельный вес, и они находятся во взвешенном состоянии.
Коагулянт (в данном случае — это сульфат алюминия) несет на себе положительный ион. Он сжимает двойной электрический слой и нейтрализует его. Частицы получают дестабилизированный вид. Они окружают коагулянт при установлении контакта с ним. Если смесь в этот момент быстро перемешать, то химическое вещество получит однородную дисперсию. Это позволит увеличить максимальный контакт между частицами.
Если перемешивать смесь несколько минут, то примеси коагулируют в более крупные хлопья. Крупные частицы, увеличиваясь в размерах и приобретая больший вес, начинают осаждаться под действием силы тяжести.
Фильтрация воды солями алюминия.
Очищенная вода теоретически должна быть чистой, без любых примесей. Но на практике коагулянт содержится в очищенной воде. Чем жестче вода, тем выше его концентрация. Это связано с тем, что в жесткой воде есть большое содержание гидроксида кальция и карбоната натрия, вступающих в реакцию с сульфатом алюминия и осаждающих алюминий в виде нерастворимого студенистого осадка гидроксида алюминия. Для измерения концентрации коагулирующего вещества в воде применяют концентратомеры, или солемеры. Хотя на самом деле концентратомерами называют приборы, определяющие концентрацию кислот и щелочей. Солемеры устанавливают для определения концентрации растворов солей.
Применение в пищевой и фармацевтической промышленности.
Сульфат алюминия известен как алюминиевые квасцы, или добавка E 520.
В пищевом производстве E 520 относится к стабилизаторам. Его получают из природных руд: боксита, алунита, глиноземов. Они подвергаются реакции с серной кислотой высокой концентрации при температурах +100…+250 °C. По окончании процесса получают соль с высоким коэффициентом чистоты.
Свойства стабилизатора:
- порошок или пластинки белого цвета с серым, розовым или голубоватым оттенком;
- без запаха;
- отличается хорошей растворимостью в воде, плохо взаимодействует со спиртом;
- концентрация — не меньше 99,5%.
- вкус добавки — сладковатый и терпкий
- очень гигроскопичное вещество, выветривается на воздухе.
Добавка E 520 отпускается в таре с дополнительными вставками, защищающими содержимое от влаги.
Сульфат алюминия применяют в рыбоперерабатывающей отрасли для сохранения товарного вида рыбы и предупреждения распада волокон. Стабилизатор используется при консервировании плодов и овощей. Добавка используется в кондитерской промышленности в производстве засахаренных и глазированных в сахаре фруктов.
Е520 сохранит продукты свежими и красивыми.
Но основное применение добавки E 520 – для очистки питьевых и сточных вод. Вещество взаимодействует с примесями, которые выпадают в осадок. Он оседает на дно емкостей или водоемов. Вода пропускается поточным методом через систему специальных фильтров, где очищается и осветляется, после чего становится пригодной для питья и применения в производстве.
Другие области применения.
Сульфат алюминия также используется:
- в косметической промышленности, входит в составы декоративной косметики;
- при производстве бытовой химии — в составе антиперспирантов;
- как компонент обезболивающих средств от укусов насекомых;
- в сельском хозяйстве для обработки почв – входит в состав ядов и удобрений для борьбы с вредителями;
- в текстильном производстве входит в состав красителей;
- является компонентом нерастворимых пигментов в печатном деле.
Соли алюминия широко используют в косметической промышленности.
Вещество применяется как гидроизолятор в бетонных конструкциях. Сульфат алюминия используется в производстве огнетушителей.
Им обрабатывают шерстяные ткани для удерживания красящих пигментов. Процесс называется протрава шерстяных волокон. В водном растворе образуется дисперсная гидроокись алюминия, которая поглощается и хорошо удерживается волокнами шерсти. Протравленные волокна приобретают способность поглощать красители за счет адсорбированной ими гидроокиси алюминия.