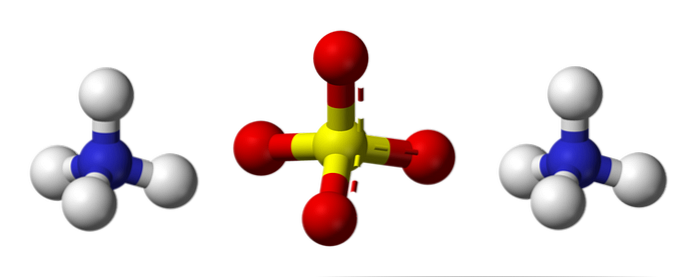
- Сульфа́т аммо́ния (аммоний серноки́слый, лат. ammonium sulphate), (NH4)2SO4 — неорганическое бинарное соединение, аммонийная соль серной кислоты. Это бесцветные прозрачные кристаллы (или белый порошок) без запаха. Получают сульфат аммония действием серной кислоты на раствор аммиака и обменными реакциями с другими солями. Применяется в качестве удобрения, при производстве вискозы, в пищевой промышленности, при очистке белков в биохимии, в качестве добавки при хлорировании водопроводной воды. Токсичность сульфата аммония очень низкая.
Источник: Википедия
Связанные понятия
Хлори́д ка́льция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным.
Карбона́т ка́лия, углеки́слый калий, арх. пота́ш K2CO3 — средняя соль калия и угольной кислоты. Это белое кристаллическое вещество, хорошо растворимое в воде. Малотоксичен, относится к III классу опасности.
Сульфид натрия, устар. сернистый натрий, — сложное неорганическое вещество с химической формулой Na2S.
Гидрокси́д на́трия (лат. Nátrii hydroxídum; другие названия — каустическая сода, едкий натр) — самая распространённая щёлочь, химическая формула NaOH. В год в мире производится и потребляется около 57 млн тонн едкого натра.
Упоминания в литературе
Укрепление осуществляется в два этапа. В начале штукатурка с красочным слоем обрабатывается насыщенным раствором карбоната аммония (NH4)2CO3, который переводит кристаллы гипса в карбонат кальция и растворимый сульфат аммония. При этом во время обработки поверхности грунта гидратом окиси бария происходит перевод оставшихся растворимых сульфатов в инертное нерастворимое состояние – сульфат бария. Укрепление разрушенной микроструктуры красочного слоя и штукатурной основы происходит за счет постепенной карбонизации оставшегося избытка гидроокиси бария в результате реакции с углекислым газом воздуха. Укрепляющий эффект консолиданта постепенно уменьшается от поверхности к основанию.
Сернокислый аммоний (в специализированном магазине его продают под названием «сульфат аммония») содержит примерно 15–20 % азота. Хранят его так же, как и аммиачную селитру. Сульфат аммония обычно применяют на почвах с избыточным увлажнением.
Сульфат аммония или сернокислый аммоний – это ценное азотное удобрение с содержанием азота до 21 %. Удобрение хорошо растворяется в воде, оно связывается в почве при нормальном уровне влажности и слабо вымывается водой из состава почвы. К недостаткам сульфата аммония можно отнести его свойство слеживаться при хранении.
Для того чтобы получить высокие урожаи овощей, следует применять не только органические удобрения, но и минеральные, в первую очередь азотные – аммиачную селитру, сернокислый аммоний, мочевину, кальциевую селитру и т. д. Аммиачная селитра, или нитрат аммония, содержит почти 35 % азота. Она хорошо растворяется в воде. Нитрат аммония можно приобрести в любом специализированном магазине. Чаще всего аммиачную селитру выпускают в виде белых гранул размером до 3 мм. Это удобрение высокоэффективно как при внесении в почву, так и в виде подкормок. Аммиачная селитра может впитывать влагу, поэтому ее нужно хранить в сухом помещении небольшими партиями. Сернокислый аммоний, или сульфат аммония, содержит около 20 % азота. Это удобрение так же хорошо растворяется в воде, как и аммиачная селитра. Азот сульфата аммония слабо вымывается водой из почвы, поэтому его можно применять на почвах с избыточным увлажнением. Не рекомендуется вносить в почву под огурцы, цветную капусту, редис и лук-порей.
Сернокислый аммоний, или сульфат аммония, на 20,5—21 % состоит из азота. Это удобрение хорошо поглощает воду из воздуха и растворяется в воде. Сернокислый аммоний эффективен на почве с избыточным содержанием влаги, так как входящий в него азот хорошо удерживается в почве и слабо вымывается водой. Его относят к кислым удобрениям, поэтому он не так эффективен, как аммиачная селитра. Перед внесением в почву для уменьшения ее кислотности на 1 ц сернокислого аммония добавляют по 120 кг извести. Если требуется внести удобрение в легкие почвы, то используют такое же количество доломитовой муки.
Мочевина. Универсальное азотное удобрение, содержащее 46 % азота. Мелкие кристаллы, хорошо растворимые. Гигроскопичность повышается при высокой влажности воздуха, ухудшается рассеиваемость. Пригодна для всех культур на нейтральных почвах. Подкисляет почву на уровне аммиачной селитры. От внесения мочевины не повышается концентрация поч венного раствора. Незаменима для внекорневых подкормок и при компостировании коры. В последнем случае она быстро гидролизуется с образованием аммиака, который нейтрализует кислотность коры. На песчаной почве азот из мочевины удерживается прочнее, чем из сульфата аммония. Может содержать цинк, медь, кобальт.
После абсорбции загрязняющих веществ облачными каплями, эти вещества могут вступать в химические реакции, подобные реакции двуокиси серы и аммиака, приводящей к образованию сульфата аммония или другие реакции.
После механической фильтрации через специальные фильтры-решетки воде дают отстояться в больших отстойниках, где из нее осаждаются частицы песка и другие мелкие частицы. Для удаления очень мелких частиц воду сначала делают слегка основной, добавляя в нее гидрооксид кальция, а затем добавляют сульфат аммония. В результате химической реакции образуется пористый желатинообразный осадок. Этот осадок медленно осаждается, захватывая с собой взвешенные в воде частицы, благодаря чему из нее удаляются практически все тонкоизмельченные вещества и большая часть бактерий. Затем воду профильтровывают через слой песка. После фильтрации воду иногда разбрызгивают в воздухе, чтобы ускорить окисление растворенных в ней органических веществ.
Для получения высокого урожая в течение периода вегетации растения требуется производить прополку участка и регулярный полив. После завершения периода роста почву удобряют, внося калийную соль (до 0,15 кг/ м2), суперфосфат (до 0,25 кг/ м2) и сульфат аммония (до 0,12 кг/ м2.)
Связанные понятия (продолжение)
Сульфа́т алюми́ния — сложное неорганическое соединение, соль алюминия и серной кислоты с химической формулой Al2(SO4)3. Выглядит как бесцветные кристаллы, может образовывать кристаллогидраты с различным содержанием воды. Применяется при очистке воды, крашении тканей, дублении кож, как реактив в фотографии, для получения квасцов.
Ионообменные смолы — синтетические органические иониты — высокомолекулярные синтетические соединения с трехмерной гелевой и макропористой структурой, которые содержат функциональные группы кислотной или основной природы, способные к реакциям ионного обмена.
Циклогексанон — органическое соединение, алициклический кетон, бесцветная маслянистая жидкость с запахом ацетона и мяты.
Аммофос — азотно-фосфорное концентрированное растворимое удобрение. (Фосфорнокислый аммоний). Содержит около 10—12 % N и 52 % Р2О5. В основном состоит из моноаммонийфосфата NH4H2PO4 и частично диаммонийфосфата (NH4)2HPO4.
Перекристаллиза́ция — метод очистки вещества, основанный на различии растворимости вещества в растворителе при различных температурах (обычно интервал температур от комнатной до температуры кипения растворителя, если растворитель — вода, или до какой-то более высокой температуры). Перекристаллизация подразумевает плохую растворимость вещества в растворителе при низких температурах, и хорошую— при высоких. При нагревании колбы вещество растворяется. После стадии адсорбции примесей (если это необходимо…
Адипи́новая кислота́ (гександио́вая кислота) НООС(СН2)4СООН — двухосновная предельная карбоновая кислота. Обладает всеми химическими свойствами, характерными для карбоновых кислот.
Карбонат аммония, углекислый аммоний, (NH4)2CO3 — аммониевая соль угольной кислоты.
Дихрома́т на́трия (бихромат натрия, натриевый хромпик) — неорганическое химическое соединение, натриевая соль дихромовой кислоты. Существует дигидрат дихромата натрия( Na2Cr2O7·2H2O) и безводная соль.
Сульфи́т на́трия (сернистокислый натрий) — неорганическое соединение, соль натрия и сернистой кислоты…
Диметилбензо́лы или ксило́лы (от др.-греч. ξύλον «дерево») — углеводороды ароматического ряда, состоящие из бензольного кольца и двух метильных групп. Химическая формула — (СН3)2С6Н4. Ксилолы получают при коксовании угля или из нефти путём каталитического риформинга прямогонной бензиновой фракции. Применяются главным образом в качестве растворителей.
Подробнее: Ксилолы
Омыление — гидролиз сложного эфира с образованием спирта и кислоты (или её соли, когда для омыления берут раствор щёлочи)…
Аллиловый спирт (пропен-2-ол-1) — кислородосодержащее органическое вещество, относящееся к классу непредельных (ненасыщенных) спиртов.
Монохлоруксусная кислота CH2ClCOOH — уксусная кислота, в которой один атом водорода метильной группы замещён на атом хлора, бесцветные кристаллы.
Амиловый спирт C5H11OH и его изомеры — предельные одноатомные спирты. Известны все 8 изомерных амиловых спиртов.
У́ксусный ангидри́д (ангидри́д у́ксусной кислоты́), (CH3CO)2O — бесцветная жидкость с резким запахом, растворимая в бензоле, диэтиловом эфире и других органических растворителях. Находит весьма широкое применение в промышленности и органическом синтезе.
Капролактам (гексагидро-2H-азепин-2-он) — циклический амид (лактам) ε-аминокапроновой кислоты, бесцветные кристаллы; Τкип = 262,5 °C, Τпл = 68—69 °C.
Хлорбензол (фенилхлорид) — ароматическое органическое соединение, имеющее формулу C6H5Cl, бесцветная горючая жидкость с характерным запахом.
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Хлораль (трихлорацетальдегид, трихлоруксусный альдегид) — органическое соединение, принадлежащее к классу альдегидов, соответствующее трихлоруксусной кислоте; бесцветная жидкость со специфическим резким запахом, растворим в органических растворителях и нерастворим в воде. Впервые получен в 1832 г. Юстусом Либихом при хлорировании этанола,.
Сульфирование (органических соединений) — введение сульфогруппы (—SO3H) в органические соединения с образованием связи S-С…
Неоргани́ческие (минера́льные) кисло́ты — неорганические вещества, обладающие комплексом физико-химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за исключением щелочных и щёлочноземельных металлов.
Аллилхлори́д или алли́л хло́ристый — хлорорганическое соединение c эмпирической формулой C3H5Cl, систематическое название 3-хлорпропен.
Этилацетат (этиловый эфир уксусной кислоты) СН3−СОО−CH2−CH3 — бесцветная летучая жидкость с резким запахом.
Хлорсульфо́новая кислота, HSO3Cl — монохлорангидрид серной кислоты, бесцветная, дымящая на воздухе и резко пахнущая жидкость.
Метилацета́т (метиловый эфир уксусной кислоты, метиловый эфир этановой кислоты, уксуснометиловый эфир, MeOAc) CH3COOCH3 — органическое вещество класса сложных эфиров.
Глико́ли (дио́лы, двухатомные спирты) — класс органических соединений, содержащих в молекуле две гидроксильные группы. Имеют общую формулу CnH2n(OH)2. Простейшим гликолем является этиленгликоль НО-СН2-СН2-ОН.
Диметиланилин (N,N-диметиланилин) — органическое соединение, принадлежащее классу третичных аминов. Формально является производным аммиака, в котором атомы водорода замещены на фенильный и два метильных радикала.
О́кись этиле́на (этиленокси́д, оксира́н, 1,2-эпоксиэтан) — органическое химическое гетероциклическое вещество, химическая формула C2H4O. При нормальных условиях — бесцветный газ с характерным сладковатым запахом. Производное этилена и представляет собой простейший эпоксид — трёхчленный гетероцикл, в кольцевой молекуле которого содержатся один атом кислорода и два атома углерода.
Диметилами́н (CH3)2NH — вторичный амин, производное аммиака, в молекуле которого два атома водорода замещены метильными радикалами.
Алюмогидрид лития (аланат лития) — неорганическое соединение, комплексный смешанный гидрид лития и алюминия с формулой Li, белые кристаллы.
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
Нитра́т на́трия (азотноки́слый на́трий, натриевая селитра, чилийская селитра, натронная селитра) — натриевая соль азотной кислоты с формулой NaNO3. Бесцветные прозрачные кристаллы с ромбоэдрической или тригональной кристаллической решеткой без запаха. Вкус — резкий солёный. Применяется очень широко и является незаменимым в промышленности соединением.
Ацетат кальция — кальциевая соль уксусной кислоты. Бесцветное кристаллическое или аморфное вещество, хорошо растворимое в воде. Технический моногидрат может быть в форме гранул или некрупных игл. Обладает слабым вкусом и запахом уксуса. Химическая формула — Ca(CH3COO)2, однако чаще получают его моногидрат Ca(CH3COO)2•H2O.
Пентаны — насыщенные ациклические углеводороды класса алканов. Имеют пять атомов углерода в молекуле (от др.-греч. πέντε — пять).
Метилэтилкетон (систематическое наименование: бутано́н) — химическое соединение класса кетонов, второй член гомологического ряда алифатических кетонов. Формула: CH3-C(O)-CH2-CH3. Это бесцветная подвижная легколетучая жидкость с запахом, напоминающим запах ацетона. Обладает всеми химическими свойствами, характерными для алифатических кетонов, используется как растворитель и сырьё в органическом синтезе.
Карбона́т на́трия (кальцинированная сода) — неорганическое соединение, натриевая соль угольной кислоты с химической формулой Na2CO3. Бесцветные кристаллы или белый порошок, хорошо растворимый в воде. В промышленности в основном получают из хлорида натрия по методу Солвэ. Применяют при изготовлении стекла, для производства моющих средств, используют в процессе получения алюминия из бокситов и при очистке нефти.
Хлорид аммония (хлористый аммоний; техническое название — нашаты́рь; NH4Cl) — соль аммония, белый кристаллический слегка гигроскопичный порошок без запаха.
Алифатические амины — разновидность органических соединений, принадлежащих к классу аминов, которая отличается содержанием алифатических заместителей у атома азота. Впервые простейшие алифатические амины (метиламины и этиламины) синтезировал Шарль Вюрц в 1849 году. Для их получения он гидролизовал соответствующие алкилизоцианаты, триалкилцианураты и алкилмочевины. Фундаментальное же изучение свойств, структуры и методов синтеза алифатических аминов провёл Август Вильгельм Гофман. Он же предложил…
Сульфа́т ка́льция (CaSO4) — неорганическое соединение, кальциевая соль серной кислоты.
Хлорат калия (бертолетова соль, калий хлорноватокислый) — KClO3, калиевая соль хлорноватой кислоты (HClO3).
Гидрокси́д алюми́ния — вещество с формулой Al(OH)3 (а также H3AlO3) — соединение оксида алюминия с водой. Белое студенистое вещество, плохо растворимое в воде, обладает амфотерными свойствами.
Хроматы — соли хромовой кислоты H2CrO4. Устойчивы в нейтральной и щелочной среде, в кислой среде обратимо переходят в дихроматы — соли дихромовой кислоты H2Cr2O7.
Тетрабора́т на́трия («бура́», «боракс» (от лат. borax)) — неорганическое соединение, натриевая соль борной кислоты с химической формулой Na2B4O7, наиболее распространённое и используемое соединение бора, образует несколько кристаллогидратов, широко применяется в промышленности.
Аминосульфоновая кислота (Сульфаминовая кислота, моноамид серной кислоты, амидосерная кислота) — кислота, формула которой NH2SO2OH (также NH2SO3H). Производные этой кислоты называют сульфаматами.
Сульфокислоты (сульфоновые кислоты) — органические соединения общей формулы RSO3H или R-SO2OH, где R — органический радикал. Сульфокислоты рассматриваются как органические соединения, замещенные по углероду сульфогруппой -SO3H .
сульфат аммония Это тройная и аммиачная неорганическая соль серной кислоты. Его химическая формула (NH4)2SW4. Поэтому стехиометрические пропорции говорят о том, что для каждого сульфат-аниона есть два катиона аммония, взаимодействующих с ним. Это позволяет нейтральность соли ((+1) + 2 + (-2)).
Его номенклатура обусловлена тем, что это соль, полученная из H2SW4, изменив суффикс «uric» на «ato». Таким образом, два начальных протона заменены на NH4+, продукт реакции с аммиаком (NH3). Тогда химическое уравнение для его синтеза имеет вид: 2 NH3 + H2SW4 => (NH4)2SW4
Сульфат аммония является хранилищем азота и серы, которые необходимы в химии почв и удобрений.
индекс
- 1 Химическая структура
- 2 Физические и химические свойства
- 2.1 Молекулярный вес
- 2.2 Внешний вид
- 2.3 Запах
- 2.4 Точка плавления
- 2.5 Растворимость
- 2.6 Плотность
- 2.7 Давление пара
- 2.8 Температура вспышки
- 2,9 рН
- 2.10 Стабильность
- 2.11 Разложение
- 2.12 Коррозия
- 3 использования
- 3.1 В сельском хозяйстве
- 3.2 В качестве аналитического реагента
- 3.3 В осаждении и выделении белков
- 3.4 В отрасли
- 3.5 Другое использование
- 4 Ссылки
Химическая структура
Верхнее изображение иллюстрирует молекулярную геометрию ионов NH4+ и так42-. Красные сферы соответствуют атомам кислорода, белые сферы соответствуют атомам водорода, синие сферы — атому азота, а желтые сферы — атому серы..
Оба иона можно рассматривать как два тетраэдра, и, таким образом, они имеют три единицы, которые взаимодействуют друг с другом, образуя ромбическую кристаллическую структуру. Сульфат-анион является SO42- и может пожертвовать или принять четыре водородные связи, так же, как катион NH4+.
Физико-химические свойства
Молекулярный вес
132 134 г / моль.
Внешний вид
Сплошной белый. Орторомбические белые или коричневые кристаллы, в зависимости от уровня примесей.
запах
туалет.
Точка плавления
280 ºC. Эта температура плавления, низкая по сравнению с другими ионными соединениями, обусловлена тем фактом, что это соль с одновалентными катионами (+1) и разнородными ионами по своим размерам, в результате чего твердое вещество имеет низкую кристаллическую ретикулярную энергию.
растворимость
76,4 г / 100 г воды при 25 ºC. Это сродство к воде обусловлено большой способностью ее молекул сольватировать ионы аммония. С другой стороны, он нерастворим в ацетоне и спирте; то есть в растворителях менее полярных, чем вода.
плотность
1,77 г / см3 при 25 ºC.
Давление пара
1871 кПа при 20 ºC.
Точка воспламенения
26 ºC.
pH
5,0-6,0 (25 ° С, 1 М раствор). Слабокислотный рН обусловлен гидролизом NH4+ в воде, производя H3О+ в низких концентрациях.
стабильность
Стабильно в подходящих условиях окружающей среды. При контакте с сильными окислителями может загореться.
разложение
Он начинает разлагаться при 150 ºC, выделяя токсичные пары оксида серы, оксида азота и аммония.
коррозия
Не атакует железо или алюминий.
приложений
В сельском хозяйстве
— Сульфат аммония используется в качестве удобрения на щелочных почвах. Соль аммония имеет 21% азота и 24% серы в своем составе. Однако существуют соединения, которые обеспечивают большее количество азота, чем сульфат аммония; Преимуществом последнего является его высокая концентрация серы.
— Сера необходима для синтеза белков, поскольку некоторые аминокислоты, такие как цистин, метионин и цистеин, содержат серу. По этим причинам сульфат аммония продолжает оставаться одним из наиболее важных удобрений..
— Используется в посевах пшеницы, кукурузы, риса, хлопка, картофеля, конопли и фруктовых деревьев..
— Низкий pH щелочных почв из-за их вклада в процесс нитрификации, осуществляемый микробами. Аммоний (NH) используется4+) для производства нитрата (НЕТ3—) и выпустить H+: 2NH4+ + 4О2 => 2НЕТ3— + 2H2O + 4H+. Увеличение концентрации водорода снижает рН щелочных почв и позволяет больше использовать.
— Помимо использования в качестве удобрения, сульфат аммония действует как вспомогательное средство для растворимых инсектицидов, гербицидов и фунгицидов, которые распыляются на сельскохозяйственные культуры..
— Сульфат способен улавливать ионы, присутствующие в почве и в поливной воде, которые необходимы для жизни определенных патогенных микроорганизмов. Среди ионов, которые захватывает сульфат аммония, Ca2+, Mg2+, вера2+ и вера3+. Это действие усиливает микробицидное действие указанных агентов..
В качестве аналитического реагента
Сульфат аммония действует как осаждающий агент в электрохимическом анализе, в микробиологических питательных средах и при получении солей аммония.
В осаждении и выделении белков
Сульфат аммония используется для выделения и очистки белков, особенно белков плазмы. Количество сульфата аммония добавляют в плазму до определенной концентрации; таким образом, осаждение группы белков вызвано.
Осадок собирают центрифугированием, и к супернатанту добавляют дополнительное количество сульфата аммония, и при новой концентрации происходит осаждение другой группы белков..
Повторение предыдущего процесса в последовательной форме позволяет в результате получать разные фракции белков плазмы..
До появления новых технологий молекулярной биологии эта процедура позволила выделить белки плазмы, имеющие большое значение в медицине, например: иммуноглобулины, факторы свертывания крови и т. Д..
В промышленности
Сульфат аммония действует, чтобы замедлить начало пожара в текстильной промышленности. Используется в качестве добавки в гальванической промышленности. Он также используется в производстве перекиси водорода, хлорида аммония и т. Д..
Другое использование
— Сульфат аммония используется в качестве регулирующего агента осмотического давления и в качестве осадителя соли.
— В форме лаурилсульфата аммония поверхностное натяжение воды уменьшается, что позволяет отделить загрязняющие вещества за счет повышения жесткости воды.
— Это антикоррозионный агент.
— Используется в качестве пищевой добавки, которая регулирует кислотность в мучном тесте и хлебе..
ссылки
- МОРГ ОЭСР. (Октябрь 2004 г.) Сульфат аммония. [PDF]. Получено 27 апреля 2018 г. с сайта inchem.org
- Мозаичная Компания. (2018). Сульфат аммония. Получено 27 апреля 2018 г. из: cropnutrition.com
- Wikipedia. (2018). Сульфат аммония. Получено 27 апреля 2018 г. с сайта en.wikipedia.org
- PubChem. (2018). Сульфат аммония. Получено 27 апреля 2018 г. из: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 июля 2015 г.) [Рисунок]. Получено 27 апреля 2018 г. с сайта: flickr.com
- Паула Папп (22 февраля 2017 г.) Применение и использование сульфата аммония. Получено 27 апреля 2018 г. из: business.com
В группе азотных минеральных удобрений сульфат аммония держится особняком. В нем, единственном, помимо азота, содержится сера, улучшающая вкусовые характеристики фруктов и овощей, ускоряющая вегетативное развитие растений.
Аммонийная соль нашла широкое применение как предпосевной тук, при этом благодаря простоте использования, отсутствию токсичных свойств, ее используют как в крупных промышленных хозяйствах, так и на обычных дачных участках.
Что это такое: состав удобрения и свойства
Аммонийная соль серной кислоты (или сульфат аммония, или аммоний сернокислый) относится к аммонийным разновидностям азотной группы минеральных туков. Соединение бинарное, в составе:
- азот – 21%
- сера – 24%.

Представляет собой белый порошок или бесцветные прозрачные кристаллики, не имеющие запаха. Как и другие виды удобрений этого типа, содержат азот в форме катиона аммония (формула NH4+). При воздействии сильных окислителей происходит реакция окисления, при нагревании (свыше +100ºC) происходит разложение с выделением аммиака.

Размеры основной части фракций – не более 0,5 мм. Вещество рассыпчатое, растворимое в воде с образование незначительного осадка, не едкое, не токсичное. Показатели гигроскопичности невысокие, при взаимодействии с солями ряда металлов образует двойные соли, при хранении не слеживается, не комкуется.
Рекомендовано применять как азотно-серную минеральную добавку на всех этапах выращивания культур. Не содержит нитратов, подходит для всех овощных, плодовых и ягодных растений. Пожаробезопасно, не горюче.
Преимущества и недостатки сульфата аммония
Сернокислый аммоний не имеет каких-то противопоказаний для использования в качестве удобрения, подходит для подкормок в любых климатических условиях. Единственное – требуется точно соблюдать пропорции при внесении тука, учитывать характеристики грунта, потребности растений в веществах.

На заметку! Реагент применяется в качестве добавки при хлорировании водопроводной воды.
Среди «плюсов» удобрения:
- оптимальное соотношение компонентов, необходимых для роста и развития растений;
- одновременно обеспечивает культуры азотом и серой;
- сера содержится в хорошо усваиваемой растениями форме – соли;
- доступность;
- невысокая стоимость (до 40 рублей за килограмм гранулированного тука);
- простота применения;
- хорошая растворимость в воде;
- подходит для использования в баковых смесях с другими агрохимикатами;
- при внесении отсутствует кумулятивный эффект (нет накопления нитратов в плодах и овощах);
- возможность вносить в сухом виде (при вспашке, при перекопке грунта), а также в виде питательных растворов (поливы, обработка по зеленым побегам и листьям).
Применение на огороде весной подкормок с сульфатом аммония способствует
- улучшению вкусовых характеристик овощей, ягод, фруктов;
- увеличению сроков хранения урожая;
- предотвращению дефицита питательных веществ.

Это одно из лучших стартовых удобрений, дающих отличный толчок в росте и развитии растений. Известно, что при дефиците серы резко замедляются процессы фотосинтеза, тормозится рост культур.
При внесении сернокислого аммония удается избежать таких проблем, увеличить устойчивость посадок к перепадам температур, болезням. Они лучше противостоят воздействию неблагоприятных погодных факторов, радиации, засухе. В отличие от аммиачной селитры, потери азота при применении сульфата меньше.
Инструкция по применению на различных почвах
Так как тук относится к аммонийной разновидности азотных добавок, то при внесении в грунт он слегка подкисляет его. Эту особенности необходимо учитывать при использовании удобрения на почвах с высоким показателем pH. Чтобы отрегулировать возможные реакции на кислых грунтах, рекомендуется заранее нейтрализовать аммоний сернокислый, добавив к нему известь пушонку (пропорции 1:1,3) или известковать участок (см. фото).

На плодородных грунтах с высоким содержанием гумуса повышение кислотности незначительное, при этом явление наблюдается спустя 10-12 лет после внесения. Поэтому на таких землях разрешено применять удобрение без дополнительных компонентов. На легких песчаных и супесчаных грунтах при внесении сульфата для лучшего усвоения требуется обязательное увлажнение земель.
Отлично зарекомендовал себя тук на щелочных грунтах. Он окисляет землю, способствует насыщению почвы такими важными компонентами как сера, озон, благотворно влияющими на рост культур.
Если грамотно, соблюдая сроки и пропорции, вносить минеральное вещество на таких участках, то обеспечена хорошая урожайность плодов и овощей, при этом в них не накапливаются опасные токсины, радионуклиды, нитраты. Специалисты рекомендуют вносить удобрение на загрязненных территориях, когда приходится выращивать растения вблизи промышленных объектов.
Сроки внесения
Соль эффективна при внесении весной: при вспашке или перекопке почвы на участках. Применяют в сухом виде (порошок, кристаллы, гранулы) с обязательной заделкой в землю.

При попадании в грунт вещество моментально растворяется, а одно из соединений – ион аммония становится малоподвижным. В таком состоянии необходимый для питания растений компонент не вымывается из грунта, постепенно усваиваясь овощными и плодовыми культурами. Удобрение используют в комплексе с калийными и фосфорными добавками.
Также тук применяют в виде водных питательных растворов на всем протяжении вегетации. Обязательно выдерживают интервалы между подкормками – не менее 12-15 дней. Достаточно 2-3 раза подкормить посадки приготовленным раствором. За пару недель до предполагаемого сбора урожая подкормки прекращают.
Нормы для различных культур
Азот необходим всем растениям, точно так же им нужна сера. Но агрономы различают культуры, особо требовательные к наличию серы в подкормках, а также те, которые не особо остро реагируют на дефицит элемента. Эти показатели учитывают при использовании туков, так как в одних случаях показано применение сульфата аммония (из-за серы и аммонийной формы азота), в других лучше вносить азотнокислый аммоний (нитрат).
От дефицита серы больше всего страдают следующие культуры:
- гречиха;
- редька;
- все представители семейства крестоцветных;
- рапс.

Также аммоний рекомендован для подкормок картофеля, ячменя, пшеницы, кукурузы. Эти растения предпочитают аммонийную форму азота нитратной.
Стандартные нормы внесения: около 24-40 граммов сухого вещества на один квадратный метр посадок. Но для различных культур применяют свои дозировки, учитывая потребности растений, особенности почвы (структуру, pH, показатели загрязненности).
В таблице представлены примерные нормы удобрения для растений:
| Культура | Сроки | Способы внесения и дозировки |
| Корнеплоды (свекла, морковь) | В сухом виде (перед посевом при подготовке грядок). В жидком – поливы на всех стадиях, в сезон – 2-3 подкормки | Сухие гранулы: 20-40 г/м2, только по влажной почве. Полив под корень: раствор на 20 литров теплой воды размешивают 20 граммов тука |
| Томаты, сладкий перчик, баклажаны, огурцы | Перед высадкой рассады, позже поливы и обработки по листочкам (2-3 раза) | Перед посадкой по 15 граммов сухого тука на каждый квадратный метр Раствор: на 20 литров теплой воды размешивают 15-20 граммов вещества. Опрыскивание проводят только раз, полив – 2-3 раза |
| Капуста | При подготовке участка под посадку, позже поливы (1-2 раза до формирования головок) | Заделка в грунт – по 20 гм2, раствор: на 20 литров воды 50-60 граммов |
| Плодовые деревья (груша, яблоня) | При посадке саженцев, также вносят в сезоне (1-2 раза) в приствольный круг (в гранулах) | При посадке в лунки добавляют по 1-2 столовых ложки тука, в текущих подкормках – по 20-25 г под взрослое дерево |
| Картофель | При подготовке участка под посадку, позже поливы (1-2 раза по кустам) | При перекопке – по 20-40 гм2, полив: на 20 литров воды 30-40 граммов |
| Клубника (садовая голубика, клюква) | Перед высадкой кустиков | В сухом виде по 25г/м2 |
| Чеснок, лук, зелень | При подготовке участка под посадку, позже поливы (1-2 раза), рассыпание сухого удобрения в междурядьях | В сухом виде – 20 г на каждый квадратный метр, жидкие подкормки: 20 г на 20 литров воды. Допускается подкормить зеленные культуры трижды за сезон. Зелень на срезку также подкармливают, но обязательно выдерживают срок перед срезкой не менее двух недель |
При перекопке удобрение вносят по влажной почве (после дождя или полива). Нельзя допускать передозировки тука, иначе легко навредить культурам.
Отзывы
Ираида, Городец
Регулярно вношу это удобрение при перекопке участка. Хорошо растет картошка, нет проблем с томатами, баклажанами. В нашем непредсказуемом климате то жара, то дожди зальют посадки, поэтому надо правильно применять препараты. Сульфат аммония недорогое удобрение и полезное. Это по себе знаю, когда столько трудов вкладываешь, то и результата ждешь.
Геннадий, Самарская область
Очень аккуратно отношусь к химикатам, но сульфат аммония считаю одной из лучших подкормок. Вношу под картофель, поливаю клубнику, ягодные кусты. Томаты не пробовал поливать, но читал в дачной газете, что также эффект хороший. Пока считаю, что достаточно, если надо будет, применю в теплице и в парнике. Стоящее удобрение!
Химическая формула сульфата аммония
Формула сульфата аммония (NH₄)₂SO₄
Неорганическое бинарное соединение, аммонийная соль серной кислоты. Это бесцветные прозрачные кристаллы без запаха. Получают сульфат аммония действием серной кислоты на раствор аммиака и обменными реакциями с другими солями. Сульфат аммония применяется в качестве удобрения, при производстве вискозы, в пищевой промышленности, при очистке белков в биохимии, в качестве добавки при хлорировании водопроводной воды. Токсичность вещества очень низкая.
Аммонийная форма азота в сульфате аммония дает продолжительное действие при минимальной потере основного вещества. Наличие серы выделяет данное удобрение из всех как единственное среди азотных удобрений. Особенно хорошие результаты обеспечивает внесение сульфата аммония под зерновые, рапс, картофель и овощи, в т.ч. сахарную свеклу.
Большая часть хозяйств получает ощутимые прибавки урожайности и качества, но немногим удается достичь максимального содержания белка в зерне пшеницы — сульфат аммония позволяет это сделать.
Сульфат аммония в первую очередь рекомендуется применять для следующих культур:
- требовательных к сере (гречиха, рапс, озимая и яровая пшеница, кукуруза, подсолнечник, капуста и другие крестоцветные культуры);
- предпочитающих аммонийную форму азота нитратной (картофель, сахарная свекла, кормовые культуры);
- лучше произрастающих при слабокислой реакции почвенного раствора (картофель, лен, чай, подсолнечник, морковь, помидоры, щавель, петрушка, репа, редька, тыква, кабачки, редис, крыжовник, малина).
Вносить удобрение сульфат аммония лучше всего весной и осенью, что дает возможность равномерного распределения удобрения по полю. Подкормки сельскохозяйственных культур сульфатом аммония также эффективны. При этом необходима внимательная работа по регулировке машин для внесения удобрений, а также непосредственно при проведении подкормок. Кроме того, сульфат аммония может добавляться в раствор жидких азотных удобрений.
В системе удобрения применение сульфата аммония рекомендуется (нормы внесения):
- при возделывании ярового рапса: 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) под предпосевную культивацию в сочетании с применением фосфорных и калийных удобрений + 30-40 кг/га сульфата аммония (143-190 кг/га в физическом весе) в стадию бутонизации + 10 кг/га в физическом весе в виде совместной некорневой подкормки с микроэлементами (бор, медь, марганец) в конце бутонизации;
- при возделывании озимого рапса: 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) весной в начале возобновления вегетации + 30-40 кг/га (143-190 кг/га в физическом весе) в стадию бутонизации + 10 кг/га в физическом весе в виде совместной некорневой подкормки с микроэлементами (бор, медь, марганец) в конце бутонизации;
- при возделывании гречихи: 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) под предпосевную культивацию в сочетании с фосфорными и калийными удобрениями.
Порядка 80% всех отечественных пашен имеет недостаточное содержание серы. Это вызывает проблемы с синтезом белков, сахаров и жиров. Малое количество серы при использовании удобрений на азотной основе, становится причиной скапливания в почве азота, имеющего вид нитратов. Помимо прочего это:
- улучшает стойкость растений к чрезмерно малым и высоким температурам, неблагоприятным для их развития;
- обеспечивает культурам более действенное противостояние к радиации и засушливости;
- нехватка серы, вызывает снижение уровня фотосинтеза примерно на 40%;
- недостаток серы активизирует распад белков и замедляет рост растений.
- при возделывании кукурузы: 100-120 кг/га сульфата аммония д.в. (476-571 ц/га в физическом весе) под предпосевную культивацию на фоне органических, фосфорных и калийных удобрений + 30-50 кг/га сульфата аммония д.в. (143-238 кг/га в физическом весе) в стадии 6-8 настоящих листьев под междурядное рыхление;
- при возделывании яровых зерновых культур (пшеница, тритикале, ячмень, овес, просо): 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) под предпосевную культивацию в сочетании с фосфорными и калийными удобрениями;
- для подкормок озимых зерновых культур: 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) весной в начале возобновления вегетации + 20-40 кг/га сульфата аммония д.в. (95-191 кг/га в физическом весе) в стадии 1-го узла;
- для ранневесенней подкормки озимых зерновых культур: N60-70 в форме КАС + 15 кг/га сульфата аммония в раствор;
- для поздней некорневой подкормки озимой и яровой пшеницы в начале колошения – 10 кг/га сульфата аммония д.в. (48 кг/га в физическом весе) или 10 кг/га сульфата аммония в физическом весе в виде совместной некорневой подкормки с медью и марганцем в стадии последнего листа;
- при возделывании картофеля: 80-100 кг/га сульфата аммония д.в. (381-476 кг/га в физическом весе) под предпосадочную культивацию на фоне органических, фосфорных и калийных удобрений;
- при возделывании сахарной свеклы: 100-120 кг/га сульфата аммония д.в. (476-571 кг/га в физическом весе) под предпосевную культивацию на фоне органических, фосфорных и калийных удобрений + 30-50 кг/га сульфата аммония д.в. (143-238 кг/га в физическом весе) в стадии 4-6 настоящих листьев под первое междурядное рыхление;
Сульфат аммония может быть гранулированным или кристаллическим. Внедрение гранулирования позволяет исключить неравномерность распределения препарата в почве. При размере товарной фракции в 2-5 мм ее массовая доля составляет около 95%, до 1 мм – в пределах 1%. Прочность статическая у гранул на порядок выше, нежели у аммиачной селитры, средний показатель равен 12-14 кгс/см2, динамическая достигает 90-95%. Значение рассыпчатости составляет 100%.
- при возделывании кормовых корнеплодов: кормовая свекла – 100-120 кг/га сульфата аммония д.в. (476-571 ц/га в физическом весе) под предпосевную культивацию на фоне органических, фосфорных и калийных удобрений + 30-60 кг/га сульфата аммония д.в. (143-286 кг/га в физическом весе) в стадии 4-8 настоящих листьев под первое междурядное рыхление; кормовая морковь, турнепс, брюква – 80-90 кг/га сульфата аммония д.в. (381-429 кг/га в физическом весе) под предпосевную культивацию на фоне органических, фосфорных и калийных удобрений + 20-40 кг/га сульфата аммония д.в. (95-191 кг/га в физическом весе) под первое междурядное рыхление;
- при возделывании кормовых крестоцветных культур (сурепица, горчица, редька масличная): 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) под предпосевную культивацию в сочетании с фосфорными и калийными удобрениями;
- на сенокосах и пастбищах: 60-80 кг/га сульфата аммония д.в. (286-381 кг/га в физическом весе) весной в начале возобновления вегетации и после каждого укоса (стравливания);
- при возделывании однолетних трав: бобово-злаковые травосмеси – 50-60 кг/га сульфата аммония д.в. (238-286 кг/га в физическом весе), злаковые травы – 70-90 кг/га сульфата аммония д.в. (333-429 кг/га в физическом весе) под предпосевную культивацию на фоне фосфорных и калийных удобрений;
- при возделывании многолетних трав: бобово-злаковые травосмеси – 50-60 кг/га сульфата аммония д.в. (238-286 кг/га в физическом весе), злаковые травы – 60-70 кг/га сульфата аммония д.в. (286-333 кг/га в физическом весе) весной в начале возобновления вегетации и после каждого укоса;
- в овощеводстве (в физическом весе): капуста белокочанная – 60 г/м2, капуста цветная – 45 г/м2, капуста брокколи – 45 г/м2, капуста краснокочанная – 75 г/м2, капуста брюссельская – 60 г/м2, капуста кольраби – 40 г/м2, редис – 30 г/м2, редька – 35 г/м2, репа – 25 г/м2, щавель – 40 г/м2; морковь – 30-40 г/м2, петрушка – 30-40 г/м2, тыква и кабачки – 30-40 г/м2, томаты (помидоры) – 30-45 г/м2, другие овощные культуры – 30-50 г/м2;
- в плодоводстве (в физическом весе): крыжовник и малина – 50-60 г/м2, другие плодовые и ягодные культуры – 40-50 г/м2.
Таблица 1 — Влияние удобрений на урожайность и качество зерна ячменя
| Варианты опыта | Урожайность, ц/га | Прибавка | Сырой протеин, % | Натура, г/л | Масса 1000 зёрен, г |
| ц/га | % | ||||
| к контролю | к фону | к контролю | к фону | ||
| 1. Контроль | 19,5 | ? | ? | ||
| 2. Р40К40 | 20,4 | 0,9 | ? | 4,6 | ? |
| 3. Р40К40N60 ам. селитра | 25,6 | 6,1 | 5,2 | 31,3 | 25,5 |
| 4. Р40К40N60 сульфат аммония | 27,3 | 7,8 | 6,9 | 40,0 | 38,2 |
| НСР095 SХ % | 1,6 2,1 |
Как видно из представленных данных (таблица 1), естественным плодородием чернозёма выщелоченного обеспечивается низкая урожайность ячменя (19,5 ц/га). Фосфорно-калийные удобрения (вариант 2) оказали слабое влияние на урожайность ячменя, прибавка составила 0,9 ц/га, что находится в пределах ошибки опыта. Добавление к фосфорно-калийному удобрению азота способствовало значительному росту урожайности, прибавка составила 6,1?7,8 ц/га к контролю и 5,2?6,9 ц/га к фону. При этом наибольшая прибавка отмечается на варианте с внесением сульфата аммония, разница с прибавкой от аммиачной селитры математически доказуема (1,7 ц/га). Это, по-видимому, связано с наличием в составе сульфата аммония серы, которая в чернозёмных почвах в настоящее время часто является лимитирующим фактором роста урожайности.
Азотные удобрения, так же оказали влияние и на качественные показатели зерна ячменя. Увеличилось содержание сырого протеина, натура и масса 1000 зёрен. При этом так же отмечается тенденция к преимуществу сульфата аммония по сравнению с аммиачной селитрой.
Таким образом, на чернозёме выщелоченном из азотных удобрений под ячмень предпочтительнее применение сульфата аммония, как обеспечивающего более высокую урожайность и лучшие показатели качества зерна.
Оптовые поставки сульфата аммония

Наше предприятие — Российский производитель сульфата аммония, в том числе и других химических субстанций любых видов, фракций и объема. Наш завод оборудован самым современным оборудованием, есть собственная доставка. Есть возможность отгрузки самых крупных партий товаров доставляем по железной дороге.
Предлагаем приобрести сульфат аммония в мешках, от 1 т. с доставкой по всей России, СНГ и странам дальнего зарубежья. Наша продукция успешно поставляется во все регионы России, такие как: Алтайский край, Ростовская область, Воронеж, Башкортостан, Краснодарский край, Белгородскую область, Тамбовскую область, Саратов, Московскую область, Курс, Оренбург, Дагестан, Ленинградскую область, Липецк, Омск, Ставропольский край и другие.
Свойства вещества сульфата аммония
 Продукт содержит 21% азота (N) и 24% серы (S)
Продукт содержит 21% азота (N) и 24% серы (S)
Химическая формула сульфата аммония — (NH4)2SO4. В состав входят следующие вещества — азот (21%) и сера (24%). на вид представляет собой белые прозрачные кристаллы.
Сульфат аммония, (NH4)2SO4, имеет второе название – аммонийная соль серной кислоты и представляет собой прозрачные кристаллы, либо белые гранулы, без запаха с кисловатым вкусом. Вещество хорошо растворяется в воде, распадается при нагревании. В чистом виде сульфат аммония в природе не встречается.
Видео поясняющее о пользе применения сульфата аммония на сельхоз угодьях. Рассказывает профессор Николай Мязин
Таблица с общими свойствами вещества сульфата аммония
| Традиционные названия | аммоний сернокислый |
|---|---|
| Хим. формула | (NH4)2SO4 |
| Рац. формула | H8N2O4S |
| Состояние | твёрдое |
| Молярная масса | 132,14052 г/моль |
| Плотность | 1,769 г/см³ (20 °C) |
| Т. плав. | 235-280 °C |
| 218 °C | |
| Мол. теплоёмк. | 187,4 Дж/(моль·К) |
| Энтальпия образования | −1180,26 кДж/моль |
| Растворимость в воде | 75,4 г/100 г (20 °C) |
| ГОСТ | ГОСТ 9097-82 ГОСТ 3967-78 ГОСТ 10873-73 ГОСТ Р 51520-99 |
| Рег. номер CAS | 7783-20-2 |
| PubChem | 24538 |
| Рег. номер EINECS | 231-984-1 |
| SMILES | O=S(=O)(O)O.N.N |
| InChI | 1S/2H3N.H2O4S/c;;1-5(2,3)4/h2*1H3;(H2,1,2,3,4) BFNBIHQBYMNNAN-UHFFFAOYSA-N |
| Кодекс Алиментариус | E517 |
| ChEBI | 62946 |
| ChemSpider | 22944 |
| ЛД50 | 2840 (крысы; орально) |
 Наш завод предоставляет гарантию 1 год на соответствие требованиям предъявляемым при хранении вещества в рекомендуемых условиях, при правильной транспортировке и хранении.
Наш завод предоставляет гарантию 1 год на соответствие требованиям предъявляемым при хранении вещества в рекомендуемых условиях, при правильной транспортировке и хранении.
Так как сульфат аммония требует к себе особого внимания при транспортировке, то нужно отнестись к его упаковке с особой тщательностью. Вообще, разработаны ГОСТы по его упаковке, и мы конечно, стараемся их соблюдать. Поэтому на нашем химическом заводе готовое вещество упаковывается в прочные полиэтиленовые мешки, которые в свою очередь завязываются двойным узлом нитью или даже запаиваются. На выбор покупателя, так же возможна упаковка этого вещества в бумажные пяти-шести-слойные мешки.
В лабораторных условиях, вещество можно получить если соединить концентрированную серную кислоту и концентрированный раствор аммиака.
2NH3+ H2SO4 → (NН4)2 SO4
В химической промышленности основными способами получения сульфата аммония являются:
Процесс нейтрализации серной кислоты синтетическим аммиаком;
Соединение аммиака из газа коксовых печей с серной кислотой;
Обработкой гипса растворами карбоната аммония;
Переработкой отходов, остающихся после производства капролактама.
Это конечно не полный перечень, имеются и другие способы производства, например из газов, производящиеся на электростанции, который по совместительству относится и к деятельности сернокислотных заводов. А именно, это происходит следующим образом: в горячие газы вводят газообразный аммиак, связывающий в газе окислы серы в различные соли аммония, в том числе и в сульфат аммония.
Промышленные объемы производства
При производстве сульфата аммония в промышленных объемах, чаше всего пользуются обработкой измельченного гипса жидкостными растворами карбоната аммония. Существует два способа обработки гипса для получения сульфата аммония. Жидкостный и газовый. Наибольшее распространение имеет жидкостный способ. При нем измельченный гипс, частями смешивается с раствором карбоната аммония. В результате реакции образуются твердые кристаллы СаСОз которые легко отфильтровываются, а оставшийся раствор сульфата аммония отправляется на выпаривание.
Газовый метод имеет ряд недостатков. Получаемые кристаллы СаСОз имеют игольчатую форму и хуже отфильтровываются. Помимо этого, требуется холодильное оборудование для охлаждения пульпы.
Вещество получается и как побочный продукт очистки дымовых газов электростанций и заводов по производству серной кислоты. Введение в дымовые газы газообразного аммиака приводит к образованию различных солей аммония, в том числе и сульфата.

В сельском хозяйстве
Самыми крупными потребителями сульфата аммония являются сельхозпроизводители, использующие его в качестве удобрения на полях. Высокое содержание азота (21%) и серы (24%) делает вещество универсальным удобрением практически на всех видах почвы (кроме закисленных), а также во всех климатических зонах.
Способность этого вещества хорошо растворяться в воде позволяет вносить его как в разведенном виде через поливальные установки, так и в гранулированном в период перепашки земли или даже в качестве подкормки после всходов растений.
В качестве удобрения в любых климатических условиях, наиболее благоприятно внесение сульфата аммония весной, так как большое количество азота, входящего в его состав, стимулирует рост и развитие культур. Аммонийный азот сульфата аммония легко усваивается растениями. Сера необходима для питания всех культур, так как входит в состав некоторых синтезируемых растениями незаменимых аминокислот.
Благотворное влияние удобрения на рост и развитие растений сказывается не только благодаря содержанию азота, но и сере, которая участвует в формировании белков и аминокислот. Многие исследователи указывают на значительное сокращение свободной серы в составе почв практически во всех регионах России. Это может привести к резкому сокращению урожайности основных сельскохозяйственных культур. Использование сульфата аммония способно восполнить недостачу серы.
Минеральные удобрения на основе этого вещества довольно универсальны и подходят почти ко всем типам почв, причём его эффективность доказана при использовании во всех климатических поясах. Единственное что не рекомендовано так это применение сульфата аммония на кислых почвах, так как это может привести к их закислению.
Это удобрение можно использовать как на фермерских угодьях так и на домашнем огороде, не говоря уже о приусадебном участке. Всё это благодаря тому что компоненты вещества находится в форме ионов, это в свою очередь, позволяет достичь максимального усвоения его растениями.
Немаловажную роль играет и экономическая составляющая использования сульфата аммония в качестве удобрения. Стоимость внесенного в почву азота практически в два раза получается дешевле чем при внесении его в виде аммиачной селитры.
На водоочистных сооружениях
Еще одной сферой применения сульфата аммония, является использование его в качестве связующего элемента при хлорировании воды на водораспределительных станциях. Свободный хлор добавляемый в воду вступает во взаимодействие с сульфатом аммония, что уменьшает его концентрацию. Это делает воду не только более безопасной для использования, но и предотвращает разрушение водопроводных труб.
Пищевая промышленность
В пищевпроме, сульфат аммония известен как эмульгатор Е 517 и используется в качестве пищевой добавки в хлебобулочных изделиях. Введение эмульгатора Е517 в тесто благотворно влияет на рост дрожжевых бактерий, что придает выпечке более пышные формы. Лучшим ростом дрожжевых бактерий при использовании вещества пользуются и производители спиртов, добавляя Е517 в свеклосахарную мелиссу для дополнительного кормления дрожжей.
Медицина
В медицине, вещество используется в составе препаратов, повышающих свертываемость крови.
Выводы
Итак, мы разобрались что сульфат аммония может служить в качестве отличного минерального удобрения, но какие именно культуры можно обрабатывать его помощью? Список довольно широк: картофель и др. овощи, редька, кукуруза, подсолнух, щавель, редис, рапс, пшеница, гречиха.
Меры предосторожности при обращении с веществом
Сульфат аммония сегодня признан безопасным для человека и используется иногда даже в виде пищевой добавки в России, на Украине и в странах ЕС, не следует пренебрегать элементарными правилами безопасности при контакте с ним. Иногда, он используется так же и в качестве заменителя соли, в этом случае о сульфате аммония говорят как о пищевой добавке Е517. Ну конечно же везде есть допустимые дозы, так и здесь, если после контакта с веществом, его проглатывании или попадании на кожу и глаза, вы почувствовали какое либо раздражение, необходимо обратиться к врачу.
При попадании на кожу не вызывает отрицательного воздействия, однако вдыхание мелкой пыли может привести к раздражению слизистых оболочек. В качестве средства защиты при работе с веществом рекомендуется работать в респираторе.
Случайное попадание в желудок может вызвать нарушение деятельности ЖКТ, понос и рвоту. В домашних условия хранить его следует исключив доступ детям.
Условия хранения Особое внимание следует уделить способу хранения. В качестве тары, чаще всего используются водонепроницаемая упаковка. Вещество слабо гигроскопично, однако хранить его следует в сухих помещениях, без воздействия прямых солнечных лучей. Следует применять его на территории закрытого типа складских помещений, где продукт будет защищен от прямого контакта с водой или воздействия повышенной влажности.
Гарантийный срок хранения 1 год со дня изготовления
Производитель сульфата аммония

Высокие стандарты, заданные еще со времен СССР на химическом производстве МЗХР, продолжаются и сегодня. Сегодня мы несем эти традиции и делаем нашу работу на «отлично». Поэтому заказывая сульфат аммония на нашем заводе, будьте уверены что продукция будет стандартно-высокого качества, и при этом, Вы получите продукт в самые сжатые сроки, на столько быстро, на сколько это позволяет сделать логистика перемещения грузов по РФ, а учитывая что у нас имеется собственный ж/д тупик, можно с уверенностью сказать что отгрузка товара происходит очень быстро. От звонка до отправки нужного продукта, может пройти всего несколько часов.
Сегодня мы с уверенностью можем заявить — любые партии и любые объемы любых химических реагентов или веществ для нас уже не вызов, а обычный заказ, которые мы выполняем каждый день.
Приглашаем к сотрудничеству
Предлагаем долгосрочное сотрудничество в области поставок химического сырья, химических реагентов и других веществ. Предлагаем производство по собственным техническим условиям, подготовка и разработка ТУ. Возможность отгрузки день-в-день после подписания договора.
В лице нашего предприятия «МЗХР» Вы будете видеть только надежного партнера, которому можно довериться даже в самых сложных экономических ситуациях.