
Общие сведения
Согласно химическим справочникам, имеет распространенное наименование – медный купорос, формула которого CuSO4. Главным отличием различных видов этого вещества является насыщение жидкостью – водой.
Помимо пентагидрата можно встретить схожий по формуле безводный сульфат, который имеет серо-белый или слегка зеленоватый оттенок. Также существует минерал Бонатит, который называется тригидратом.
Стандартный медный купорос имеет вид кристаллов характерного синего цвета. При употреблении человеком чувствуется слегка металлический привкус. Вещество способно растворяться в воде, метиловом спирте и соляной кислоте.
Некоторое время тому назад Е519 была доступна в пищевой промышленности Российской Федерации. С ее помощью создавали необычный синеватый цвет каких-либо продуктов, использовали как один из лучших консервантов. Наиболее распространенным считается изготовление маслин. В 2010 году на использование медного купороса наложили вето. Несмотря на общепринятое употребление в пищу, современные исследования доказывают некоторое токсическое воздействие, приводящее к мутациям внутри организма.
Наименования продукта
В общепринятых стандартах указывается официальное наименование сульфат меди. В международном обществе принято наименование Cupric Sulphate.
Помимо пищевой промышленности, Е519 используют в фармацевтике, фотографии, сельском хозяйстве, текстильной отрасли.
В странах Европейского союза пищевую добавку называют согласно шифрованному коду – Е519 (иногда указывается с тире между буквой и цифрами).

Тип пищевой добавки
Вещество официально зарегистрировано как стабилизатор, применяемый при изготовлении еды или продуктов питания. В природном виде его можно встретить в некоторых минералах. Это бутит или халькантит. Несмотря на природное происхождение самого источника, вещество неорганическое, относящееся к бинарным соединениям.
С целью применения медного купороса в промышленности, медь растворяют в ранее подогретой серной кислоте. При этом обеспечивается обдувание воздухом. Альтернативным вариантом считается окислительный обжиг. В этом случае окись меди взаимодействует с серной кислотой
Очистка готового продукта подразумевает образование новых кристаллов в дистиллированной воде, которая подвергается процессу кипения. В результате охлаждения образуется осадок, выделяемый из вещества посредством применения специальных фильтров.
| Показатель | Свойства |
|---|---|
| Цвет | Без цвета; в форме кристаллов – синий, бирюзовый или голубой |
| Состав | Сернокислая медь с формулой CuSO4 |
| Внешняя форма | Порошок, кристаллы или кристаллические гранулы |
| Аромат | Нет |
| Растворимость в жидкостях | В воде, метаноле и серной кислоте; нерастворим в этаноле |
| Количество основного компонента | Не менее 98% |
| Вкусовые качества | Неприятный, имеющий вкрапление металла |
| Плотность | 3,64 г/см3 |
| Прочие | При воздействии открытого пространства теряется цвет; повышенная гигроскопичность |
Упаковывание и применение

В современном обществе применение пищевой добавки Е519 запрещается законодательством некоторых стран, в том числе и Российской Федерацией. Процедура исключения была проведена в 2010 году, когда некоторые независимые исследования указали на вред для человеческого организма. Также запрещено использование в Норвегии, некоторых странах Европейского союза, Великобритании и государствах ЕАЭС. До сих пор разрешается применение в Японии, частично – в Украине. Сведения о сульфате меди в Соединенных Штатах Америки отсутствуют.
Польза и вред
Многочисленные современные научные исследовательские центры, проведя точное изучение всех возможных последствий влияния на человеческий организм пищевой добавки Е519, пришли к выводу о ее опасности – присвоен второй класс опасности. Причиной такой ситуации считается возможность накопления вещества в печени и почках, причиняя непоправимый вред организму.
Особенно опасным считается случайное проглатывание пищевой добавки. Токсичное воздействие начинает проявляться в зависимости от возраста человека, массы его тела, общего состояния. Средние показатели свидетельствуют примерно о 0,5 г, приводящих к серьезным нарушениям здоровья.
Стандартными симптомами при отравлении считаются тошнота, позывы к рвоте, появление ожогов на слизистых оболочках, диарея, непроизвольные судороги, сопровождаемые изменением ритма сердечных сокращений. Организм начинает быстро терять воду.
При проявлении подобных симптомов рекомендуется незамедлительно вызывать врача. Пациенту проводят промывание желудка. Для этой цели используется раствор перманганата калия (0,1%), прописывается до 2 ложек сульфата магния (предпочтительно вводить внутривенно).
Опасны и испарения сернокислой меди, которые могут вызвать отек легких при частом вдыхании. При необходимости проведения работ с минеральными удобрениями, рекомендуется использовать респиратор. По их окончанию – тщательно вымываются руки и лицо. Доза, равная 45 г вещества, приводит к летальному исходу.
Применение в других сферах
Сульфат меди разрешено использовать в других сферах деятельности человека – это медицина, сельское хозяйство и ветеринария.
Е915 считается одним из самых сильнодействующих антисептиков. Нередко используется с целью ускорения выработки гемоглобина, а также снимает негативное воздействие отравляющих организм человека фосфорных соединений. Принимается внутрь для эффективного и быстрого очищения желудка посредством выведения содержимого в виде рвоты. Распространено лечение некоторых инфекционных заболеваний, а также анемии.
В сельском хозяйстве является отличным фунгицидом. Используется с целью избавления растений от многих паразитов и микроорганизмов, а также грибковых инфекций. Раствором медного купороса обрабатывают землю перед посевом. Редко используется как удобрение с целью обогащения медью.
В ветеринарии применяется как антисептик и антигельминтное средство. При опрыскивании стойла, исчезают комары и блохи. Обрабатываются и конечности животного с целью излечения от дерматита, язв и прочих недугов. Пищевая добавка Е519 используется с целью излечения от различных инфекций аквариумных рыбок.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Это химическое вещество пользуется популярностью у садоводов, которые заботятся о состоянии растений на дачном участке. Совсем необязательно знать его формулу, важно, что регулярное опрыскивание деревьев весной, обработка кустарников осенью помогает спасти урожай от заболеваний и вредителей. Как правильно приготовить раствор, какие еще есть области применения этого вещества, представляет ли оно опасность – ответы на вопросы полезны не только садоводам.
Что такое медный купорос
Медь сернокислая пятиводная – это название имеет неорганическое химическое соединение. Если соблюдать дозировку, оно обладает полезными свойствами, при больших количествах способно провести к смерти. Состав характеризуется токсичностью, относится к 4 классу опасности ядовитых веществ:
-
при попадании порошка внутрь раздражает слизистые оболочки;
- проникает через кожу в организм при обратном всасывании пота;
- при попадании на еду может вызвать пищевое отравление;
- не исключен летальный исход.
Химическое соединение – порошок голубого цвета или прозрачные ярко-синие триклидные кристаллы, содержащее в составе 24% меди. Препарат обладает физическими свойствами:
-
металлический привкус;
- отсутствие запаха;
- высокая гигроскопичность;
- хорошая растворимость в спирте воде, растворах серной кислоты с большой концентрацией;
- температура разложения – 100-250;
- выветривается на воздухе;
- смертельная доза – 35 мл жидкости концентрацией 5%.
Формула
Что такое сульфат меди? Это вещество, получаемое в промышленных условиях как результат химической реакции. Оно обладает очень высокой гигроскопичностью, при поглощении жидкости образует кристаллы – пентагидрат сульфата меди. Другое название соединения – медный купорос или медная соль серной кислоты. Состав имеет химическую формулу CuSO4 5H2O. В ней наблюдается связь одной молекулы соли с пятью молекулами воды.
Свойства
Если сернокислую медь использовать правильно, то будут только положительные эффекты от применения. При этом она безопасна, не накапливается организмом, растениями и почвой, не дает побочных эффектов. Полезные свойства соединения:
-
вяжущее;
- антисептическое;
- прижигающее;
- дезинфицирующее;
- фунгицидное – противодействует грибкам, бактериям, плесени;
- не вызывает привыкания у вредоносных насекомых;
- способствует синтезу фитогормонов у растений.
Для чего нужен
Благодаря своим химическим свойствам медь сернокислая находит огромное применение во многих областях. Ее используют как пищевую добавку при выращивании сельскохозяйственных животных, для дезинфекции при содержании скота. Состав применяется:
-
для очистки водоемов, бассейнов;
- как компонент для изготовления препаратов в фармакологии;
- при химической обработке воды.
Состав широко используется в промышленности:
-
горнодобывающей – при получении кобальта, цинка, свинца;
- металлургической – как состав для гальванических ванн, изготовления медных катодов;
- для производства печатных плат;
- при изготовлении электрических батарей;
- для выпуска стекла, зеркал;
- при производстве пигментов, красителей для кожи, керамики, текстиля;
- как пищевая добавка Е 519 в продуктах;
- для изготовления ацетатного полотна, красок.
Применение медного купороса в садоводстве
Особой популярностью пользуется купорос в сельском хозяйстве и в огородах. Он находит применение в различных качествах. Химическое вещество используется:
-
для борьбы с фитофторозом на томатах и картофеле;
- как средство от садовых вредителей;
- для обеззараживания земли;
- как подкормка при дефиците меди в почве;
- как удобрение для садовых и комнатных растений;
- для обработки стен от плесени в ямах, сараях;
- для целей профилактики грибковых заболеваний кустов и деревьев, садовых вредителей.
Весной
Как обрабатывать медным купоросом растения на садовом участке? Применение химического вещества имеет особенности, зависящие от времени года. В весеннее время:
-
до распускания почек обрабатывают растения от плодовой гнили готовым раствором с концентрацией 1% – яблони, груши, айву;
- ранней весной проливают землю рабочей жидкостью с насыщенность 0,5% от черной ножки, серой гнили;
- перед посадкой производят обеззараживание картофеля 0,2% жидкостью от фитофтороза;
- добавляют к раствору для побелки деревьев.
Чтобы получить ранние всходов огурцов, семена замачивают на 10 часов в теплом 0,2% составе. К весенним работам относится дезинфекция корней саженцев. Их выдерживают 3 минуты в составе с насыщенностью 1%, затем тщательно промывают водой. Для протравливания от болезней семян выдерживают 15 минут в специальной смеси, затем хорошо промывают. Для приготовления раствора в 10 литрах теплой воды растворяют:
-
2 г борной кислоты;
- 10 граммов марганцовокислого калия;
- столько же порошка медной соли серной кислоты.
Летом
При появлении на участке вредителей или признаков заболеваний, производят обработку винограда, опрыскивания роз, листьев растений и кустарников. С возникновением летом признаков фитофтороза на картофеле, томатах применяют фунгициды. Для приготовления состава:
-
налить 10 литров воды;
- развести медный купорос – 100 грамм порошка;
- произвести опрыскивание кустов в сухую погоду без ветра.
Осенью
При окончании огородного сезона проводят обработку растений, деревьев и приствольных кругов от вредителей и заболеваний. Для лечения грибка в осеннее время рекомендуют применять крепкий раствор бордоской жидкости. Чтобы его приготовить, необходимо:
-
взять 10 литров воды;
- добавить 400 г гашеной извести;
- всыпать 300 г порошка медной соли серной кислоты;
- тщательно размешать.
Применение медного купороса в медицине
Хотя врачи официальной медицины настороженно относятся к применению этого вещества для лечения заболеваний, народные целители практикуют использование и показывают положительные результаты. Они отмечают, что полезные свойства медной соли серной кислоты способствуют выздоровлению при наличии:
-
радикулита;
- грибковых заболеваний;
- сахарного диабета;
- гинекологических патологий;
- инфекционных болезней;
- злокачественных опухолей;
- приступов эпилепсии;
- полиартрита.
Антисептик
Применение раствора рекомендуется при гинекологических заболеваниях, вследствие антисептических, прижигающих, противоинфекционных свойств. Можно ли спринцеваться медным купоросом? Лучше перед проведением процедуры посоветоваться с гинекологом. После его разрешения важно соблюдать все пропорции, чтобы не получить побочных эффектов, опасных для жизни.
Для спринцевания сначала делают маточный раствор – разводят в литре кипятка столовую ложку чистых кристаллов сульфата меди, приобретенных в аптеке. Состав необходимо отфильтровать. Для приготовления рабочего раствора потребуется:
-
взять 0,5 литра теплой кипяченой воды;
- влить столовую ложку маточного состава;
- перемешать;
- вечером провести процедуру спринцевания;
- утром повторить с раствором соды;
- выполнять раз за неделю.
Для прижиганий
Опытные дерматологи отмечают эффект от использования пентагидрата сульфата меди при лечении мокрой экземы. Для этого необходимо приготовить синюю мазь. При ее регулярном нанесении происходит прижигание болезненных язвочек. Через два дня они из синих становятся коричневыми и отваливаются. Для изготовления состава потребуется:
-
измельчить голубые кристаллы пентагидрата сульфата меди;
- просеять их через 3 слоя марли;
- смешать равные части с чистым вазелином;
- легонько расчесать небольшой участок кожи;
- нанести мазь;
- втереть;
- постепенно обработать всю поверхность.
При отравлении
Долгие годы существовала практика применения медного купороса при появлении признаков отравлении в качестве средства, вызывающего рвоту. Поскольку даже небольшое нарушение концентрации раствора может вызвать серьезные проблемы со здоровьем, современные медики отказались от такого метода лечения. Однако Всемирная организация здравоохранения в своей анатомической терапевтической системе классификации считает это вещество антидотом.
Лечение медным купоросом в народной медицине
Народные целители применяют слабый раствор для дезинфекции ран. Мазь, сделанная на основе медной соли серной кислоты, избавляет от грибка ногтей. Смесь доводится до кипения, охлажденной наноситься на поверхность до устранения симптомов. Для приготовления требуется смешать равные части:
-
порошка сернокислой меди;
- гусиного жира;
- белой серы.
Для эффективного лечения рака кишечника, желудка, молочной железы, рекомендуют по утрам принимать внутрь по 50 мл раствора. Для приготовления нужно настоять в течение суток щепотку вещества с половиной литра воды. Лечебными свойствами при диабете отличаются ванны, снижающие потребность в инсулине, если их принимать трижды за неделю. Процедуру проводят до 15 раз. Для ее проведения:
-
наполнить ванну водой;
- добавить 3 ложки кристаллов сульфата меди;
- полежать 15 минут.
Применение медного купороса в строительстве
Благодаря огнеупорным, фунгицидным свойствам водный раствор сульфата меди с концентрацией 10% используется при выполнении строительных работ. Препарат наносится на деревянные, бетонные, кирпичные поверхности. Состав медного купороса способствует:
-
антисептической защите деталей из дерева от гниения;
- удалению ржавых пятен на поверхности строений;
- приданию материалам огнеупорных свойств;
- нейтрализации протечек;
- противогрибковой защите поверхности стен, полов, потолков перед отделочными работами.
Вред медного купороса
Необходимо соблюдать осторожность при использовании химического средства в домашних и огородных условиях. Во время работы с купоросом рядом не должны находиться дети и животные, требуется соблюдение инструкции по технике безопасности. При попадании вещества в организм необходимо срочное обращение к врачу. Промывание желудка может усугубить положение. Если препарат попал внутрь:
-
при вдыхании – происходит ожог слизистой легких;
- во время проглатывания – возникает раздражение желудочно-кишечного тракта;
- при поражении глаз – ожоги поверхности глазного яблока.
Особую опасность для жизни представляет попадание сульфата меди в кровь. Как результат токсического действия происходит:
-
разрушение мембраны эритроцитов;
- негативное воздействие измененной крови на клетки нервной системы, легких;
- накапливание вещества в почках, печени, что нарушает их нормальное функционирование;
- отравление организма, при больших дозах заканчивающееся летальным исходом.
Видео
Нашли в тексте ошибку? Выделите её, нажмите Ctrl + Enter и мы всё исправим!
Медный купорос – это вещество, принадлежащее к классу неорганических. Оно представляет собой медную соль серной кислоты. Другое название – сульфат меди. Особенной популярностью медный купорос пользуется у владельцев как огромных полей, так и совсем маленьких огородов – применяют вещество практически все дачники и садоводы. Медный купорос традиционно применяют для обработки деревьев весной. Его также применяют для защиты кустарников в осенний период и предотвращения появления заболеваний.
Визуально медный купорос – это сравнительно небольшие кристаллы с голубоватым или синеватым оттенком. Вещество нелетучее, запах у него полностью отсутствует. Для вещества характерен горький вкус с металлическим оттенком.
В природе медный купорос можно встретить в составе некоторых минералов. На крупных предприятиях его производят посредством воздействия серы на основной компонент.

Данное вещество легко растворяется в обычной воде, особенно легко кристаллы купороса таят в подогретой жидкости. При попадании в воду вещество выделяет тепло, а при длительном пребывании на открытом воздухе соединение теряет все свои свойства, а его цвет меняется из голубого на белый или серый.
Что такое медный купорос
Медный купорос – это неорганическое соединение, представленное голубыми кристаллами, которое достигло наибольшей популярности в сельскохозяйственной сфере: его используют для защиты плодовых деревьев и различных кустарников, для обработки почвы с целью предотвращения развития различных заболеваний и для защиты от грибка. Стоит отметить, что данное соединение не вызывает привыкания у вредителей и бактерий, поэтому его эффективность со временем не снижается.
Сульфат меди во всемирной классификации значится под индексом Е519. Получают данное соединение исключительно синтетическим способом. Добавку, помимо обработки растений, применяют также в качестве консерванта. В малых дозах она безопасна для человеческого организма. Впрочем, начиная с 2010 года применение сульфата меди в качестве пищевой добавки на территории Российской Федерации запрещено: специалисты утверждали, что несмотря на общее мнение о безопасности медного купороса, он способен вызывать мутации в организме и оказывать на него токсическое воздействие.
Визуально сульфат меди представляет собой однородный порошок с легким синеватым оттенком. В безводной среде вещество выглядит как белый порошок.

Кристаллы медного купороса
Формула медного купороса и его свойства
Формула медного купороса:
CuSO4
Основные сведения о медном купоросе:
- Молярная масса – 160 г/моль.
- Плотность – 3,64 г/см3.
- Твердость кристаллов – 2,5.
- Цвет – синий или голубоватый, в определенных условиях может быть белым или сероватым.
- Внешняя форма – крупные кристаллы или гранулы.
- Запах – отсутствует.
- Растворимость – кристаллы медного купороса легко таят в воде, метаноле и серной кислоте.
- Вкус – горький, с металлическим послевкусием.
- Температура, при которой вещество начинает разлагаться – 650 градусов.
При нагревании медного купороса до 110 градусов, отщепляется 4 молекулы воды, а при повышении показателя температуры до 150 градусов и вовсе теряет всю жидкость, содержащуюся в его составе.
В процессе нагревания медный купорос отщепляет две молекулы воды и преобразуется в тригидрат, затем в моногидрат, а при нагревании до отметки в 258 градусов – в безводную соль. Разложение вещества происходит при повышении температуры до отметки 650 градусов. По завершении реакции разложения образуются оксиды меди и серы и выделяется кислород.
Медный купорос прекрасно растворяется в воде, причем его способность к растворению возрастает при нагревании жидкости. При гидролизации вещество дает кислую среду.
При взаимодействии с щелочными металлами купорос образует комплексные соли.
При добавлении вещества в пламя, оно меняет свой цвет из красно-оранжевого в зеленый.
Кроме того, сульфату меди присущи следующие свойства:
- вяжущее – вещество способно регулировать консистенцию;
- антибактериальное – медный купорос устраняет бактерии, защищая тем самым растения от развития заболеваний;
- прижигающее;
- обеззараживающее;
- фунгицидное – сульфат меди борется с грибками и различными видами плесени;
- ускоряет синтез фитогормонов у растений.

Молекула медного купороса
Получение медного купороса
В современном мире известны разные методы получения медного купороса. Так, например, наибольшей популярностью пользуются следующие способы:
- растворение разного рода отходов, основу которых составляет меть, в слабой серной кислоте с параллельным обдувом воздушными массами;
- растворение оксида меди в высококонцентрированной серной кислоте (в данном случае обдув воздухом не требуется);
- обжиг меди;
- электролитическое воздействие на чистую медь – при данном методе вместе с медным купоросом выделяются и другие, побочные продукты.
Реакции с медным купоросом и соединения на его основе
Характерной для сульфата меди является реакция электрической диссоциации, в ходе которой медный копорос образует два вещества – медь и оксид серы:
CuSO4 → Cu2 + SO4
Реакция замещения медного купороса возможна исключительно в водных растворах, в которых присутствуют металлы, чья активность превышает активность меди – то есть, металлов, которые располагаются в электрохимическом ряду левее купрума. Рассмотрим реакцию замещения с цинком:
CuSO4 + Zn → Cu ↓ + ZnSO4
Сульфат меди с легкостью вступает в реакции со щелочами с выделением гидроксида меди, представленного осадком насыщенного голубого или синего цвета:
CuSO4 + 2KOH → Cu(OH)2↓ + K2SO4
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
Медный купорос вступает в обменные реакции с солями:
CuSO4 + BaCl2 → CuCl2 + BaSO4↓
Взаимодействие сульфата меди с аммиаком:
CuSO4 + 4NH3 → [Cu(NH3)4]SO4
Допустимые нормы приема медного купороса
Употреблять медный купорос в пищу не рекомендуется – отечественные специалисты заявляют о его токсичности и способности вызывать мутации в организме. Максимально допустимой дозировкой вещества для взрослого здорового человека считается 2,5 грамма. При превышении этого показателя велик риск ухудшения самочувствия.
Сферы применения медного купороса
Сульфат меди крайне часто применяют как исходное сырье для получения длинного перечня соединений.
Безводный вариант вещества применяют для определения уровня влажности. Кроме того, с его участием осуществляется осушка этанола и некоторых других соединений.
Большая часть от всего производимого в мире купороса уходит на борьбу с вредителями в сельскохозяйственной сфере. На основе сульфата меди готовят специальные растворы, защищающие растения от появления плесени, от грибка, от отрицательного воздействия насекомых и бактерий.
В сфере строительства раствор медного купороса необходим для устранения последствий протечек разного рода жидкостей, а также удаления въевшейся ржавчины и следов соли на кирпичных и каменных стенах. Раствором пропитывают деревянные конструкции, дабы защитить их от гнилостных процессов, от грибка и плесени.
Встретить медный купорос можно в перечне ингредиентов некоторых красящих средств.
В медицине раствор медного купороса применяется как один из компонентов электролитических ванн. В фармакологии его используют как ингредиент для приготовления лекарственных смесей.
В производстве продуктов питания медный купорос применяют в качестве вещества, продлевающего срок хранения различной продукции, добавка известна под индексом Е519. Однако применение медного купороса в сфере производства продуктов питания строго ограничено, а в некоторых странах (например, в России) и вовсе запрещено.
Также медный купорос применяется для обработки водоемов и бассейнов – там его действие аналогично тому, какое он оказывает в сельскохозяйственной сфере: соединение препятствует образованию бактерий.

Раствор медного купороса
Сульфат меди можно встретить и в горнодобывающей промышленности – он применяется при получении различных цветных металлов. В металлургии медный купорос применяют в гальванических ваннах для производства медных катодов.
Медный купорос применяется на производстве зеркал и стекол, полотен и красок для них.
Медный купорос в садоводстве
Наибольшей популярностью, как уже было сказано выше, раствор медного купороса пользуется в сельскохозяйственной сфере, где он применяется для:
- борьбы с фитофторозом (заболеванием, причиной которого является воздействие грибоподобных микроорганизмов, поражающих томаты и картофельные клубни – в результате они начинают гнить, покрываются плесенью;
- защиты растений от воздействия на них вредителей. Причем медный купорос не вызывает привыкания – со временем эффект от его применения не становится менее заметным;
- обеззараживания земли;
- как удобрение в случае нехватки меди в почве – такая проблема наиболее характерна для известковых грунтов;
- удобрения как садовых, так и комнатных, горшковых растений;
- профилактики грибковых заболеваний у кустарников и деревьев.
Краткие выводы о применении медного купороса в различных сферах:
| Сфера применения | Назначение медного купороса |
| Тяжелая промышленность | Гальванические процессы |
| Пищевая промышленность | Консервант |
| Химическая промышленность | Сырье для получения различных соединений, анализ металлов |
| Строительство | Защита деревянных конструкций, удаление ржавчины и солевого налета со стен |
| Производство лакокрасочных материалов | Компонент красок, регулирующих их консистенцию |
| Медицина | Антисептик, прижигающее средство, раствор, улучшающий состояние больного при тяжелых отравлениях |
| Животноводство | Пищевая добавка |
| Сельское хозяйство | Обработка почвы с целью защиты растений от различных заболеваний |
| Обработка водоемов и растений | Предотвращение негативного воздействия бактерий на качество воды |
Влияние медного купороса на организм человека
При взаимодействии с раствором на основе сульфата меди необходимо строго следовать правилам, позволяющим обеспечить безопасность работников. Так, крайне важным является строгое соблюдение рекомендуемых дозировок.
В избыточных количествах рассматриваемое соединение опасно для человека: особенно агрессивное воздействие оно оказывает на кожу и слизистые оболочки, вызывая раздражение, покраснение и сыпь. При регулярном контакте с медным купоросом велик риск разрушения мембранного слоя у эритроцитов, возникновения проблем с бронхами, легкими и органами пищеварительной системы.
Опасным считается медный купорос в количестве 11 мк на 1 килограмм веса.
С точки зрения токсичности рассматриваемое соединение принадлежит ко 2 классу опасности – это высокоопасные вещества. Они оказывают негативное воздействие на состояние здоровья человека и животных.
Фармакологическое действие медного купороса
Медный купорос способен оказывать антисептическое воздействие, и, вместе с этим, вызывать рвотные реакции. В определенных условиях вещество способно нейтрализовать фосфор и выводить его из организма.
В небольших количествах медный купорос стимулирует выработку гемоглобина, поэтому препараты, включающие его в свой состав, часто назначают пациентам, страдающим анемией.
Польза медного купороса
Наибольшую пользу сульфат меди несет не людям, а растениям – медный купорос помогает предотвратить развитие длинного перечня заболеваний у различных растений. Благодаря медному купоросу можно защитить от грибка и вирусных болезней.
Для человека медный купорос способен нести пользу только в составе лекарственных препаратов.
Вред медного купороса
Специалисты, проводившие исследования в разных странах и в разное время, установили токсичное воздействие медного купороса на здоровье человека. Так, сульфат меди обладает способностью скапливаться в организме, оказывая негативное воздействие на состояние печени и почек.
Особенно сильное негативное воздействие можно получить при случайном проглатывании вещества. Степень вреда определяется возрастом человека, его весом и состоянием здоровья.
Специалисты называют следующие симптомы отравления медным купоросом:
- сильная рвота;
- диарея и вздутие в области живота;
- поражение слизистых оболочек;
- судороги;
- ускорение сердечного ритма.
В случае отравления необходимо срочно промыть желудок.
Инструкция по применению медного купороса
Садоводство
Чтобы приготовить раствор медного купороса для обработки растений, потребуется горячая вода и, собственно, сам медный купорос. Его объем зависит от того, с каким конкретно растением вы имеете дело.
Традиционно применяют 1% раствор медного купороса, норма расхода которого составляет 10 литров на 100 м2. Объем раствора, который необходим для обработки, зависит от того, с каким конкретно растением вы имеете дело.
Существуют следующие правила разведения медного купороса для получения раствора для обработки:
- яблоня груша и айва – 100 г порошка на 10 л воды, расход – от 2 до 5 литров на одно дерево;
- абрикос, персик, слива и вишня – 50-60 г порошка на 10 литров воды, расход – от 2 до 3 литров на дерево;
- крыжовник и смородина – 50-60 г порошка на 10 л воды, а один куст потребуется приблизительно 1,5 литра;
- картофель – 2 г препарата на 10 л воды.
Сульфат меди разводят в воде до полного растворения кристаллов. В теплое время года и весной рекомендуется применение 1%-го раствора купороса, для более взрослых растений лучше использовать более концентрированный препарат.
Весеннюю обработку осуществляют в начале марта (еще до образования и набухания почек), когда температура задерживается на отметке от 5 до 6 градусов. Повторную обработку проводят в начале осени.
Важно ограничить доступ детям и животным к местам обработки растений.
Долго хранить готовый раствор не рекомендуется – со временем он теряет свои свойства.
Работать с раствором купороса разрешается исключительно в защитных перчатках, не допуская его попадания в кожу и глаза.
Медный купорос для бассейна, дозировка на куб
Для обеззараживания воды в бассейне используется пропорция 0,9 грамм медного купороса на 1 куб (1000 литров). Часто в воду для бассейна вместе с купоросом добавляют соль, это дополнительный антисептик для воды. Пропорция – 3:1, т.е. три части соли и 1 часть купороса.
Такие пропорции воды и медного купороса считаются безопасными для бассейна. Что будет при попадании раствора медного купороса внутрь описано выше, это канцерогенное вещество и чем больше его попадет внутрь, тем выше вероятность отравления и летального исхода. Поэтому дезинфицируя воду для бассейна не превышайте установленные пропорции.
Фармакология
Для лечения разного рода заболеваний также применяют раствор медного купороса:
| Концентрация раствора сульфата меди | Назначение |
| 0,1 % | Отравление фосфором – раствор применяют для промывки желудка и выведения следов фосфора |
| 0,25 % | Конъюнктивит – раствор применяют в виде глазных капель, для одного глаза используют от 2 до 3 капель препарата |
| 0,25 – 1,0 % | Уретрит и вагинит |
| 0,5 – 1,0 % | Витилиго – препарат принимают вовнутрь, во время еды. Используют от 5 до 15 капель лекарства трижды в день |
| 1 % | Рвотное средство – рекомендуется применение 15 мл раствора внутрь каждые 10 минут до возникновения рвотных позывов |
| 5,0 % | Ожоги от фосфора – ватные диски пропитывают лекарственным раствором, затем делают примочки для пораженных участков кожи |
Медный купорос как пищевая добавка: его класс опасности и особенности хранения
Медный купорос в пищевой промышленности известен под индексом Е519. Он принадлежит к классу стабилизаторов, регулирующих консистенцию пищевых продуктов.
В наши дни медный купорос запрещается применять в производстве продуктов питания в следующих странах: Норвегии, Англии, России и странах ЕС. Но существуют государства, которые его применяют в пищевой промышленности, к ним относятся Япония и Украина.
Медный купорос принадлежит к 2 классу опасности – то есть, высокоопасным соединениям. Вещество обладает свойством накапливаться в организме человека, вызывая нарушение работы печени и почек.
Хранить сульфат меди рекомендуется в многослойных бумажных или полипропиленовых мешках, обладающих дополнительной полиэтиленовой вставкой. На полки специализированных магазинов медный купорос поступает в пластиковых банках или флаконах, реже его можно встретить в плотных полиэтиленовых пакетах.
Где можно приобрести медный купорос и сколько он стоит
Приобрести медный купорос можно в специализированных хозяйственных магазинах или в интернете.
100 граммов медного купороса будет стоить вам примерно 60-70 рублей.
Заключение
Медный купорос – это соединение, принадлежащее к классу неорганических веществ. Наибольшей популярностью оно пользуется в сфере садоводства: сульфат меди необходим для обработки плодовых растений и деревьев – он предотвращает развитие заболеваний, причиной которых является воздействие бактерий и микроорганизмов, защищает от грибка.
В пищевой промышленности применение вещества ограничено из-за его способности оказывать сильный вред на здоровье человека. В России и большинстве стран Евросоюза применение медного купороса как пищевой добавки запрещено. При попадании в организм сульфат меди вызывает сильное отравление, поражает кожный покров, вызывает нарушение работы органов пищеварительной системы.
Читайте также:
- Пропиленгликоль: описание, свойства, вред, применение
- Нитрат калия (Е252, калиевая селитра): вред и польза, применение, реакции
- Формальдегид: опасность, влияние на организм, где содержится
- Бензоат натрия (Е211): применение, вред и польза, инструкция, описание
Загрузка…
У этого термина существуют и другие значения, см. Сульфат меди.
Кристаллогидрат сульфата меди CuSO4 · 5H2O
Сульфат меди(II) (CuSO4) — медная соль серной кислоты, белые кристаллы, хорошо растворимые в воде. Однако из водных растворов, а также на воздухе хотя бы с незначительным содержанием влаги кристаллизуется голубой пентагидрат CuSO4 · 5H2O — медный купорос.
Получение
В промышленности получают растворением Cu и медных отходов в разб. H2SO4 при продувании воздуха; растворением CuO в H2SO4; сульфатизирующим обжигом сульфидов Cu; как побочный продукт электролитич. рафинирования Cu.
В лаборатории можно получить действием концентрированной серной кислотой на медь при нагревании:
Температура не должна превышать 60 градусов Цельсия, так как образуется побочный продукт:
Также в лабораторных условиях сульфат меди (II) может быть получен реакцией нейтрализации гидроксида меди (II) серной кислотой:
Очистка
Обычно технический сульфат меди загрязнен сульфатом железа (II). Реактив Ч. Д. А. не содержит ионов Fe2+. Реактив загрязнен изоморфически и его невозможно очистить простой перекристаллизацией. В нашем случае можно окислить Fe2+ до Fe3+ кипячением полученного раствора сульфата меди с PbO2. Fe2(SO4)3 не формирует изоморфическую смесь с сульфатом меди. После кипячения раствор фильтруют. А потом кристаллизацией получают чистый сульфат меди.
Физические свойства
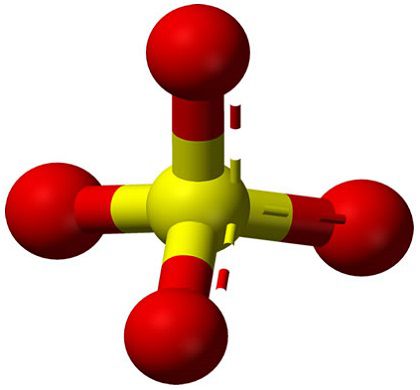
Строение кристаллогидрата
Структура медного купороса приведена на рисунке. Как видно, вокруг иона меди координированы два аниона SO42− по осям и четыре молекулы воды (в плоскости), а пятая молекула воды играет роль мостиков, которые при помощи водородных связей объединяют молекулы воды из плоскости и сульфатную группу.
Растворимость CuSO4, г/100 г H2O
Термическое воздействие
При нагревании последовательно отщепляет две молекулы воды, переходя в тригидрат CuSO4 · 3H2O (этот процесс, то есть выветривание, частично идёт и просто на воздухе), затем в моногидрат (110°) CuSO4 · H2O, и выше 258 °C образуется безводная соль. Термическое разложение становится заметным выше 650 °C:
Растворимость
Растворимость сульфата меди(II) по мере роста температуры проходит через плоский максимум, в течение которого растворимость соли почти не меняется (в интервале 80-200 °C). (см. рис.)
Как и все соли, образованные ионами слабого основания и сильной кислоты, сульфат меди(II) гидролизуется, (степень гидролиза в 0,01М растворе при 15 °C составляет 0,05 %) и даёт кислую среду (pH указанного раствора 4,2). Константа диссоциации составляет 5·10−3.
Химические свойства
Диссоциация
CuSO4 — хорошо растворимая в воде соль и сильный электролит, в растворах cульфат меди (II) так же, как и все растворимые соли, диссоциирует в одну стадию:
Реакция замещения
Реакция замещения возможна в водных растворах сульфата меди с использованием металлов активнее меди, стоящих левее меди в электрохимическом ряду напряжения металлов.
Реакция с растворимыми основаниями (щелочами)
Сульфат меди(II) реагирует с щелочами с образованием осадка гидроксида меди(II) голубого цвета:
Реакция обмена с другими солями
Сульфат меди вступает также в обменные реакции по ионам Cu2+ и SO42-
Прочее
С сульфатами щелочных металлов и аммония образует комплексные соли, например, Na2[Cu(SO4)2]·6H2O.
Ион Cu2+ окрашивает пламя в зеленый цвет.
Применение
Кристаллы сульфата меди (II), выращенные в домашних условиях
Монокристалл сульфата меди (II), выращенный в домашних условиях
Сульфат меди(II) — наиболее важная соль меди — часто служит исходным сырьём для получения других соединений. Например, гидроксида меди (II) — Cu(OH)2 — вещества, необходимого для качественных реакций на глюкозу, глицерин.
Безводный сульфат меди можно использовать как индикатор влажности, с его помощью в лаборатории проводят обезвоживание этанола и некоторых других веществ.
Наибольшее количество непосредственно применяемого CuSO4 расходуется на борьбу с вредителями в сельском хозяйстве, в составе бордоской смеси с известковым молоком — от грибковых заболеваний и виноградной тли. Для этих целей сульфат меди (II) имеется в розничной торговле.
В строительстве водный раствор сульфата меди применяется для нейтрализации последствий протечек, ликвидации пятен ржавчины, а также для удаления выделений солей («высолов») с кирпичных, бетонных и оштукатуренных поверхностей; а также как антисептическое и фунгицидное средство для предотвращения гниения древесины.
Также он применяется для изготовления минеральных красок, в медицине, как один из компонентов электролитических ванн для меднения и т. п. и как часть прядильных растворов в производстве ацетатного волокна.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E519. Используется как фиксатор окраски и консервант.
В пунктах скупки лома цветных металлов раствор медного купороса применяется для выявления цинка, марганца и магния в алюминиевых сплавах и нержавейке. При выявлении этих металлов появляются красные пятна.
Токсикология
Токсикологические данные
Сульфат меди (II) относится к классу опасности 1 (малоопасное вещество), как вещество, содержащее сульфат-ион. С другой же стороны, на стограммовой упаковке сульфата меди, поступающей в розничную продажу, указан класс опасности 2 (высокоопасное вещество). Смертельная доза медного купороса составляет от 8 до 30 граммов для взрослого человека перорально (через рот)[1][2] . Летальная доза зависит от состояния здоровья человека, от его массы, от иммунитета именно к данному веществу и от других факторов.
Первая помощь при отравлении
При попадании вещества на кожу необходимо снять его ватой или куском ткани, затем обмыть прохладной водой с мылом. При попадании в глаза необходимо обильно промыть их проточной водой. При попадании через дыхательные пути нужно вывести пострадавшего на свежий воздух, прополоскать рот водой. При попадании в желудочно-кишечный тракт необходимо промыть желудок пострадавшего 0,1%-ым раствором марганцовки, дать выпить пострадавшему солевое слабительное — сульфат магния 1-2 ложки, вызвать рвоту, дать мочегонное.
Безопасность
При обращении с сульфатом меди (II) в бытовых условиях стоит быть очень осторожным, иначе можно нанести непоправимый вред здоровью[3]. При приготовлении растворов желательно использовать резиновые или одноразовые полиэтиленовые перчатки, очки, резиновые сапоги и также настоятельно рекомендуется использовать респиратор. Ни в коем случае не использовать пищевую посуду. Приготовление раствора и использование медного купороса стоит производить в отсутствие детей и животных. Во время использования нельзя пить, курить, принимать пищу. После работы лицо и руки вымыть с мылом, прополоскать рот.
Хранить в сухом прохладном месте при температуре от −30 до +30 °C, отдельно от лекарств, пищевых продуктов и кормов для животных, в недоступном для детей и животных месте. Запрещается хранение вещества в поврежденной упаковке.
Производители и поставщики
Сульфат меди (II), как средство от гниения, сорняков и т. д. находится в розничной продаже в супермаркетах и хозяйственных магазинах. Чаще всего на прилавках можно найти упаковку весом в 100 граммов. Производство данной продукции осуществляется компанией ЗАО Фирма «Август». Также медный купорос можно найти в химических магазинах разной фасовки. Обычно это пластиковые банки весом в 1 кг или полиэтиленовые мешки весом в 500 г.
Нахождение в природе
В природе изредка встречается минерал халькантит, состав которого близок к CuSO4 ∙ 5H2O
См. также
- Халькантит
- Сульфаты
- Медь
- Соединения меди
- Купорос
- Пищевые добавки
- Сульфат меди(I)
Примечания
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.








![Сульфат меди в химии как пишется mathsf{2CuSO_4 xrightarrow[]{^ot} 2CuO + 2SO_2 + O_2}](https://dic.academic.ru/dic.nsf/ruwiki/3b263af760ea620184767f698f4678c0.png)







