- урология
- услуги и цены
- заболевания
- симптомы
- видео
- сотрудники
Нефролитолапаксия (эндоскопическое дробление камней почек), также называемая перкутанной (чрескожной) нефролитотрипсией – это хирургическое вмешательство при мочекаменной болезни по удалению камней, не поддающихся дистанционной литотрипсии, или при технической невозможности проведения последней. Операция является малотравматичной, проводится эндоскопически, т.е. через небольшой прокол кожи (около 10 мм) в поясничной области, и является альтернативой более травматичной открытой операции на почке.
Нефролитолапаксия — наиболее эффективный метод удаления из почек камней больших размеров и высокой плотности.
В зависимости от категории сложности от 110 000 — 150 000 руб.
В стоимость входит:
проведение операции, анестезиологическое пособие, перевязки, медикаменты, питание и пребывание в стационаре
40-90 минут
(продолжительность процедуры)
Показания
- камни почек размером более 15 мм, в том числе коралловидные камни
- неэффективность дистанционной литотрипсии
Противопоказания
- острые воспалительные, гнойные процессы в организме
- беременность
- нарушение свертываемости крови
- острое воспаление почек (острый нефрит)
Как выполняется нефролитолапаксия в ЦЭЛТ?
- Безболезненно
Процедура проводится под наркозом - Под визуальным контролем
Под рентгеновским и ультразвуковым наведением выполняется пункция почечной лоханки. Хирург делает разрез в области поясницы и вводит через него эндоскоп. Через эндоскоп врач визуализирует камни и выполняет дробление - Безопасно
Дробление камня выполняется с помощью контактного ультразвукового или пневматического литотриптера. Мелкие фрагменты камней удаляются путем промывания лоханок, крупные камни фрагменты извлекаются специальным инструментом. В конце процедуры в почке оставляют дренаж для профилактики осложнений. Его удаляют через 1-2 дня.
Почему нам доверяют и выбирают клинику ЦЭЛТ?
- За 25 лет мы выполнили более 4000 таких операций
- В клинике накоплен большой опыт успешного лечения острых и осложненных форм мочекаменной болезни
- Огромный опыт урологов и современное оборудование гарантируют эффект и практически полное отсутствие осложнений
- Комфортное пребывание без боли во время операции и в послеоперационный период
Отзывы о врачах оказывающих услугу — Нефролитолапаксия
Перепечай Дмитрий Леонидович, спасибо, что Вы есть. 21 год знаю выдающегося Врача Уролога — Перепечая Дмитрия Леонидовича. У меня были проблемы, теперь у меня их нет, лишь езжу периодически на плановую проверку и пожать руку Дмитрию Леонидовичу.
Николай
07.03.2019
Спасибо доктору!
Перепечай Дмитрий Леонидович — очень помог. Это знающий, опытный, доброжелательный, широкого профиля врач. Низкий ему поклон.
Благодарна также сотрудникам кабинета компьютерной томографии (Червоненко Светлана Владимировна и др.) и всем сотрудникам
Валентина
03.03.2019
Часто задаваемые вопросы
Безопасные камни в почках встречаются крайне редко. Рано или поздно болезнь переходит из разряда камненосительства в стадию различных осложнений: развивается почечная колика, острый пиелонефрит (воспаление почки), гнойный пиелонефрит, пионефроз, гидронефроз, почечная недостаточность. Поэтому мочекаменная болезнь требует своевременного лечения.
Чем отличается нефролитолапаксии от дистанционной литотрипсии?
При нефролитолапаксии используется не дистанционное, а контактное дробление. В некоторых случаях применение дистанционной литотрипсии (ДУВЛ) малоэффективно, а иногда даже невозможно из-за локализации камней, их больших размеров или высокой плотности. Иногда нефролитолапаксию используют в комплексе с ДУВЛ. Сначала выполняют дробление более мелких камней, а более крупные дробят и удаляют с помощью эндоскопа.
Нужна ли специальная подготовка к нефролитолапаксии?
Специальной подготовки не требуется. При наличии выраженного воспалительного процесса мочевых путей перед процедурой проводится противовоспалительная терапия.
Нужна ли дополнительная диагностика перед операцией?
Перед госпитализацией необходимо получить консультацию врача-уролога (с УЗИ) и выполнить стандартное обследование. Сдать анализы:
- клинический анализ крови
- общий анализ мочи
- биохимический анализ крови (мочевина, креатинин, билирубин, глюкоза)
- коагулограмма (МНО, протромбин, АЧТВ)
- анализ крови на ВИЧ, RW, HBsAg, HCV
- анализ крови на группу, резус-фактор и антитела к резус-фактору с фенотипированием
- ЭКГ (электрокардиограмма)
- рентгенография органов грудной клетки
Может потребоваться компьютерная томография.
О необходимости дополнительной диагностики врач сообщит на консультации.
Чем определяется категория сложности нефролитолапаксии?
Категория сложности зависит от размера камней, расположения, их количества, наличия сопутствующих заболеваний. Все определяется врачом на консультации после сбора анамнеза, осмотра и оценки результатов диагностики.
Послеоперационная реабилитация
Пациент выписывается через 2 суток после операции, а вставать и ходить можно уже на следующий день. В первые 2-3 дня могут беспокоить неприятные ощущения в области разреза, который окончательно заживает через 5-7 дней. В течение 2 недель рекомендуется исключить большую физическую нагрузку.
На вопросы отвечает:
Запишитесь на прием через заявку или по телефону +7 (495) 788-33-88
+7 (495) 788 33 88
Мы работаем каждый день:
- Понедельник—пятница: 8.00—20.00
- Суббота: 8.00—18.00
- Воскресенье: выходной
Ближайшие к клинике станции метро и МЦК:
- Шоссе энтузиастов или Перово
- Партизанская
- Шоссе энтузиастов
Схема проезда
В Российской Федерации, как и во многих экономически развитых странах мира, основной причиной смертности населения остается ишемическая болезнь сердца (ИБС) [1]. В этой ситуации огромное значение имеет реализация основных положений рекомендаций экспертов по диагностике и современному лечению больных с ИБС. В последние годы все более широко используются чрескожные коронарные вмешательства (ЧКВ), направленные на полное или частичное восстановление коронарного кровотока. Первичная ангиопластика в остром периоде инфаркта миокарда (ИМ) с подъемом сегмента ST снижает смертность и риск повторного ИМ [2]. Кроме того, у больных с нестабильной стенокардией и ИМ без подъема сегмента ST проведение ЧКВ также сопровождается улучшением краткосрочного и отдаленного прогноза [3]. В то же время оптимальная современная стратегия применения инвазивного лечения ИБС вне обострения, т.е. при стабильной стенокардии, и влияние на прогноз до сих пор точно не определены. Частично это связано со значительным прогрессом как в области медикаментозного, так и инвазивного лечения, произошедшим за последние два десятилетия (табл. 1).
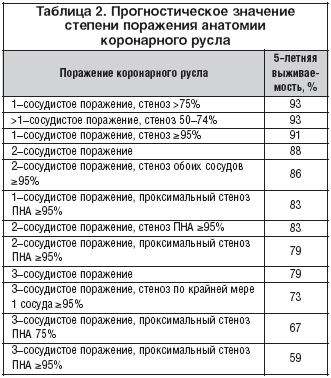
Существует ряд теоретических предпосылок для положительного влияния ЧКВ на прогноз пациентов со стабильной ИБС. Доказана четкая связь степени выраженности каждого отдельного гемодинамически значимого стеноза при коронароангиографии (КАГ), а также количества пораженных артерий и риска развития отдаленных неблагоприятных событий (табл. 2) [4].
Выявление ишемии миокарда у больных с подтвержденной или предполагаемой ИБС увеличивает риск общей и сердечно–сосудистой смертности, частоты развития ИМ, даже при отсутствии стенокардии. Проведение реваскуляризации у бессимптомных больных со значительной массой ишемизированного миокарда приводит к улучшению их отдаленного прогноза. С другой стороны, отрицательный тест на ишемию при нагрузочной сцинтиграфии миокарда даже при наличии болевого синдрома в грудной клетке является маркером благоприятного отдаленного прогноза. Кроме того, ишемия миокарда является пусковым механизмом, запускающим полиморфную желудочковую тахикардию/фибрилляцию желудочков и, соответственно, приводит к развитию внезапной смерти. Поэтому неудивительно, что степень поражения коронарного русла коррелирует с выживаемостью в отдаленном периоде. Учитывая указанные теоретические предпосылки, были проведены несколько клинических исследований, в которых сравнивались консервативная – оптимальная медикаментозная терапия (ОМТ) и инвазивная тактики, при которой наряду с ОМТ проводилось ЧКВ.
Современная ОМТ
В соответствии с рекомендациями по лечению больных ИБС для снижения риска развития осложнений используются такие классы препаратов, как антитромбоцитарные (ацетилсалициловая кислота, клопидогрел), липидснижающие (статины и др.), ингибиторы ангиотензинпревращающего фермента (АПФ), β–блокаторы (после перенесенного ИМ).
Для лечения стенокардии применяются препараты, направленные либо на увеличение доставки кислорода к сердечной мышце, либо на уменьшение потребности в нем миокарда (табл. 3). Препараты, традиционно используемые для этих целей, – β–блокаторы, антагонисты кальция и нитраты, оказывают свое антиангинальное/антиишемическое действие через изменение гемодинамических параметров деятельности сердца (ЧСС, коронарный кровоток, пред– и постнагрузка и др.) и АД, а также средства метаболического или цитопротективного действия.
β–блокаторы уменьшают ЧСС и АД во время нагрузки, задерживают или предотвращают развитие болей и ишемических изменений по данным ЭКГ. При подборе дозы ориентируются на частоту приступов, обычно стараются замедлить ЧСС до 55–60 уд./мин. Антагонисты кальция обычно назначаются при недостаточном антиангинальном эффекте нитратов или β–блокаторов. Этот класс препаратов обладает различным гемодинамическим эффектом (группа дигидропиридинов и препараты с ритм–замедляющими эффектами – верапамил и дилтиазем) и, соответственно, спектром побочного действия, что необходимо учитывать при выборе препарата. Антагонисты кальция, в основном верапамил и дилтиазем, особенно показаны для лечения вазоспастической стенокардии. При применении нитратов уменьшаются частота и тяжесть приступов стенокардии, однако назначение длительно действующих нитратов после перенесенного ИМ не приводит к улучшению прогноза. При развитии толерантности к нитратам ухудшается контроль за приступами стенокардии.
Ивабрадин – ингибитор If–тока клеток синусового узла, рекомендуется для клинического применения как антиангинальное средство у больных стабильной стенокардией с синусовым ритмом как при непереносимости или противопоказаниях к применению β–блокаторов, так и для совместного применения с β–блокаторами, если последние не контролируют ЧСС, а увеличение их дозы невозможно.
Активатор калиевых каналов – препарат никорандил – одновременно обладает свойствами органических нитратов и активирует АТФ–зависимые калиевые каналы. Никорандил расширяет коронарные артериолы и вены, воспроизводит защитный эффект ишемического прекондиционирования.
Миокардиальный цитопротектор триметазидин в монотерапии и в комбинации с любым из антиангинальных средств не только уменьшает количество приступов стенокардии и число потребляемых таблеток нитроглицерина, но и достоверно увеличивает время физической нагрузки на велоэргометре и тредмиле, объем выполненной работы, толерантность к физической нагрузке. Триметазидин может с успехом применяться у лиц пожилого и молодого возраста, с нарушениями углеводного обмена и при сопутствующей недостаточности кровообращения. Получены данные о том, что триметазидин до и после процедур реваскуляризации миокарда может оказать благоприятное влияние на ишемическое повреждение миокарда и быть эффективным в лечении стенокардии, возобновившейся после ЧКВ.
Первые исследования по изучению влияния ЧКВ на отдаленный прогноз у больных стабильной ИБС
В исследовании ACME [5] пациенты с одно– и двухсосудистым поражением и верифицированной ишемией миокарда или перенесенным ИМ в анамнезе при наличии подходящих для ЧКВ стенозов были рандомизированы к медикаментозной терапии, или им выполнялась транслюминальная баллонная коронарная ангиопластика (ТБКА). При анализе больных с однососудистым поражением оказалось, что в группе ТБКА через 6 мес. было достоверно больше пациентов без приступов стенокардии (64 против 46%), что сопровождалось большей толерантностью к физической нагрузке. Вместе с тем достоверной разницы при длительном наблюдении отмечено не было. Через 3 года наблюдения преимущество ТБКА перед медикаментозной терапией по приступам стенокардии сохранялось, и также без влияния на прогноз. В подгруппе пациентов с двухсосудистым поражением через 6 мес. ТБКА и медикаментозная терапия были одинаково эффективны в плане избавления от стенокардии, повышения толерантности к физической нагрузке и качества жизни.
В крупном исследовании RITA–2 (1018 участников) пациенты со стенозами коронарных артерий, подходящими для проведения ЧКВ, были рандомизированы в группу медикаментозного лечения, или им дополнительно проводилась ТБКА [6]. У значительного числа включенных больных было многососудистое поражение (40%), в том числе у 34% – гемодинамически значимое поражение проксимального сегмента передней нисходящей артерии. Через 3 мес. у пациентов в группе инвазивного лечения на 16,5% реже встречалась стенокардия II–IV ФК (р=0,001), достоверно выше (на 35 с) было общее время нагрузки при повторном проведении нагрузочной пробы, а также выше качество жизни. В группе медикаментозной терапии 23% пациентов потребовалось проведение ТБКА вследствие неэффективности медикаментозного лечения. Однако через 2,7 лет наблюдения в группе ТБКА суммарная частота смерти/ИМ была достоверно выше (6,3 против 3,3%) в группе консервативной терапии за счет частоты перипроцедуральных ИМ; разница по частоте стенокардии снизилась до 7,6%, хотя и сохранялась достоверность в пользу ТБКА. При более длительном (7–летнем) наблюдении частота смерти/ИМ между группами уже достоверно не различалась.
В исследовании MASS (у пациентов с поражением проксимального отдела передней нисходящей артерии) и MASS II (у пациентов с многососудистым поражением) ТБКА была также более эффективной в плане уменьшения симптомов стенокардии и показателей нагрузочных проб как через 12 мес., так и при длительном наблюдении (4–5 лет). При этом достоверной разницы по частоте развития смерти/ИМ между группой медикаментозной терапии и ТБКА отмечено не было [7,8]. У пожилых больных в исследовании TIME (старше 75 лет) лечение с помощью ЧКВ снова оказалось более эффективным, чем медикаментозная терапия в плане уменьшения приступов стенокардии и улучшения качества жизни. Указанная разница сохранилась и после 4 лет наблюдения [9].
Все ранее описанные исследования были проведены до внедрения в клиническую практику стентов и современных стандартов медикаментозного лечения. Кроме того, число включенных больных не позволяло сделать точный вывод при сравнении влияния ЧКВ и медикаментозной терапии на отдаленный прогноз.
Современные исследования
по изучению влияния ЧКВ на прогноз при стабильной ИБС
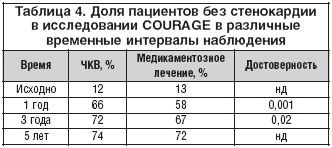
Наиболее современными и крупными из завершенных на данный момент исследований являются COURAGE, BARI 2D, JSAP. В исследование COURAGE было включено 2287 пациентов с ишемией миокарда, доказанной при проведении нагрузочных проб, и гемодинамически значимыми стенозами, выявленными во время КАГ [10]. После заключения экспертов о том, что выявленные стенозы подходят для проведения ЧКВ, больные были рандомизированы к ОМТ, или помимо ОМТ им дополнительно проводилось ЧКВ. ОМТ включала в себя антиангинальные препараты, антиагреганты, агрессивную липидснижающую и гипотензивную терапию. Важной особенностью исследования было частое (90%) применение стентов, хотя стенты с лекарственным покрытием использовались менее чем в 3% случаев. В течение длительного периода наблюдения (в среднем 4,6 лет) достоверной разницы по частоте смерти, развития ИМ, инсульта, потребности в госпитализации из–за развития ОКС отмечено не было. Как и ожидалось, ЧКВ оказалось более эффективным в плане избавления от стенокардии (табл. 4), а также повышения качества жизни (согласно различным опросникам), однако через 5 лет разница и по уровню качества жизни, и доле пациентов без стенокардии между группами не различалась, во многом за счет высокой частоты внеплановой реваскуляризации в группе исходно медикаментозного лечения вследствие развития рефрактерной стенокардии (33% в группе ОМТ и 21% в группе ЧКВ, р<0,001).
Надо отметить, что в исследование COURAGE не включались пациенты высокого риска. Так, в частности, критериями исключения в нем было сохранение стенокардии IV ФК, несмотря на проведение антиангинальной терапии, не включались также пациенты, у которых во время нагрузочной пробы отмечалась резко положительная проба (выраженная депрессия сегмента ST или падение АД на первой стадии нагрузки), пациенты с недавно перенесенным ИМ, у которых сохранялись приступы покоя, пациенты со сниженной ФВ, а также больные, у которых в предшествующие 6 мес. проводилось ЧКВ или КШ, больные с гемодинамически значимым поражением ствола ЛКА. Частота включения больных с 3–сосудистым поражением также была низкой – 30%. Кроме того, рандомизация проводилась после проведения КАГ, что снизило число пациентов с критическими стенозами, т.к. врачам–исследователям психологически было трудно их рандомизировать в исследование, где с 50% вероятностью они могли попасть в группу медикаментозного лечения.
Интересные данные были получены при отдельном анализе небольшой группы (n=300) пациентов, участвовавших в исследовании COURAGE, которым проводилась сцинтиграфия миокарда. Оказалось, что у небольшой группы пациентов (n=100) с большой и умеренной областью ишемии (с 10% и более объемом ишемизированного миокарда, согласно данным исходной сцинтиграфии миокарда) проведение ЧКВ привело к более выраженному снижению объема ишемизированного миокарда, что сопровождалось достоверным снижением смертности и частоты ИМ.
В исследование BARI 2D было включено 2368 пациентов со стабильной ИБС, страдающих СД 2 типа [11]. Пациенты были рандомизированы к ОМТ, или помимо ОМТ им проводилась реваскуляризация миокарда в виде ЧКВ или коронарного шунтирования (КШ) на усмотрение лечащего врача. Через 5 лет выживаемость между группами достоверно не различалась: 88,3% в группе реваскуляризации и 87,8% в группе медикаментозного лечения (p=0,97). Доля пациентов без неблагоприятных сердечно–сосудистых событий (смерть, ИМ, инсульт) также достоверно не различалась (77,2% в группе реваскуляризации против 75,9% в группе медикаментозной терапии, p=0,70). При отдельном анализе групп ЧКВ и медикаментозной терапии также достоверной разницы выявлено не было. Таким образом, в группе больных СД 2 типа проведение ЧКВ также не приводит к улучшению отдаленного прогноза по сравнению с ОМТ.
В относительно небольшом рандомизированном исследовании JSAP (Japanese Stable Angina Pectoris), проведенном в Японии, 384 пациента со стабильной ИБС низкого риска, направляемые лечащими врачами на инвазивное лечение, были рандомизированы к проведению ОМТ, или наряду с ОМТ им выполнялось ЧКВ [12]. Через 3,3 года наблюдения частота смерти достоверно не различалась между группами (2,9% в группе инвазивного лечения против 3,9% в группе ОМТ), однако частота комбинированной конечной точки (смерть + ОКС) достоверно реже встречалась в группе инвазивного лечения (7,9 и 14,9%, p=0,018). Недостатком данного исследования является небольшое число включенных пациентов, а также использование внутрисосудистого ультразвукового исследования при всех ЧКВ. Этим объясняется увеличение частоты первоначального успеха ЧКВ в исследовании JSAP (99,5%) по сравнению с COURAGE (93%), что, возможно, и является причиной различий в полученных результатах.
Результаты метаанализов
После публикации результатов исследований COURAGE, BARI 2D, JSAP был выполнен ряд метаанализов по той же тематике. В ряде из них были получены противоречащие COURAGE результаты. Так, в метаанализе A. Schomig и соавт., в который вошли данные 17 исследований, было выявлено 20% снижение общей смертности при проведении ЧКВ по сравнению с медикаментозной терапией [13]. Однако в указанный метаанализ был включен ряд исследований, в которых участвовали пациенты с недавно перенесенным ИМ, где ЧКВ, как было указано выше, улучшает прогноз пациентов, а также исследования пациентов с безболевой ишемией миокарда. Поэтому правомочность указанного метаанализа по отношению к больным со стабильной стенокардией вызывает сомнения. В метаанализ A. Jeremias был включен 13 121 пациент из исследований, где сравнивались реваскуляризация миокарда (ЧКВ или КШ) и медикаментозная терапия [14]. Согласно данным этого метаанализа, у больных после реваскуляризации миокарда отмечено снижение общей смертности, но не частоты ИМ. Указанный эффект был более выраженным в группе КШ по сравнению с ЧКВ (OP=0,62 95% CI 0,5–0,77 против OP=0,82 95% CI 0,68–0,99). При этом даже после исключения больных с недавним ИМ указанные различия сохранялись. В 2012 г. был выполнен еще ряд метаанализов, где были получены несколько иные результаты. В метаанализе, выполненном Stergiopoulos, проведение ЧКВ не только не привело к снижению смертности, ИМ и потребности в экстренной реваскуляризации, но и не оказалось более эффективным в плане снижения частоты стенокардии по сравнению с ОМТ [15]. Однако в данный метаанализ были включены не все исследования со стабильной ИБС, кроме того, в некоторые из них также были включены пациенты со стенокардией после перенесенного ИМ. Этого недостатка лишен метаанализ Pursnani, куда были включены исследования, в которых участвовали только пациенты со стабильной стенокардией и не включались больные с ОКС. Строгие критерии отбора больных только со стабильной ИБС, исключение пациентов с КШ, включение в анализ данных по длительности последующего наблюдения за больными делают данный метаанализ самым лучшим на данный момент [16]. Согласно полученным результатам, частота ССС при применении ЧКВ не снижается по сравнению с ОМТ, однако оно действительно на 20% снижает долю пациентов без стенокардии, при этом указанная разница сохранялась во всех проанализированных временных точках 1, 1–5 лет и 5 лет. Была выявлена также интересная временная закономерность: по мере включения более современных исследований, где чаще применялись стенты и более агрессивная медикаментозная терапия, влияние ЧКВ на улучшение прогноза уменьшалось.
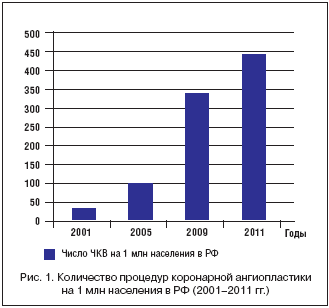
После публикации данных исследования COURAGE, BARI 2D, JSAP, а также указанных метаанализов во всем мире отмечается снижение частоты инвазивных вмешательств у больных со стабильной ИБС. Какие же тенденции наблюдаются в нашей стране? Согласно данным статистики, в РФ наблюдается непрерывный рост числа выполняемых ЧКВ [17]: с 2001 по 2011 г. отмечено 16–кратное увеличение числа выполняемых ЧКВ на 1 млн населения (рис. 1). Несмотря на это, мы все еще отстаем по данному показателю от многих стран Европы. Кроме того, доля ЧКВ, проводимых при ОКС, составляет всего 40,1% от всех ЧКВ при ИБС, что ниже среднеевропейского уровня, который составляет 60%. Т.е. в нашей стране сохраняется парадоксальная ситуация, когда в условиях ограниченного финансирования ЧКВ чаще применяется у больных со стабильной ИБС, где его прогностическая роль не ясна.
В то же время наблюдается рост приверженности пациентов к лечению препаратами, положительное влияние большинства из которых при стабильной ИБС не вызывает сомнений. Хотя надо отметить, что мы и по этим показателям отстаем от лучших центров США, где проводилось исследование COURAGE (табл. 5).
Таким образом, в настоящее время нет убедительных данных, что проведение ЧКВ у больных со стабильной ИБС, получающих ОМТ, приводит к снижению общей, сердечно–сосудистой смертности, нефатального ИМ или потребности в экстренной реваскуляризации. В то же время проведение ЧКВ приводит к значительному снижению выраженности стенокардии по сравнению с медикаментозной терапией. Следует отметить, что дискуссия о прогностическом влиянии ЧКВ продолжается. Критики исследования COURAGE утверждают, что незначительная частота использования СЛП, отсутствие СЛП нового поколения, которые, как было показано в ряде исследований, не только снижают частоту рестеноза стента, но и снижают частоту ИМ по сравнению с непокрытыми стентами и СЛП первого поколения, недостатки дизайна (в частности рандомизация после КАГ и нечеткие критерии ишемии), данные подысследования пациентов с большим объемом ишемизированного миокарда, не позволяет заключить, что данное исследование дало окончательный ответ на вопрос о влиянии ЧКВ на прогноз больных со стабильной ИБС. Кроме того, как уже отмечалось ранее, за последнее время произошел качественный скачок как в медикаментозном лечении, так и технике и фармакологии инвазивного лечения. Поэтому было инициировано крупнейшее исследование International Study of Comparative Health Effectiveness with Medical and Invasive Approaches (ISCHEMIA), в котором ЧКВ + ОМТ и ОМТ будут сравниваться у больных с верифицированной, по крайней мере умеренной, ишемией. При этом будет использоваться весь арсенал современной медикаментозной и инвазивной терапии (в частности СЛП). Планируется включить как минимум 8000 пациентов, что позволит определить даже небольшую разницу в исходах [20].
Литература
1. The World Health Organization the top ten causes of death fact sheet. 2004. Available at: http://www.who.int/mediacentre/factsheets/fs310/en/ index.html. Accessed February 2, 2012.
2. Ribeiro E.E., Silva L.A., Carneiro R. et al. Randomized trial of direct coronary angioplasty versus intravenous streptokinase in acute myocardial infarction // J. Am. Coll. Cardiol. 1993. Vol. 22. P. 376–380.
3. The Fragmin and Fast Revascularization During Instability in Coronary Artery Disease (FRISC) Investigators. Invasive compared with non–inva–sive treatment in unstable coronary–artery disease: FRISC–II prospective randomised multicentre study // Lancet. 1999. Vol. 354. P. 708.
4. 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention: A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the Society for Cardiovascular Angiography and Interventions // Circulation. 2011. Vol. 124(23). P. e574–e651.
5. Folland E.D., Hartigan P.M., Parisi A.F. Percutaneous transluminal coronary angioplasty versus medical therapy for stable angina pectoris: outcomes for patients with double–vessel versus single–vessel coronary artery dis–ease in a Veterans Affairs Cooperative randomized trial. Veterans Affairs ACME InvestigatorS // J. Am. Coll. Cardiol. 1997. Vol. 29. P.1505–1511.
6. Coronary angioplasty versus medical therapy for angina: the second Randomised Intervention Treatment of Angina (RITA2) trial // Lancet. 1997. Vol. 350. P. 461468.
7. Hueb W.A., Soares P.R., Almeida De Oliveira S. et al. Five–year follow–op of the medicine, angioplasty, or surgery study (MASS): A prospective, random¬ized trial of medical therapy, balloon angioplasty, or bypass surgery for single proximal left anterior descending coronary artery stenosis // Circulation. 1999. Vol. 100(19 Suppl). P. II107–II113.
8. Hueb W., Lopes N.H., Gersh B.J. et al. Five–year follow–up of the Medicine, Angioplasty, or Surgery Study (MASS II): a randomized controlled clinical trial of 3 therapeutic strategies for multivessel coronary artery disease // Circulation. 2007. Vol.115. P.1082–1089.
9. Pfisterer M. Trial of Invasive versus Medical therapy in Elderly patients Investigators. Long–term outcome in elderly patients with chronic an¬gina managed invasively versus by optimized medical therapy: four–year follow–up of the randomized Trial of Invasive versus Medical therapy in Elderly patients (TIME) // Circulation. 2004. Vol. 110. P.1213–1218.
10. Boden W.E., O’Rourke R.A., Teo K.K. et al. Optimal medical therapy with or without PCI for stable coronary disease // N. Engl. J. Med. 2007. Vol. 356. P. 15031516.
11. Dagenais G.R., Lu J., Faxon D.P. et al. Bypass Angioplasty Revascularization Investigation2 Diabetes (BARI 2D) Study Group. Effects of optimal medical treatment with or without coronary revascularization on angina and subsequent revascularizations in patients with type 2 diabetes mellitus and stable ischemic heart disease // Circulation. 2011. Vol. 123. P.1492–1500.
12. Nishigaki K., Yamazaki T., Kitabatake A. et al. Japanese Stable Angina Pectoris Study Investigators. Percutaneous coronary intervention plus medical therapy reduces the incidence of acute coronary syndrome more effectively than initial medical therapy only among patients with low–risk coronary artery disease a randomized, comparative, multicenter study // JACC Cardiovasc. Interv. 2008. Vol. 1. P. 469–479.
13. Schomig A., Mehilli J., de Waha A. et al. A meta–analysis of 17 randomized trials of a percutaneous coronary intervention–based strategy in patients with stable coronary artery disease // J. Am. Coll. Cardiol. 2008. Vol. 52.
14. Jeremias A., Kaul S., Rosengart T.K. et al. The impact of revascularization on mortality in patients with nonacute coronary artery disease // Am. J. Med. 2009. Vol. 122. P. 152–161.
15. Stergiopoulos K., Brown D.L. Initial coronary stent implantation with medical therapy vs medical therapy alone for stable coronary artery disease // Arch. Intern. Med. 2012. Vol. 172. P. 312–319.
16. Pursnani S., Korley F., Gopaul R. et al. Coronary Intervention Versus Optimal Medical Therapy in Stable Coronary Artery Disease. A Systematic Review and Meta–Analysis of Randomized Clinical Trials. // Circ. Cardiovasc. Interv. 2012. Vol. 5. P. 476–490.
17. Бокерия Л.А., Алекян Б.Г. Рентгенэндоваскулярная диагностика и лечение заболеваний сердца и сосудов в Российской Федерации – 2011 год.– М.: Издательство НЦССХ им. А.Н. Бакулева РАМН, 2012.
18. Карпов Ю.А., Самко А.Н., Буза В.В. Коронарная ангиопластика и стентирование. – М.: Медицинское информационное агентство, 2010.
19. Karpov Y., Buza V. Pre–procedure C–reactive Protein and Erythrocyte Sedimentation Rate but not Lipoprotein–associated Phospholipase A2 Predict Clinical Outcomes after Drug–eluting Stents Implantation in Patients with Stable Coronary Disease on Chronic Statin Therapy .. AHA 2012. Abstract Poster Board Number: 2026.
20. International Study of Comparative Health Effectiveness with Medical and Invasive Approaches (ISCHEMIA) home page. 2012. Available at: https://www.ischemiatrial.org. Accessed June 11, 2012.

Развитие медицинских технологий позволило минимизировать операционную травму с помощью эндоваскулярных вмешательств через прокол кожи и без разрезов. Основными эндоваскулярными операциями являются ангиопластика нижних конечностей и установка стентов в сосуд. Смысл ангиопластики сосудов заключается в раздувании суженного или закупоренного сегмента с помощью специального баллона, проводимого по тонкому проводнику. После ангиопластики в просвет восстановленного сосуда для поддержания стенки может устанавливаться специальная металлическая сетка — стент. Исторически для разрушения бляшки в сосудах использовалась лазерная ангиопластика, однако она уступила место новым, совершенным эндоваскулярным инструментам.
Эндоваскулярные технологии в Инновационном сосудистом центре
Основной миссией нашей клиники является лечение критической ишемии и гангрены конечностей. Мы стремимся к использованию новейших подходов для решения этой задачи. С 2011 года в практику наших сосудистых хирургов внедрены методы эндоваскулярной хирургии при критической ишемии. Отмечая преимущества эндоваскулярного подхода, мы с каждым годом расширяем возможности нашей клиники в применении данных методов.
Роль малоинвазивных технологий растёт — сейчас более 50% с критической ишемией и гангреной оперируется эндоваскулярно, а ещё более, чем у 40% применяется гибридный подход. Это шунтирование с ангиопластикой и стентированием артерий нижних конечностей. Инновационный сосудистый центр — это клиника, где делают более 500 операций ангиопластики и стентирования артерий нижних конечностей в год.
Возможности эндоваскулярной хирургии развиваются синхронно с созданием инновационных инструментов для лечения, поэтому в нашей практике операции через прокол всё больше вытесняют открытые вмешательства.
 Виды стентов
Виды стентов
Самораскрывающиеся стенты являются более предпочтительными для протяжённого поражения, извитых сосудов и в местах предполагаемого внешнего воздействия — сгибы и скручивания. Они идеально подходят для бедренно-подколенных поражений, но имеют высокую стоимость Такие стенты сделаны из металла с памятью формы и при раскрытии занимают свободный просвет. С целью лучшего прилегания после установки стенты дополнительно раздуваются баллоном.
Баллонные расширяемые стенты рекомендованы при выраженном кальцинировании стенки сосуда. Они подходят для идеально точного расположения и не смещаются при установке.
Баллоны и стенты с лекарственным покрытием пришли из коронарной ангиопластики и могут применяться при повторных вмешательствах на артериях голени. Они меньше склонны к зарастанию неоинтимой. Цены на ангиопластику нижних конечностей во многом зависят от выбора инструмента и его производителя.
Подготовка к стентированию
Перед выполнением операции стентирования пациент должен быть соответствующим образом обследован на предмет сосудистых поражений, рисков осложнений. Должен быть выполнен комплекс лабораторных обследований перед операцией и коагулограмма. Учитывая нагрузку пациента антитромботическими препаратами, необходимо исключить возможные источники кровотечения (язву желудка, кровоточащий геморрой).
Накануне вмешательства вводится лёгкий седативный препарат, позволяющий пациенту хорошо поспать и не нервничать. Перед операцией пациенту выбривается место предполагаемого доступа. В предоперационной сестра установит мочевой катетер и внутривенную иглу для инфузий. В операционной на плечо накладывается манжета для измерения давления и датчики для непрерывного снятия ЭКГ фиксируются на груди.
Анестезия при стентировании
Большинство эндоваскулярных процедур ангиопластики и стентирование сосудов нижних конечностей могут быть выполнены с умеренной внутривенной седацией и местной анестезией в месте прокола для доступа. Обязательно проводится мониторинг артериального давления, электрокардиограммы и уровня насыщения крови кислородом (пульсоксиметрия). На случай непредвиденных осложнений в операционной имеется дыхательный аппарат и дефибриллятор. Если операция проводится по поводу критической ишемии, то для комфортного положения пациента проводится эпидуральная анестезия (введение через катетер в область позвоночника анестезирующего препарата).
 Как проходит ангиопластика сосудов нижних конечностей
Как проходит ангиопластика сосудов нижних конечностей
Для проведения оперативного вмешательства на артериях нижних конечностей пациент укладывается в положении лёжа на спине с руками по бокам. Если предполагается плечевой доступ через локтевую ямку, то рука отводится на 45-90º от пациента для удобства пункции. Чаще применяется доступ через бедренную артерию, но возможен и ретроградный доступ через сосуды на стопе.
Чрескожная ангиопластика начинается доступом к сосуду по пульсации, а если она отсутствует, то пункция проводится по анатомическим ориентирам, но в нашей клинике для доступа используется ультразвуковое сканирование в B-режиме. После попадания иглой в сосуд проводится тонкий проводник, по которому устанавливается специальная трубочка — интрадьюссер с клапаном на конце и возможностью промывания. Затем выполняется введение контраста — ангиография для уточнения тактики операции. Проводник проводится до места сужения, преодолевает это сужение и проводится дальше. После прохождения всех сужений по проводнику проводится баллон, который раздувается и моделирует просвет сосуда (ангиопластика). После этого проводится контрольная ангиография и если выявляется расслоение стенки артерии, то в это место необходимо установить стент, подходящий по диаметру.
Виды ангиопластики
- Субинтимальная баллонная ангиопластика сосудов — проводник проводится под изменённой внутренней стенкой (интимой) сосуда и дальше выходит в свободный просвет.
- Интралюминарная ангиопластика — разновидность вмешательства, когда проводник проходит по естественному просвету артерии, проскальзывая через суженные и закупоренные участки.
- При лазерной ангиопластике — атеросклеротическая бляшка выжигается специальным лазерным катетером.
Баллонная ангиопластика артерий нижних конечностей без стентирования рекомендуется для лечения поражений голени. Обязательно надо стентировать подвздошные артерии, так как частота повторных сужений (рестенозов) без стента очень высока.
После проведения ангиопластики и стентирования обязательно проводится контрольная ангиография для оценки результата.
Возможные осложнения
Осложнения после баллонной ангиопластики сосудов нижних конечностей обычно развиваются в ходе проведения вмешательства и должны немедленно устраняться. Способы для устранения этих осложнений имеются в арсенале сосудистых хирургов. Чаще всего наблюдаются следующие осложнения:
- Кровотечение из места доступа (гематома или псевдоаневризма) — чаще всего бывает при нарушении пациентом постельного режима. Иногда требует открытого доступа для устранения источника кровотечения.
- Инфекция места пункции — очень редкое осложнение. Она может развиваться при тяжёлых гнойно-деструктивных процессах на нижней конечности. Лечить необходимо антибиотиками. При необходимости проводить вскрытие гнойного очага.
- Повреждение почек контрастом — редкое осложнение от контрастного вещества.
- Диссекция (расслоение) артерии — иногда наблюдается при сложных поражениях и попытках субинтимального прохождения. Чаще всего удаётся устранить с помощью установки стента.
- Закупорка артериального русла кусочками бляшки — может определяться при контрольной ангиографии.
- Перелом стента в местах его изгиба — позднее осложнение, связанное с механической нагрузкой на металл.
- Повторное сужение в месте установки стента (рестеноз) — процесс зарастания просвета стентированного сегмента.
- Разрыв артерии — осложнение, развивающееся из-за избыточного раздувания баллона в резко кальцинированном сосуде. Выявляется в ходе контрольной ангиографии. Часто удаётся стабилизировать ситуацию длительной экспозицией баллона, может потребоваться установка стент-графта или открытая операция.
- Спазм артерий — реакция на раздувание сосуда баллонном. Встречается в 10% процедур. Для устранения спазма могут вводиться лекарственные препараты (папаверин, нитроглицерин).
Частота всех осложнений составляет не более 5% от всех проведённых процедур и они обычно своевременно устраняются в ходе вмешательства.
Наблюдение после ангиопластики и стентирования
В нашей клинике принята схема ведения пациента после операции для исключения осложнений ангиопластики и стентирования периферических артерий нижних конечностей:
- Для лучшего результата показана двойная дезагрегантная терапия, включающая приём плавикса и аспирина. Медикаментозная профилактика играет важную роль в отдалённых результатах вмешательства и продолжительности жизни пациентов.
- Первый осмотр проводится в первые 2 недели послеоперационного периода с обязательным УЗИ периферических сосудов.
- Следующие осмотры проводятся через несколько месяцев.
- Через год после хирургического лечения обязательно делают МСКТ ангиографию ног.
Баллонная ангиопластика и стентирование артерий нижних конечностей является эффективным методом восстановления кровотока при большинстве окклюзионных поражений кроме подколенной артерии. По своим непосредственным результатам этот метод не уступает открытым операциям шунтирования, если проводится по строгим показаниям. Преимуществом эндоваскулярной хирургии является малая травматичность, отсутствие боли, возможность повторных вмешательств, а также меньший риск для жизни.
По мере совершенствования инструментария для ангиопластики и стентирования малоинвазивные вмешательства занимают всё большее место в ведении пациентов с критической ишемией и гангреной.
В диагностике злокачественных опухолей и ряда других заболеваний ключевую роль играет патоморфологическая верификация диагноза с помощью биопсии. Врач должен получить образец патологически измененной ткани и отправить в лабораторию для гистологического исследования. Это помогает установить тип опухоли, правильно составить программу лечения, определить показания к назначению иммунотерапии, таргетной терапии. Существуют разные способы забора материала. При новообразованиях брюшной полости и забрюшинного пространства зачастую прибегают к чрескожной биопсии с помощью специальных игл.
Наш эксперт в этой сфере:
Рябов Константин Юрьевич
Хирург, онколог, эндоскопист
Существуют две методики:
- Тонкоигольная аспирационная биопсия — наиболее простая и наименее инвазивная процедура, которую можно выполнить в амбулаторных условиях. Суть метода в том, что врач вводит в опухоль тонкую иглу под контролем УЗИ. Когда игла оказывается в нужном месте, ее соединяют со шприцем и путем потягивания за поршень получают образец ткани. Тонкоигольная чрескожная биопсия имеет множество преимуществ, но у нее есть один существенный недостаток: с помощью нее удается получить лишь небольшое количество материала. Можно провести только цитологическое исследование, чтобы установить, присутствуют ли в образце злокачественные клетки. Приготовить из ткани парафиновый блок, провести
молекулярно-генетические и иммуногистохимические исследования практически невозможно. - Чрескожная трепан-биопсия зачастую представляет собой «золотую середину»: это малоинвазивное вмешательство, его проводят под местной анестезией, но с помощью него можно получить достаточно большое количество материала и провести все необходимые исследования. Процедуру выполняют с помощью специальной толстой иглы, которая позволяет получить столбик ткани.
Для чего проводят чрескожную биопсию органов брюшной полости и забрюшинного пространства?
Данное исследование помогает решать важные диагностические задачи:
- подтвердить злокачественный характер опухоли и установить ее тип;
- отличить доброкачественное новообразование от злокачественного;
- правильно определить показания к хирургическому вмешательству, спланировать тактику лечения;
- провести
молекулярно-генетические , иммуногистохимические анализы опухолевой ткани и правильно подобрать таргетные препараты, иммунопрепараты; - спланировать лечение при опухолях с неизвестной первичной локализацией;
- установить точный диагноз при диффузных поражениях паренхиматозных органов, таких как печень, почки.
С помощью чрескожной пункции можно провести биопсию печени и поджелудочной железы, почек, яичников, надпочечников, предстательной железы, лимфатических узлов, образований в мягких тканях. Эту процедуру не проводят при новообразованиях в полых органах, например, желудке, толстой кишке — потому что тут намного проще и безопаснее получить образец ткани во время эндоскопического исследования.
Противопоказания
Противопоказаний к чрескожной биопсии органов брюшной полости и забрюшинного пространства немного:
- Неконтролируемые коагулопатии — тяжелые нарушения свертываемости крови, которые грозят опасным кровотечением во время процедуры. Пункция внутренних органов противопоказана пациентам с уровнем тромбоцитов менее 50×109/л и международным нормализованным отношением более 1,6. Перед манипуляцией это нарушение должно быть устранено. Например, в ряде случаев показано переливание кровекомпонентов.
- Невозможность найти безопасный путь для иглы, когда на ее пути находятся органы, повреждение которых грозит опасными осложнениями, крупные кровеносные сосуды. В таких случаях оптимальным способом получить образец ткани может стать тонкоигольная биопсия под контролем
эндо-УЗИ . - Возбужденное состояние пациента, неконтролируемая двигательная активность при некоторых психических, неврологических расстройствах. Решением этой проблемы может стать применение общей анестезии.
Врачи в Международной клинике Медика24 всегда тщательно оценивают состояние пациентов перед инвазивными процедурами, учитывают возможные риски и принимают необходимые меры, чтобы их минимизировать.
Закажите обратный звонок. Мы работаем круглосуточно
Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Подготовка к процедуре
Во время предварительной консультации врач выясняет, какими хроническими заболеваниями страдает пациент, какие он принимает лекарственные препараты, нет ли у него аллергии на лекарства. Если пациент принимает антикоагулянты (препараты для снижения свертываемости крови) или нестероидные противовоспалительные средства, такие как аспирин, то обычно пункцию проводят не менее чем через пять дней после их отмены.
Обычно тонкоигольная и
До проведения биопсии важно спланировать наиболее безопасное место и направление введения иглы. Для этого применяют компьютерную томографию,
томографию. Важно убедиться, что на пути иглы нет других органов, крупных кровеносных сосудов.
Также врач должен правильно выбрать метод навигации. Чаще всего чрескожную биопсию проводят под контролем УЗИ. Это наиболее простой, доступный и недорогой метод. Но в некоторых случаях целесообразно проведение биопсии под
Как выполняют чрескожную биопсию органов брюшной полости и забрюшинного пространства?
Во время процедуры пациента укладывают в определенное положение, в зависимости от того, в каком месте планируется вводить иглу. Место пункции обрабатывают раствором антисептика, проводят местную анестезию. Если биопсия проводится под контролем УЗИ, то чаще всего врачи используют метод «свободной руки»: одной рукой доктор держит датчик, а второй вводит иглу. Эта техника требует соответствующих навыков и опыта. Работа рук врача должна быть хорошо скоординирована, чтобы игла постоянно полностью визуализировалась.
Во время биопсии под КТ навигацией пациент находится в кабинете компьютерной томографии на столе томографа. Выполняют снимки, чтобы определить расположение патологического образования, соседних анатомических структур и точно наметить путь иглы. Затем врач вводит иглу бля биопсии. По мере ее продвижения выполняют серию контрольных снимков. Когда игла попадает в нужное место, врач осуществляет забор материала. В некоторых случаях образцы тканей нужно получить из нескольких участков — это помогает обеспечить максимально точную диагностику.
После того как материал получен, врач извлекает иглу и накладывает на место прокола повязку.
В среднем процедура продолжается 30 минут, и в течение всего этого времени пациент должен находиться в неподвижном положении. Нельзя кашлять, делать глубокие резкие вдохи. Пункция обычно безболезненна, во время нее ощущается лишь давление. После биопсии, в зависимости от того, в какой орган вводилась игла, пациент должен находиться в стационаре от 2–4 часов до 1–2 суток. Сразу после процедуры выполняют ультразвуковую допплерографию — это исследование помогает обнаружить кровотечение.
После выписки можно заниматься привычными делами, в течение некоторого времени запрещаются интенсивные физические нагрузки. Если повысилась температура тела или появились другие симптомы — нужно немедленно обратиться к врачу.
Особенности чрескожной биопсии разных органов
Биопсию печени, в зависимости от того, в какой части органа находится опухоль, выполняют через прокол под нижним ребром или между ребрами. Во избежание риска сильного кровотечения, врач выбирает место введения иглы таким образом, чтобы она прошла через как можно больший объем нормальной печеночной ткани, но чтобы при этом на ее пути не было крупных кровеносных сосудов и желчных протоков.
Поджелудочная железа — один из самых «сложных» органов для чрескожной биопсии, так как она находится глубоко и окружена сетью кровеносных сосудов, другими органами. Зачастую оптимальным способом получить ткань для исследования является тонкоигольная биопсия под контролем эндосонографии. Если эту процедуру невозможно выполнить, или с помощью нее не удается получить достаточное количество клеток для исследования, в качестве альтернативы может быть выполнена чрескожная биопсия.
Чрескожная биопсия селезенки — процедура, которой многие врачи стараются избегать, так как опасаются риска тяжелого кровотечения. Однако, исследования показывают, что данная манипуляция, при правильном ее проведении, довольно безопасна, и частота осложнений невелика. В отличие от биопсии печени, направление введения иглы стараются выбрать так, чтобы было затронуто как можно меньше здоровой ткани органа. Чаще всего пункцию проводят в положении пациента на спине в межреберном промежутке слева. Но могут быть выбраны и другие позиции, в зависимости от локализации патологического образования в органе.
К чрескожной биопсии желчного пузыря прибегают редко
Биопсия почек часто применяется для диагностики
Во время биопсии надпочечников место пункции зависит от стороны поражения, локализации патологического образования и его размера. Чрескожную биопсию удобнее всего выполнять при поражении правого надпочечника чреспеченочным доступом, так как ткань печени служит хорошим ультразвуковым окном. Пункцию левого надпочечника проводят трансабдоминально в положении на спине или из заднего доступа в положении на животе.
Чрескожную биопсию кишечника выполняют очень редко. Если патологическое образование находится в толстой кишке, то безопаснее и проще получить образец ткани во время эндоскопии. Чрескожная пункция может потребоваться, когда опухоль локализуется глубоко под слизистой оболочкой или находится в тонкой кишке.
Чрескожная биопсия позволяет получать образцы ткани лимфоузлов, расположенных как недалеко от поверхности кожи, так и в брюшной полости, в области таза. При этом диаметр лимфатического узла должен быть не менее 1 см. В некоторых случаях более удобны другие доступы, например, через слизистую оболочку прямой кишки (трансректально).
Чрескожным доступом можно провести биопсию брюшины и сальника. Эти структуры в норме не видны во время УЗИ, но видны их патологически измененные утолщенные участки, узловые образования.
При подозрении на рак яичника гистологическое исследование обычно проводят после того, как пораженный орган удален. В редких случаях, если невозможно выполнить операцию, может быть принято решение провести биопсию во время диагностической лапароскопии или чрескожно.
Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Возможные осложнения
В целом чрескожная биопсия патологических образований брюшной полости и забрюшинного пространства является безопасной процедурой. Тем не менее, это инвазивное вмешательство, оно сопровождается небольшим риском осложнений. Чаще всего встречаются кровотечения, инфекционные осложнения, случайные повреждения внутренних органов, распространение опухолевых клеток вдоль введения иглы.
Частота кровотечений после пункционной биопсии внутренних органов составляет менее 3,5%. Свежая кровь выглядит на изображениях во время УЗИ так же, как ткань плотных органов, поэтому ее зачастую сложно обнаружить. Для этого применяют компьютерную томографию. Борьба с этим осложнением зависит от тяжести кровотечения. Например, в случае с селезенкой может потребоваться эмболизация сосудов или экстренное хирургическое удаление органа.
Чтобы минимизировать риск распространения злокачественных опухолей, при подозрении на рак врачи делают минимальное количество введений иглы.
Риск повреждения внутренних органов во время процедуры минимален, но он увеличивается, если пациент совершает движения, очень глубокие вдохи.
В Международной клинике Медика24 чрескожную биопсию внутренних органов выполняют ведущие врачи-специалисты с применением новейшего оборудования. В умелых руках эта манипуляция является безопасной и ценной диагностической процедурой, которая помогает установить точный диагноз и назначить пациенту оптимальное лечение.
Материал подготовлен врачом-онкологом, хирургом Международной клиники Медика24 Рябовым Константином Юрьевичем.
Чрескожная нефролитотрипсия надежна как для детей, так и для пациентов старшего возраста. Успешность лечения путем чрескожной нефролитотрипсии достигает 98%.

Рисунок. Нефроскоп, введенный в чашечно-лоханочную систему почки.
Показания к чрескожной нефролитотрипсии
- Различные врожденные и приобретенные, анатомические и функциональные нарушения оттока мочи. Наличие у пациента аномалий мочевыделительной системы препятствует самостоятельному отхождению фрагментов конкремента после дистанционной или трансуретральной нефролитотрипсии. В этом случае чрескожная нефролитотрипсия – наилучший выбор лечения камней в почках. Кроме того во время чрескожной нефролитотрипсии можно не только удалить камень, но и скорректировать некоторые аномалии мочевыделительной системы.
- Несмотря на то, что теоритически большие камни почки можно раздробить и дистанционно, эффективность лечения невысока и нередко требуются повторные процедуры. По этой причине, конкременты размером 2-3 см и более в диаметре лучше всего удалять путем чрескожной нефролитотрипсии.
- Коралловидные конкременты или камни в виде оленьего рога – сложная задача для хирургов. Чаще всего эти конкременты имеют инфекционную природу, но кальциевые, уратные и цистиновые конкременты могут заполнять чашечно-лоханочную систему почки и принимать форму коралла или оленьего рога. Полностью удалить их возможно путем чрескожной нефролитотрипсии.
- Особенности пациента. Иногда выраженное ожирение или аномалии расположения почек не позволяют направить ударные волны на камень для его дистанционного дробления. В этом случае показана чрескожная нефролитотрипсия. Однако выполнение чрескожной нефролитотрипсии будет возможно только в том случае, если длина нефроскопа больше, чем расстояние от кожи до почки.
- Расположение камня. Камни, расположенные в нижнем полюсе почки тяжело извлечь трансуретральным путем, кроме того вероятность самостоятельного отхождения фрагментов конкремента из нижнего полюса после дробления крайне мала. В таких случаях показана чрескожная нефролитотрипсия.
- Химический состав конкремента. Выше мы уже упоминали, что инфекционные камни должны удаляться только путем чрескожной нефролитотрипсии, так как этот способ позволяет извлечь все фрагменты камня до последнего. Еще одна проблема – это твердые камни, состоящие из кальций оксалатов. При дистанционной нефролитотрипсии тяжело раздробить очень твердые камни до фрагментов, которые смогут самостоятельно покинуть мочевыделительную систему, нередко требуется множество повторных процедур. Поэтому в таких случаях чрескожная нефролитотрипсия будет менее болезненной в сравнение с дистанционной нефролитотрипсией.
- Неудача при лечении путем дистанционной или трансуретральной нефролитотрипсии является показанием к чрескожной нефролитотрипсии.
Противопоказания к чрескожной нефролитотрипсии
Абсолютными противопоказаниями к чрескожной нефролитотрипсии является беременность и нарушения со стороны свертывающей системы крови.
Оборудование для чрескожной нефролитотрипсии

Рисунок. Процедура чрескожной нефролитотрипсии. Через просвет нефроскопа проведен литотриптер, посылающией ударные волны к конкременту.
Нефроскоп – эндоскопический инструмент, обеспечивающий выполнение различных лечебных и диагностических манипуляций в чашечно-лоханочной системе почки. Он представляет собой полый стержень, диаметр может варьировать в зависимости от вида нефроскопа. Нефроскоп оборудован волоконной оптикой и осветительными элементами, позволяющими получать изображение обследуемой области. В нефроскопе есть рабочий канал, через просвет которого к камню подводятся различные инструменты, в том числе и литотриптер.
Выделяют жесткие и гибкие нефроскопы. Для чрескожной нефролитотрипсии чаще используется жесткий нефроскоп. Хотя усовершенствование гибких нефроскопов значительно расширило круг их применения.
Литотриптер – инструмент для дробления камня. В настоящее время для чрескожной нефролитотрипсии широко применяется современный литотриптер, сочетающий в себе возможности ультразвукового и пневматического дробления камней. Лазерные литотриптеры используются для выполнения мини-перкутанной нефролитотрипсии или при операциях с использованием гибкого нефроскопа.

Рисунок. Современная установка, наиболее часто используемая для дробления конкрементов при чрескожной контактной нефролитотрипсии.
Подготовка к хирургическому вмешательству
Во-первых, перед операцией необходимо пройти стандартное обследование, включающее в себя общий анализ крови и мочи, исследование мочи на стерильность, биохимический анализ крови и коагулограмму, электрокардиограмму, при необходимости – рентген органов грудной клетки.
При наличии в моче признаков инфекции или обнаружении бактерий, за неделю до хирургического вмешательства врач назначит курс антибиотиков для очищения мочевыделительной системы от болезнетворных микроорганизмов.
Если вам прописаны препараты, разжижающие кровь, то за 7-10 дней до операции необходимо прекратить их прием, чтобы снизить вероятность кровотечения во время хирургического вмешательства.
Вечером накануне и утром в день операции, необходимо сделать очистительные клизмы. Это уменьшит загазованность кишечника, что в свою очередь сделает процесс установки нефроскопа более безопасным.
Установка нефроскопа выполняется через разрез кожи в поясничной области, поэтому перед хирургическим вмешательством волосяной покров в этой области необходимо сбрить.
Конечно же, перед хирургическим вмешательством вами побеседует хирург. Врач расскажет вам о том, как будет проходить операция, какие риски и осложнения существуют, как будет происходить период после операции. Не стесняйтесь задавать вопросы. В конце беседы необходимо будет подписать согласие на оперативное вмешательство.
Анестезия

Рисунок. Положение пациента при чрескожной нефролитотрипсии.
Чрескожная нефролитотрипсия начинается с оказания анестезиологического пособия. После этого в мочеточник вводится тонкий стент, а в мочевой пузырь устанавливается катетер для оттока мочи. Вас уложат на операционном столе в наиболее удобную для выполнения нефролитотрипсии позицию. Чрескожная нефролитотрипсия выполняется в положении лежа на животе, как показано на рисунке. В случае выраженного ожирения или противопоказаний со стороны сердечно-сосудистой или дыхательной систем, операция проводится в положении лежа на боку или на спине.
Установка нефроскопа в почку сопровождается рядом сложных технических и очень выверенных моментов:
Поясничная область обеззараживается и обкладывается стерильными пеленками. Сначала через небольшой разрез с помощью специального проводника под рентген контролем хирург проникает чашечно-лоханочную систему почки. Разрез расширяют с помощью специальных инструментов. Когда отверстие становиться достаточно большим, по проводнику в почку вводят нефроскоп. Проводник извлекают. Так как нефроскоп оборудован осветительными и оптическими элементами, теперь хирург может осмотреть глазом чашечно-лоханочную систему почки и установить место расположения камня. Обнаружив конкремент, врач дробит его с помощью литотриптера, после чего все фрагменты извлекаются. В конце операции устанавливается нефростомическая трубка или мочеточниковый стент для обеспечения нормального оттока мочи в первые дни после хирургического вмешательства.
После чрескожной нефролитотрипсии
Сразу после операции вас поместят в комнату пробуждения. После полного восстановления сознания вы сможете отправиться в свою палату.
Боль. При возникновении болевых ощущений обязательно скажите об этом медицинскому персоналу. Для уменьшения боли вам введут обезболивающие препараты.
Антибиотики. Антибиотик вводится в день операции. Кроме того необходимо принимать антибиотики и после чрескожной нефролитотрипсии для профилактики инфекционных осложнений.
Нефростомическая трубка, или нефростома. Если в конце операции вам установили нефростому, то в поясничной области у вас будет видна трубка, подсоединенная к пакету для сбора мочи. Через 1-2 дня трубка извлекается абсолютно безболезненно. В редких случаях требуется более длительное дренирование чашечно-лоханочной системы почки, в этом случае вас выпишут домой с нефростомой.

Рисунок. Нефростомическая трубка, присоединенная к мочеприемнику.
Стент. Если вам установили стент, а не нефростому, то первое время вы можете испытывать умеренный дискомфорт. Стент удаляется через 1-4 недели после операции.
Мочевой катетер. Мочевой катетер удаляют на следующий день после чрескожной нефролитотрипсии.
Физическая активность. Уже через несколько часов после операции, когда вы придете в сознание, вы сможете вставать с постели. На помощь вам могут прийти медицинский персонал или родственники. Важно как можно раньше восстановить физическую активность, это поможет избежать развития таких осложнений, как формирования сгустков в венах нижних конечностей.
Дома после чрескожной нефролитотрипсии
Болевой синдром. Первое время после чрескожной нефролитотрипсии может сохраняться незначительный дискомфорт или умеренные болевые ощущения, требующие приема обезболивающих препаратов. Перед выпиской врач пропишет вам болеутоляющие лекарства.
Душ и ванна. Дома вы можете смело принимать душ, лежать в ванне нежелательно. Если повязка на ране намокла, просто поменяйте ее на сухую.
Физическая активность. Ведите обычный образ жизни, конечно же, избегая тяжелых физических нагрузок. Врачи советуют не садиться за руль 1-2 недели после операции. К работе вы сможете вернуться через 1-2 недели после чрескожной нефролитотрипсии.
Удаление стента. Как мы говорили, стент удаляется через 1-4 недели после чрескожной нефролитотрипсии по указанию врача. Для удаления стента вам необходимо будет записаться на прием к врачу. Очень важно, чтобы вы вовремя удалили стент, длительное его стояние может привести к его инкрустации солями и камнями, инфекции или нарушению оттока мочи.
Уход за нефростомой. Если вас выписали домой с нефростомой, важно обеспечить адекватный уход за ней. Ежедневно следите за количеством отделяемой мочи, ее цветом. Первое время после операции в моче может быть примесь крови, это нормальное явление. Важно, чтобы нефростомическая трубка не забилась. Мешок для сбора мочи должен находиться ниже уровня почки. Кожа вокруг нефростомы необходимо ежедневно обрабатывать антисептическими растворами и укрывать стерильными повязками. Если у вас появилась температура, озноб, покраснение вокруг нефростомы, или прекратился отток мочи через трубку, незамедлительно обратитесь к врачу.

Рисунок. Нефростома прикрыта стерильной повязкой.
Осложнения чрескожной нефролитотрипсии
Частота возникновения осложнений чрескожной нефролитотрипсии невысока и составляет не более 3%. Частота тяжелых осложнений – 1%.
- Инфекционные осложнения, проявляющиеся ознобом, лихорадкой, тошнотой и рвотой, болями в поясничной области и др., нередкое осложнение у пациентов пренебрегающих антибиотикопрофилактикой до и после чрескожной нефролитотрипсии. Очень важно, чтобы перед операцией мочевыделительная система была стерильна, т.е. очищена от болезнетворных бактерий. После чрескожной нефролитотрипсии необходимо строго следовать рекомендациям врача по приему антибиотиков, что снизит вероятность инфекционных осложнений.
- Одним из редких осложнений на этапе установки нефроскопа является повреждение довольно крупных ветвей кровеносных сосудов. В таком случае операцию проходится прекращать, а в месте ранения сосуда раздувается баллон катетера на 2-3 дня.
- Так же в случае очень крупного камня возможны остаточные фрагменты в мочевыделительной системе, что потребует дальнейшего лечения.





 Виды стентов
Виды стентов Как проходит ангиопластика сосудов нижних конечностей
Как проходит ангиопластика сосудов нижних конечностей
